Clear Sky Science · sv
Målstyrd långläsningssekvensering för högupplöst kartläggning av repetitioner vid myoton dystrofi typ 1
Varför detta är viktigt för familjer och läkare
Vissa ärftliga sjukdomar drivs av staplingsliknande avsnitt i vårt DNA—korta sekvenser som upprepas hundratals eller till och med tusentals gånger. När dessa repetitioner blir för långa kan de orsaka allvarliga tillstånd som myoton dystrofi, en muskelförtvining. Att exakt mäta hur långa dessa repetitioner är, och hur de kemiskt märkts, är dock förvånansvärt svårt med dagens sjukhustester. Denna artikel presenterar ett strömlinjeformat sätt att läsa dessa svåråtkomliga DNA‑regioner i detalj på ungefär en dag, vilket kan ge läkare tydligare svar och patienter bättre vägledning.
En närmare titt på en knepig muskelsjukdom
Myoton dystrofi typ 1 (DM1) orsakas av en överväxt av en trippel bokstavssekvens i en gen som är viktig för muskler och andra vävnader. Personer med fler repetitioner tenderar att få svårare sjukdom, så att känna till den exakta repetitionslängden är avgörande för diagnos och prognos. Standardverktyg i kliniska laboratorier—såsom specifika PCR-tester och Southern blot—fungerar väl när repetitionen är måttlig i storlek, men de misslyckas ofta eller blir mycket oprecisa när expansionerna överstiger några hundra kopior. Det lämnar en gråzon där familjer kan veta att en mutation finns men sakna en klar bild av hur omfattande den är eller hur den kan utvecklas över tid.
Kombination av molekylära saxar och långläsningssekvensering
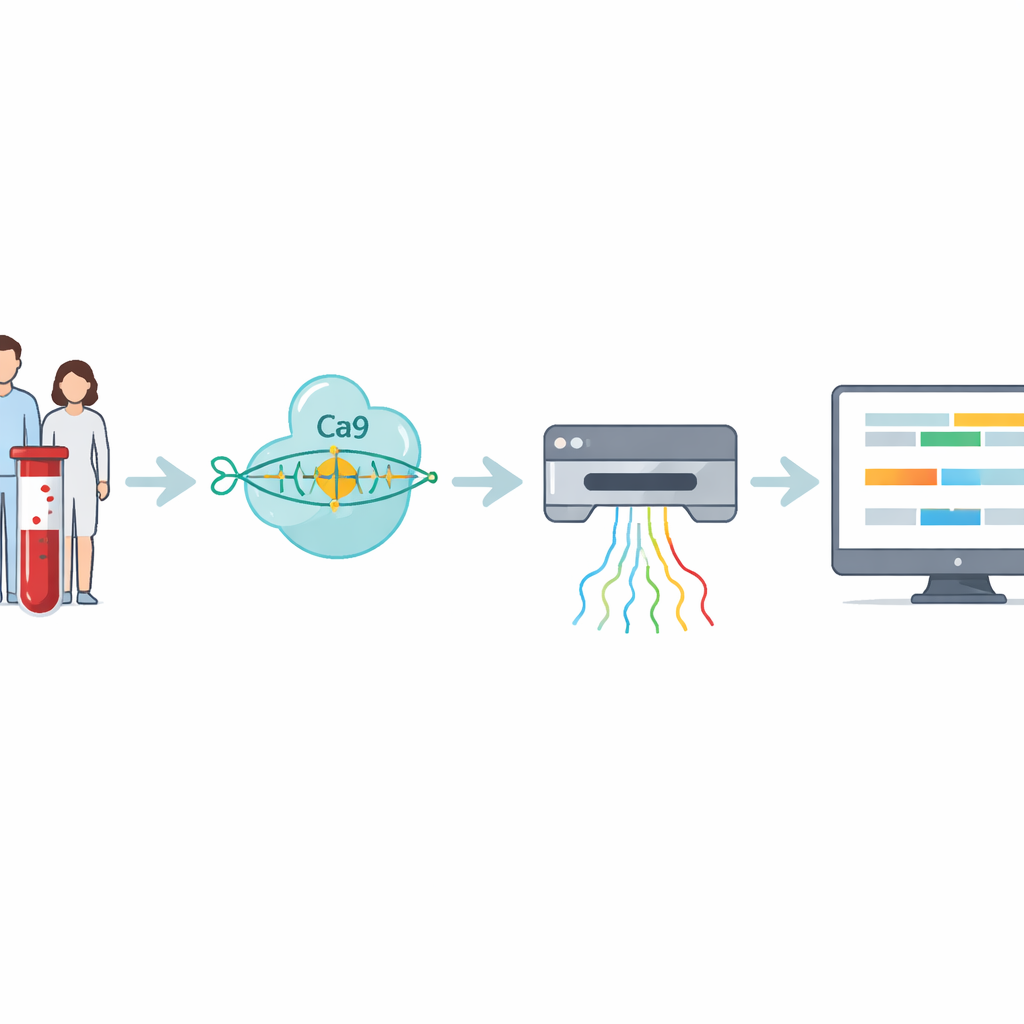
Forskarna byggde ett fyrastegs arbetsflöde som angriper dessa svåravlästa repetitioner direkt. Först extraheras DNA från blod- eller cellprov. Därefter använder teamet CRISPR–Cas9—molekylära saxar styrda till en specifik plats i genomet—för att klippa runt det DNA‑stycke som innehåller repetitionen. Eftersom endast de klippta bitarna förbereds för sekvensering, berikar metoden starkt för intresseområdet samtidigt som man undviker PCR-amplifiering, som tenderar att missa mycket stora expansioner. Det förberedda DNA:t matas sedan in i en nanoporsekvenserare, en handhållen enhet som trär DNA‑strängar genom små porer och känner av deras sammansättning i realtid som elektriska signaler.
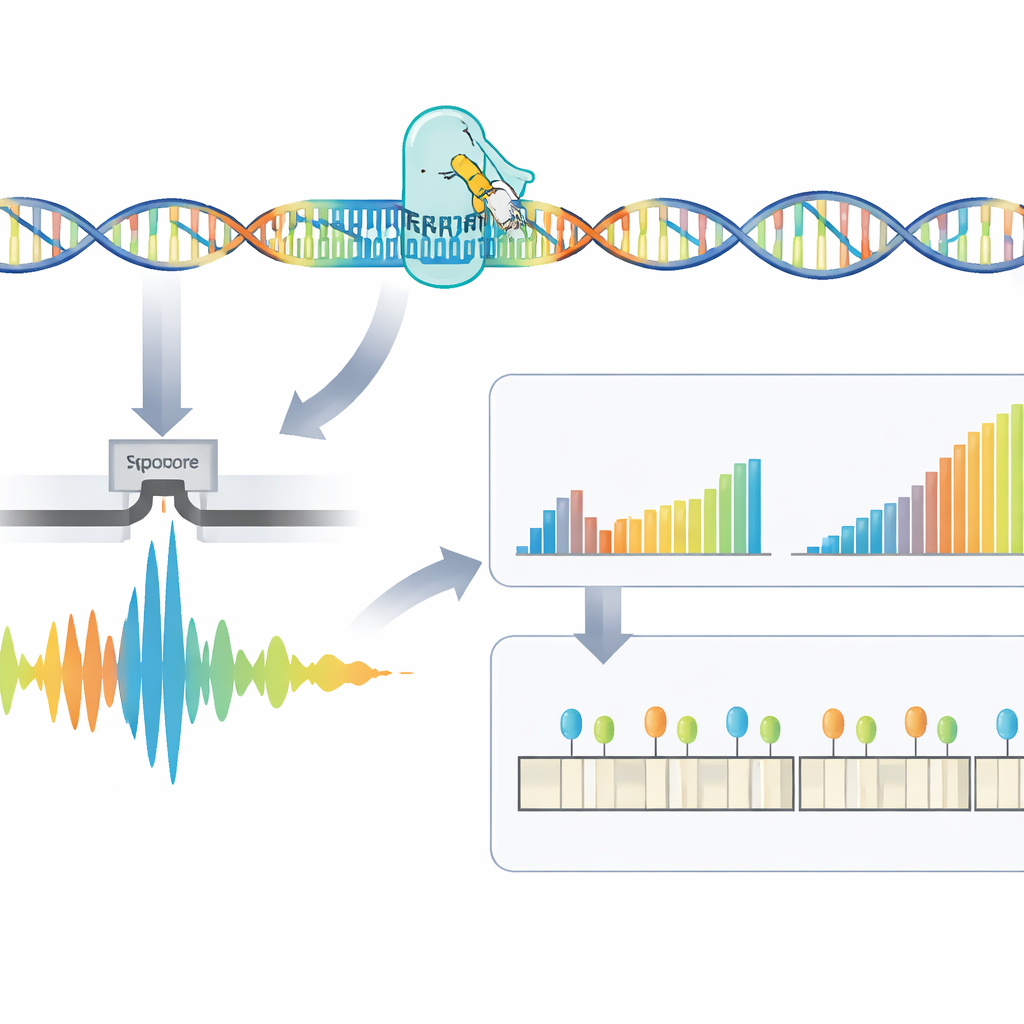
Smart mjukvara för att läsa längd och kemiska markörer
Råsignaler från sekvenseraren måste översättas till DNA‑kod och sedan till meningsfulla mått. Här introducerar författarna RepeatLab, en automatiserad analys‑pipeline utformad för att kunna användas även på en vanlig moln‑notebook. RepeatLab utför först en snabb genomgång för att hitta reads som täcker det målade genområdet, och återbearbetar sedan dessa reads med en mer krävande, högprecisionsinställning skräddarsydd för långa, repetitiva sträckor. Den använder en modifierad statistisk strategi för att klustra enskilda molekylmätningar i två grupper—vanligtvis den normala och den expanderade kopian av genen i varje person—och uppnår tillförlitliga längdskattningar med så få som ungefär ett dussin reads. Samma ramverk kan analysera många prover eller flera gener i ett kör, vilket håller kostnaderna jämförbara med befintliga kliniska tester.
Granska interruptioner och epigenetiska signaler
Utöver att bara räkna repetitioner undersöker metoden den finare strukturen i det upprepade området och hur det kemiskt är dekorerat. Vissa patienter har interruptioner—små avsnitt av annan sekvens inom repetitionen—som kan kopplas till mildare sjukdom. Teamet fann att många till synes förekommande interruptioner faktiskt var artefakter från hur råsignalen bearbetades, och de visade att användning av större analysfönster under avkodningen kraftigt minskade dessa falska positiva. RepeatLab använder också ett specialläge för att läsa DNA‑metylering, en kemisk tagg som kan slå på eller av gener. Runt DM1‑genen kartlade författarna metyleringsmönster på en‑allelnivå och identifierade flera nyckelzoner där tyngre metylering följer längre repetitions‑expansioner, vilket stöder idén att dessa kemiska markörer hjälper till att forma hur sjukdomen utvecklas.
Ett snabbare, mer innehållsrikt test för svårmätbara repetitioner
Tillsammans visar detta arbete att CRISPR‑styrd berikning, nanopore‑långläsningssekvensering och användarvänlig mjukvara kan ge en detaljerad profil av sjukdomsframkallande DNA‑repetitioner på under 24 timmar. För DM1 och närliggande tillstånd mäter tillvägagångssättet inte bara hur långa repetitionerna är utan fångar också subtila sekvensförändringar och epigenetiska mönster som dagens sjukhustester i stort sett missar. Även om vidare validering och anpassning till nyare sekvenseringskemier fortfarande krävs, pekar denna integrerade plattform mot framtida genetiska tester som är snabbare, mer informativa och lättare att införa i rutinvård.
Citering: Han, Y., Jang, JH. & Chang, H. Targeted long-read sequencing for high-resolution repeat profiling in myotonic dystrophy type 1. Exp Mol Med 58, 1203–1215 (2026). https://doi.org/10.1038/s12276-026-01683-6
Nyckelord: myoton dystrofi, tandemrepetitionsexpansion, nanoporsekvensering, CRISPR Cas9-berikning, DNA-metylering