Clear Sky Science · it
Sequenziamento mirato a lettura lunga per un profilo ad alta risoluzione delle ripetizioni nella distrofia miotonica di tipo 1
Perché questo conta per famiglie e medici
Alcune malattie ereditarie sono causate da tratti "balbettanti" nel nostro DNA—brevi sequenze ripetute centinaia o persino migliaia di volte. Quando queste ripetizioni diventano troppo lunghe, possono provocare condizioni gravi come la distrofia miotonica, una malattia che porta alla degenerazione muscolare. Tuttavia misurare con precisione la lunghezza di queste ripetizioni, e come siano chimicamente segnate, è sorprendentemente difficile con i test ospedalieri attuali. Questo articolo presenta un metodo semplificato per leggere in dettaglio queste regioni difficili del DNA in circa un giorno, potenzialmente offrendo ai medici risposte più chiare e ai pazienti orientamenti migliori.
Uno sguardo più attento a una malattia muscolare insidiosa
La distrofia miotonica di tipo 1 (DM1) è causata da un tratto eccessivamente lungo di tre nucleotidi in un gene importante per i muscoli e altri tessuti. Le persone con un numero maggiore di ripetizioni tendono ad avere una malattia più grave, quindi conoscere la lunghezza esatta della ripetizione è fondamentale per diagnosi e prognosi. Gli strumenti classici nei laboratori clinici—come particolari test PCR e Southern blot—funzionano bene quando la ripetizione è di dimensioni modeste, ma spesso falliscono o diventano molto imprecisi quando le espansioni superano alcune centinaia di copie. Questo lascia una zona grigia in cui le famiglie possono sapere che è presente una mutazione ma non avere un quadro chiaro di quanto sia estesa o di come potrebbe evolvere nel tempo.
Combinare forbici molecolari e lettura del DNA a lettura lunga
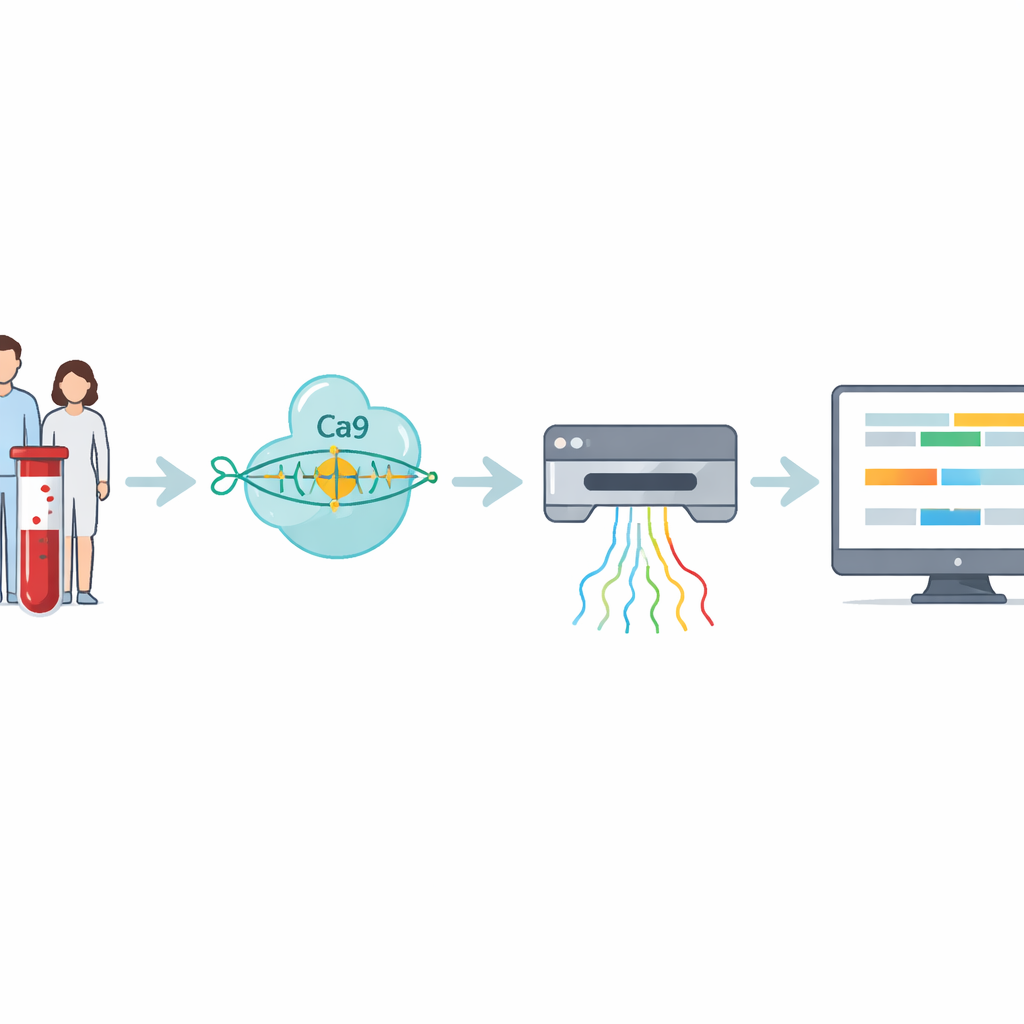
I ricercatori hanno costruito un flusso di lavoro in quattro fasi che affronta direttamente queste ripetizioni difficili da leggere. Innanzitutto si estrae il DNA da sangue o campioni cellulari. Poi il gruppo usa CRISPR–Cas9—forbici molecolari guidate a un indirizzo specifico nel genoma—per tagliare intorno al tratto di DNA che contiene la ripetizione. Poiché solo quei frammenti tagliati vengono preparati per il sequenziamento, il metodo arricchisce fortemente la regione d'interesse evitando l'amplificazione del DNA tramite PCR, che tende a perdere le espansioni molto grandi. Il DNA preparato viene quindi inserito in un sequenziatore nanopore, un dispositivo portatile che fa passare i filamenti di DNA attraverso pori minuscoli e ne rileva la composizione in tempo reale tramite segnali elettrici.
Software intelligente per leggere lunghezza e marcature chimiche
I segnali grezzi del sequenziatore devono essere tradotti in codice DNA e poi in misure significative. Gli autori presentano RepeatLab, una pipeline di analisi automatizzata progettata per essere utilizzabile anche su un comune notebook cloud. RepeatLab esegue prima una scansione rapida per trovare le letture che coprono il gene target, quindi rielabora quelle letture con un'impostazione più esigente e ad alta accuratezza tarata per tratti lunghi e ripetitivi. Utilizza una strategia statistica modificata per raggruppare le misurazioni a livello di singola molecola in due gruppi—tipicamente la copia normale e quella espansa del gene in ciascuna persona—raggiungendo stime di lunghezza affidabili con anche solo una dozzina di letture circa. Lo stesso framework può analizzare molti campioni o più geni in una sola corsa, mantenendo i costi comparabili ai saggi clinici esistenti.
Osservare interruzioni e segnali epigenetici
Oltre a contare semplicemente le ripetizioni, il metodo esamina la struttura fine della regione ripetuta e come è chimicamente decorata. Alcuni pazienti portano interruzioni—piccole porzioni di sequenza diversa all'interno della ripetizione—che possono essere associate a una malattia più lieve. Il gruppo ha riscontrato che molte presunte interruzioni erano in realtà artefatti del processo di elaborazione del segnale grezzo, e ha dimostrato che l'uso di finestre di analisi più ampie durante la decodifica riduce notevolmente questi falsi positivi. RepeatLab utilizza anche una modalità specializzata per leggere la metilazione del DNA, un'etichetta chimica che può accendere o spegnere i geni. Intorno al gene DM1, gli autori hanno mappato i pattern di metilazione a risoluzione di singola allele e identificato diverse zone chiave dove una metilazione più intensa si associa a espansioni di ripetizione più lunghe, a supporto dell'idea che questi marchi chimici contribuiscano a modellare l'evoluzione della malattia.
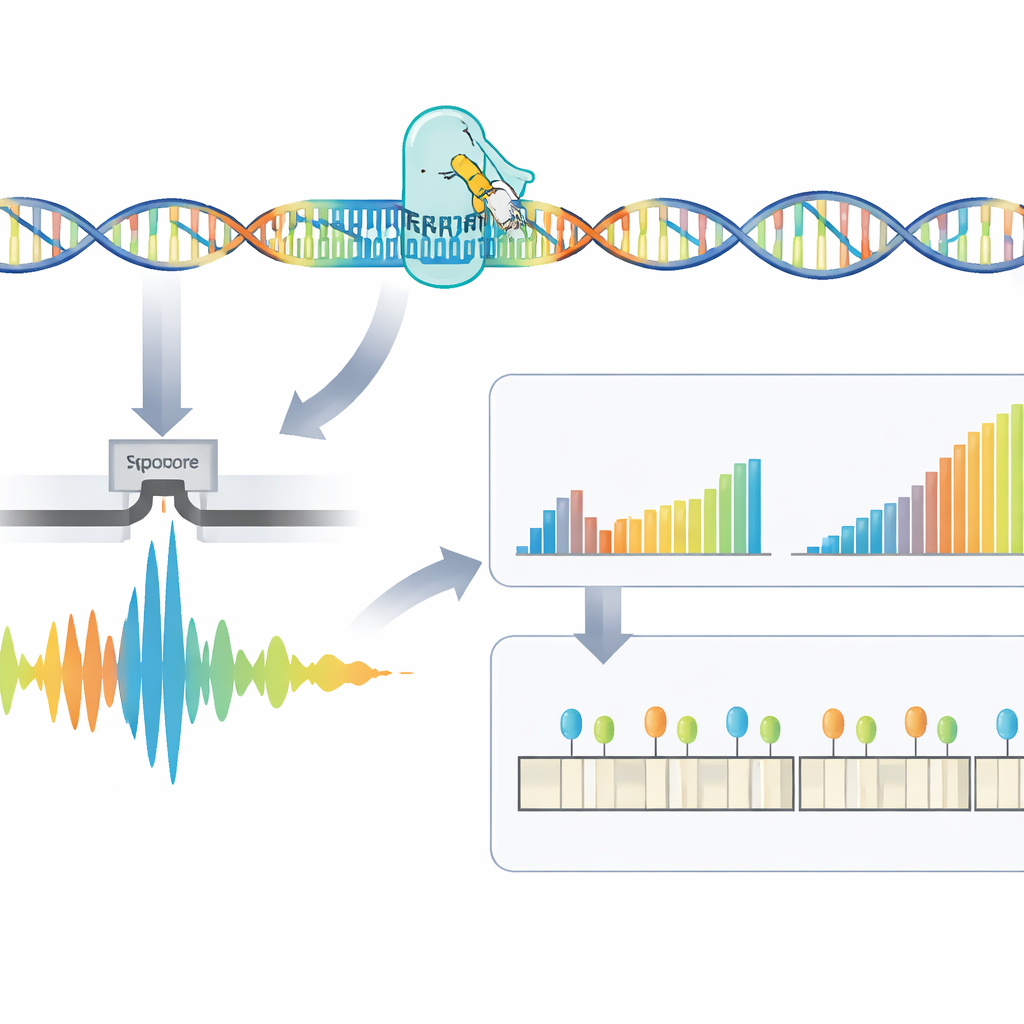
Un test più rapido e ricco per ripetizioni difficili da misurare
Nel complesso, questo lavoro mostra che l'arricchimento guidato da CRISPR, il sequenziamento a lettura lunga nanopore e un software di facile uso possono fornire un profilo dettagliato delle ripetizioni del DNA che causano malattia in meno di 24 ore. Per DM1 e condizioni correlate, l'approccio non solo misura la lunghezza delle ripetizioni ma cattura anche sottili variazioni di sequenza e pattern epigenetici che i test ospedalieri attuali in gran parte ignorano. Sebbene siano necessari ulteriori studi di validazione e adattamenti alle nuove chimiche di sequenziamento, questa piattaforma integrata indica la direzione per test genetici futuri più rapidi, più informativi e più facilmente implementabili nella pratica clinica di routine.
Citazione: Han, Y., Jang, JH. & Chang, H. Targeted long-read sequencing for high-resolution repeat profiling in myotonic dystrophy type 1. Exp Mol Med 58, 1203–1215 (2026). https://doi.org/10.1038/s12276-026-01683-6
Parole chiave: distrofia miotonica, espansione di ripetizioni tandem, sequenziamento nanopore, arricchimento CRISPR Cas9, metilazione del DNA