Clear Sky Science · nl
Gerichte lange-lezingsequencing voor hoogresolutieprofielen van herhalingen bij myotone dystrofie type 1
Waarom dit belangrijk is voor gezinnen en artsen
Sommige erfelijke ziekten worden veroorzaakt door haperende reeksen in ons DNA — korte sequenties die honderden of zelfs duizenden keren worden herhaald. Wanneer deze herhalingen te lang worden, kunnen ze ernstige aandoeningen veroorzaken, zoals myotone dystrofie, een spiervervalsaandoening. Toch is het verrassend lastig om precies te meten hoe lang deze herhalingen zijn en hoe ze chemisch gemarkeerd zijn met de huidige ziekenhuisanalyses. Dit artikel beschrijft een gestroomlijnde manier om deze moeilijk leesbare DNA-regio’s in detail uit te lezen in ongeveer een dag, wat artsen mogelijk duidelijkere antwoorden en patiënten betere begeleiding kan bieden.
Een nadere blik op een lastige spierziekte
Myotone dystrofie type 1 (DM1) wordt veroorzaakt door een overmatige opeenvolging van drie DNA-letters in een gen dat belangrijk is voor spieren en andere weefsels. Mensen met meer herhalingen hebben doorgaans ernstigere ziekteverschijnselen, dus het kennen van de exacte herhalingslengte is cruciaal voor diagnose en prognose. Standaardmethoden in klinische laboratoria — zoals specifieke PCR-tests en Southern blots — werken goed wanneer de herhaling bescheiden van omvang is, maar falen vaak of worden zeer onnauwkeurig zodra de expansies enkele honderden kopieën overschrijden. Dat laat een grijs gebied over waarin families weten dat er een mutatie aanwezig is, maar geen helder beeld hebben van hoe uitgebreid die is of hoe deze in de loop van de tijd kan veranderen.
Combinatie van moleculaire scharen en lange-lezing DNA-lezen
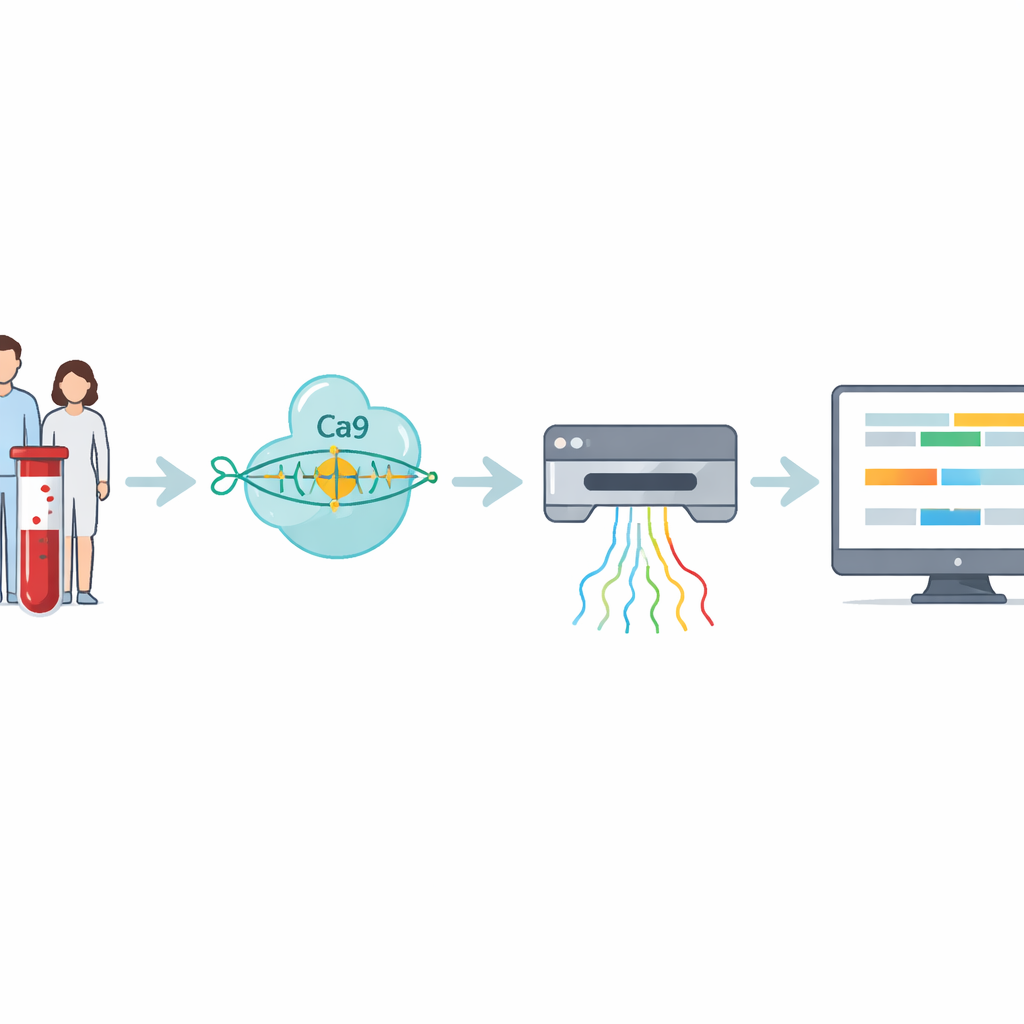
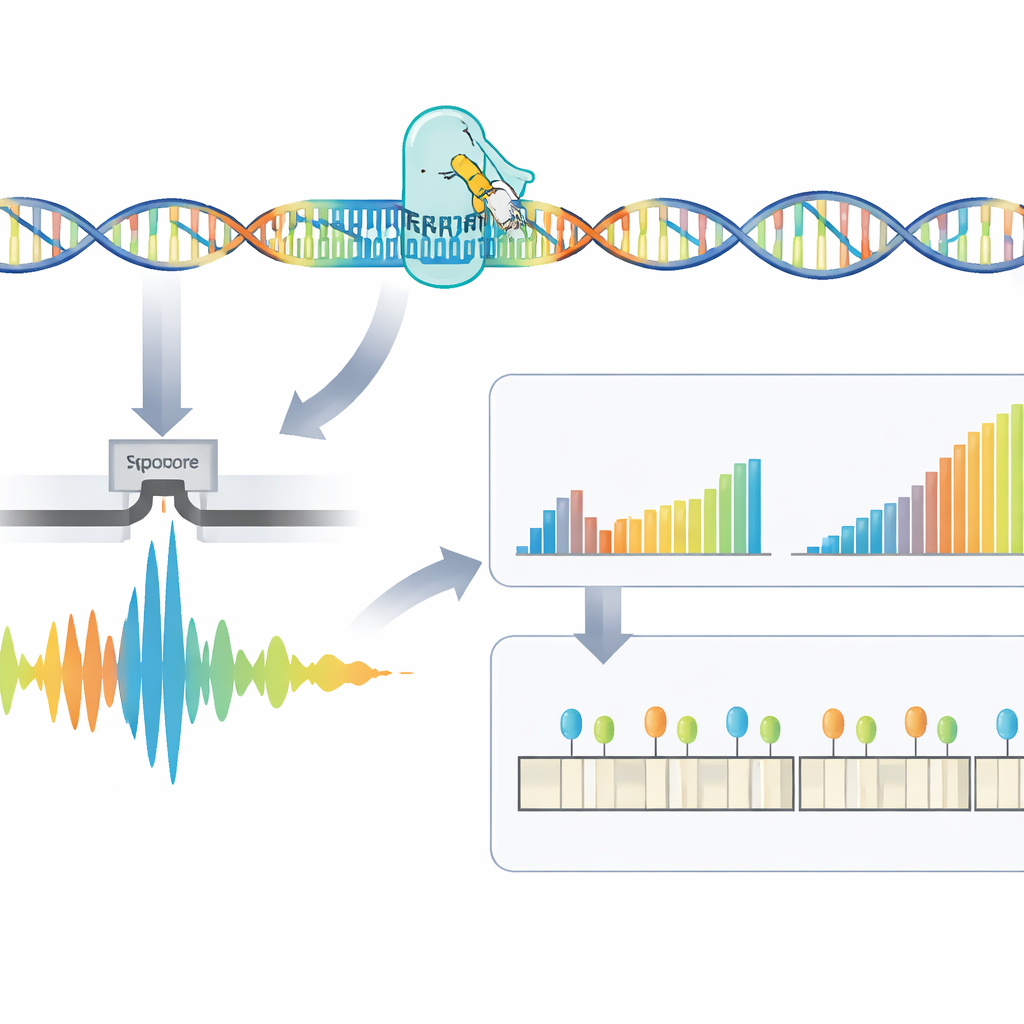
De onderzoekers ontwikkelden een workflow in vier stappen die deze moeilijk leesbare herhalingen rechtstreeks aanpakt. Eerst wordt DNA uit bloed- of celmonsters geëxtraheerd. Vervolgens gebruikt het team CRISPR–Cas9 — moleculaire scharen die naar een specifiek adres in het genoom worden geleid — om rond het DNA-stuk met de herhaling te knippen. Omdat alleen die geknipte fragmenten worden voorbereid voor sequencing, verrijkt de methode sterk voor het interessegebied en vermijdt ze PCR-amplificatie, die grote expansies doorgaans mist. Het voorbereide DNA wordt vervolgens in een nanopore-sequencer gevoerd, een draagbaar apparaat dat DNA-strengen door minuscule poriën leidt en hun samenstelling in real time als elektrische signalen waarneemt.
Slimme software om lengte en chemische markeringen te lezen
Ruwe signalen van de sequencer moeten worden vertaald naar DNA-code en vervolgens naar zinvolle metingen. Hier introduceren de auteurs RepeatLab, een geautomatiseerde analysepipline die zelfs op een gewone cloudnotebook kan worden gebruikt. RepeatLab voert eerst een snelle doorloop uit om reads te vinden die het doorgenomen gen beslaan, en verwerkt die reads daarna opnieuw met een zwaardere, hogernauwkeurige instelling die is afgestemd op lange, repetitieve reeksen. Het gebruikt een aangepaste statistische strategie om single-molecule-metingen in twee clusters te groeperen — gewoonlijk de normale en de uitgebreide kopieën van het gen bij elke persoon — en behaalt betrouwbare lengteschattingen met al zo weinig als ongeveer een dozijn reads. Hetzelfde raamwerk kan meerdere monsters of meerdere genen in één run analyseren, waarbij de kosten vergelijkbaar blijven met bestaande klinische assays.
Inzoomen op onderbrekingen en epigenetische signalen
Buiten het simpelweg tellen van herhalingen onderzoekt de methode de fijne structuur van het herhaalde gebied en hoe het chemisch is gedecoreerd. Sommige patiënten dragen onderbrekingen — kleine stukjes afwijkende sequentie binnen de herhaling — die mogelijk gekoppeld zijn aan een mildere ziekte. Het team ontdekte dat veel schijnbare onderbrekingen in feite artefacten waren van de verwerking van het ruwe signaal, en ze toonden aan dat het gebruik van grotere analysevensters tijdens decodering deze vals-positieven sterk verminderde. RepeatLab gebruikt ook een gespecialiseerde modus om DNA-methylering te lezen, een chemische markering die genen aan of uit kan schakelen. Rond het DM1-gen brachten de auteurs methyleringspatronen in kaart op enkel-allelresolutie en identificeerden ze meerdere sleutelzones waar zwaardere methylering samenvalt met langere herhalingsexpansies, wat de gedachte ondersteunt dat deze chemische markeringen mede bepalen hoe de ziekte zich ontwikkelt.
Een snellere, rijkere test voor moeilijk meetbare herhalingen
Gezamenlijk tonen deze bevindingen aan dat CRISPR-gestuurde verrijking, nanopore lange-lezingsequencing en gebruiksvriendelijke software een gedetailleerd profiel van ziekteveroorzakende DNA-herhalingen kunnen leveren in minder dan 24 uur. Voor DM1 en aanverwante aandoeningen meet de aanpak niet alleen hoe lang de herhalingen zijn, maar legt ze ook subtiele sequentieveranderingen en epigenetische patronen vast die huidige ziekenhuisanalyses grotendeels missen. Hoewel verdere validatie en aanpassing aan nieuwere sequencingschemieën nog nodig zijn, wijst dit geïntegreerde platform in de richting van toekomstige genetische tests die sneller, informatiever en eenvoudiger inzetbaar zijn in de reguliere zorg.
Bronvermelding: Han, Y., Jang, JH. & Chang, H. Targeted long-read sequencing for high-resolution repeat profiling in myotonic dystrophy type 1. Exp Mol Med 58, 1203–1215 (2026). https://doi.org/10.1038/s12276-026-01683-6
Trefwoorden: myotone dystrofie, tandemherhalingsexpansie, nanopore-sequencing, CRISPR Cas9-verrijking, DNA-methylering