Clear Sky Science · ru
Расшифровка взаимодействий жидкость — твердое при декаализации O3-слоистых оксидов
Почему это исследование батарей важно
Когда мир ищет более чистые и дешевые способы хранения возобновляемой энергии, натриевые батареи становятся перспективной альтернативой нынешним литий‑ионным элементам. Но тонкая проблема поверхностной химии делает некоторые из наиболее привлекательных натриевых материалов нестабильными при контакте с жидкостями в процессе производства. В этой работе подробно изучается скрытое взаимодействие между твердыми частицами батареи и жидкостями для их очистки и показано, как выбор правильного растворителя может решить судьбу — надежная батарея или материал, разрушающийся до того, как достигнет сети.
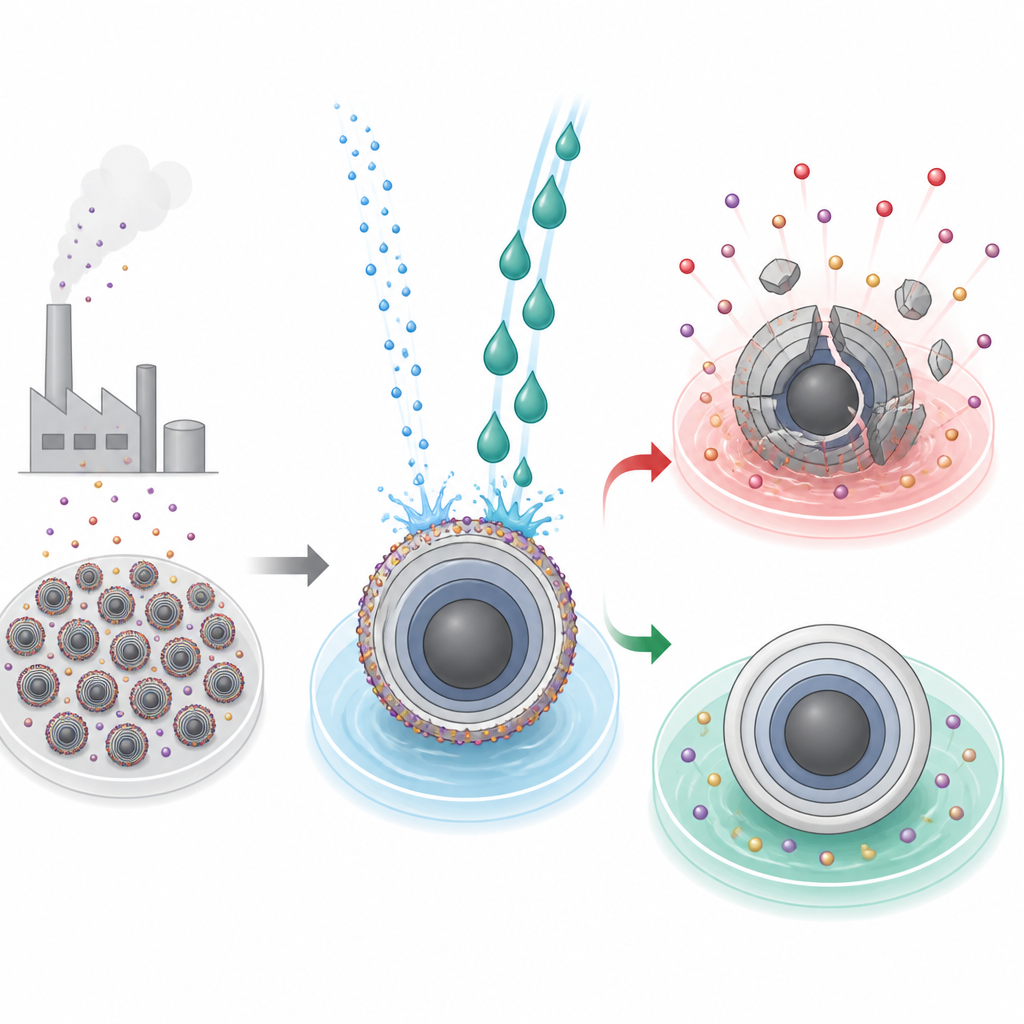
Скрытая «грязь» на частицах батареи
Современные высокоэнергетические батареи опираются на слоистые оксидные частицы в положительном электроде, где ионы входят и выходят при заряде и разряде. При изготовлении этих материалов применяют сильно щелочные условия, которые оставляют на поверхности частиц нежелательную корку остаточных щелочных соединений. Для литиевых материалов эту корку можно смыть водой по отработанным промышленным процедурам. Для натриевых аналогов та же промывка может обернуться катастрофой: вода не только удаляет остатки, но и вымывает активные ионы натрия и дестабилизирует кристаллическую сетку, что приводит к трещинам, разрушению структуры и резкой потере ёмкости батареи.
Две жидкости — два совершенно разных исхода
Исследователи сосредоточились на типичном натриевом слоистом оксиде NaNi1/3Fe1/3Mn1/3O2, уже использующемся в пилотных натриевых батареях. Они сравнили воду и этиленгликоль, распространённую автомобильную антифризную жидкость, как промывочные растворы. Оба растворителя эффективно растворяли нежелательные поверхностные щелочи, но их влияние на внутренние частицы разошлось. Материал, обработанный этиленгликолем, показал более гладкую поверхность частиц, улучшенное течение пасты при изготовлении электродов, лучшее сцепление с токоприёмниками, более высокую восстановленную ёмкость и повышенную циклическую стабильность. В отличие от этого, образцы после промывки водой подверглись глубоким трещинам, потере натрия по всему объёму частицы, замедлению переноса ионов и значительно меньшей ёмкости, а также большему выделению газов, связанному с разложением оставшихся карбонатов при высоком напряжении.
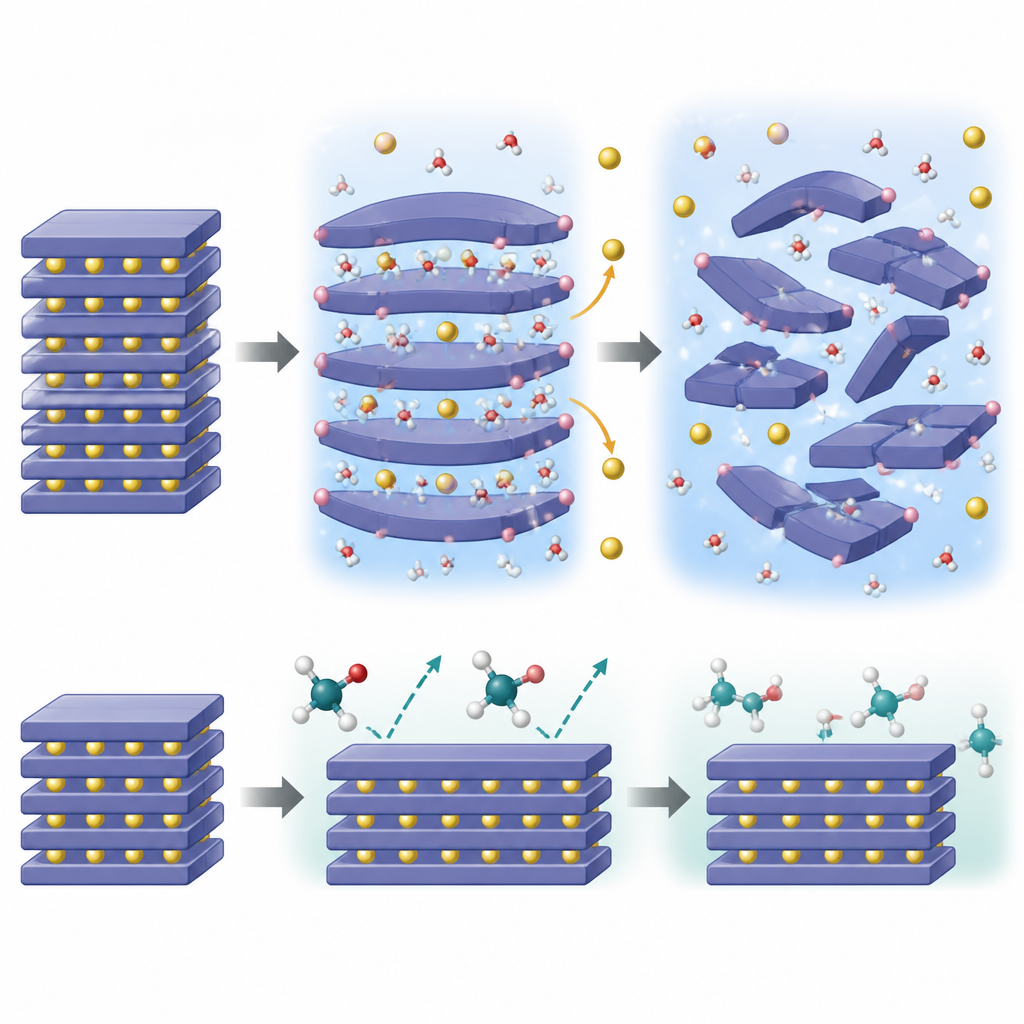
Что происходит внутри частиц
Чтобы понять, почему вода так разрушительна, команда комбинировала передовую микроскопию, зондирование поверхностной химии, нейтронную дифракцию и температурно‑зависимые рентгеновские измерения с квантово‑механическими моделями. Они выяснили, что маленькие молекулы воды могут проскальзывать между натриевыми слоями внутри кристалла, расширять межслойные расстояния и затем отдавать протоны, которые связываются с кислородной сетью. Эта «самораспространяющаяся» инвазия приводит к вытеканию ионов натрия, чтобы сохранить электронейтральность, сжимая натриевые слои и провоцируя каскад фазовых превращений и деформаций решетки. Со временем упорядоченная слоистая структура трансформируется в более неупорядоченные формы со сдвинутыми или призматическими слоями, в конечном счёте теряя способность обратимо хранить и высвобождать натрий.
Почему этиленгликоль действует мягче
Расчёты показывают, что молекулы этиленгликоля просто слишком громоздки, чтобы легко втиснуться между натриевыми слоями. Их внедрение в структуру энергетически невыгодно, поэтому их действие остаётся ограниченным поверхностью. Хотя этиленгликоль всё ещё помогает корректировать поверхностную щёлочность и удалять остаточные натриевые соединения, он не запускает ту же внутреннюю цепную реакцию с проникновением протонов и потерей натрия. Измерения подтверждают, что массоперенос между твёрдым телом и гликолем ограничен, и слоистая структура в основном остаётся нетронутой даже после обработки. Этот «эффект размера» означает, что этиленгликоль может очищать поверхность, не раскрывая структуру изнутри.
От одного материала к общему правилу проектирования
Помимо конкретного натриевого оксида, авторы распространили анализ на другие слоистые катоды на основе лития и натрия. Они показали, что способность молекул воды самопроизвольно интеркалироваться зависит от расстояния между слоями щелочных ионов и силы связи между этими ионами и кислородом. Литиевые оксиды, с более мелкими ионами и более плотными слоями, сопротивляются глубокой пенетрации воды, поэтому повреждение остаётся в основном поверхностным. Натриевые оксиды, с более широкими слоями и более слабыми связями, гораздо более уязвимы, если только не заменить некоторые переходные металлы для укрепления связи. Команда предлагает простой критерий стабильности, основанный на потере активных щелочных ионов, который можно использовать для сравнения того, как разные материалы и растворители выдерживают жидкостную обработку.
Что это значит для будущих батарей
Проще говоря, эта работа показывает, что не все промывочные жидкости равнозначны при подготовке чувствительных батарейных материалов. Вода, хоть и дешевая и удобная, способна тихо выедать натриевые слоистые оксиды изнутри, лишая их ионов, необходимых для хранения энергии. Этиленгликоль, напротив, может удалить вредные поверхностные остатки, оставляя внутреннюю структуру в основном нетронутой. Связав эти результаты с размерами молекул, силой связей и межслойными расстояниями, исследование даёт практические рекомендации по выбору и разработке жидких обработок, которые защищают производительность, а не подрывают её, помогая натриевым батареям приблизиться к надёжному широкомасштабному применению.
Цитирование: Zhang, W., Zhu, J., Song, A. et al. Deciphering the liquid-solid interactions in dealkalization of O3 layered oxides. Nat Commun 17, 4166 (2026). https://doi.org/10.1038/s41467-026-70581-2
Ключевые слова: натриевые батареи, катодные материалы, поверхностная химия, эффекты растворителя, накопление энергии