Clear Sky Science · fr
Déchiffrer les interactions liquide‑solide lors de la désalkalisation des oxydes en couches O3
Pourquoi cette étude sur les batteries est importante
Alors que le monde recherche des moyens de stocker l’énergie renouvelable plus propres et moins coûteux, les batteries à base de sodium apparaissent comme un partenaire prometteur aux cellules lithium‑ion actuelles. Mais une chimie de surface subtile rend certains des matériaux sodiques les plus attractifs instables lorsqu’ils rencontrent des liquides lors de la fabrication. Cette étude explore cette interaction cachée entre particules solides de batterie et les liquides de nettoyage, et montre comment le choix du solvant peut faire la différence entre une batterie robuste et une batterie qui se désagrège avant d’atteindre le réseau.
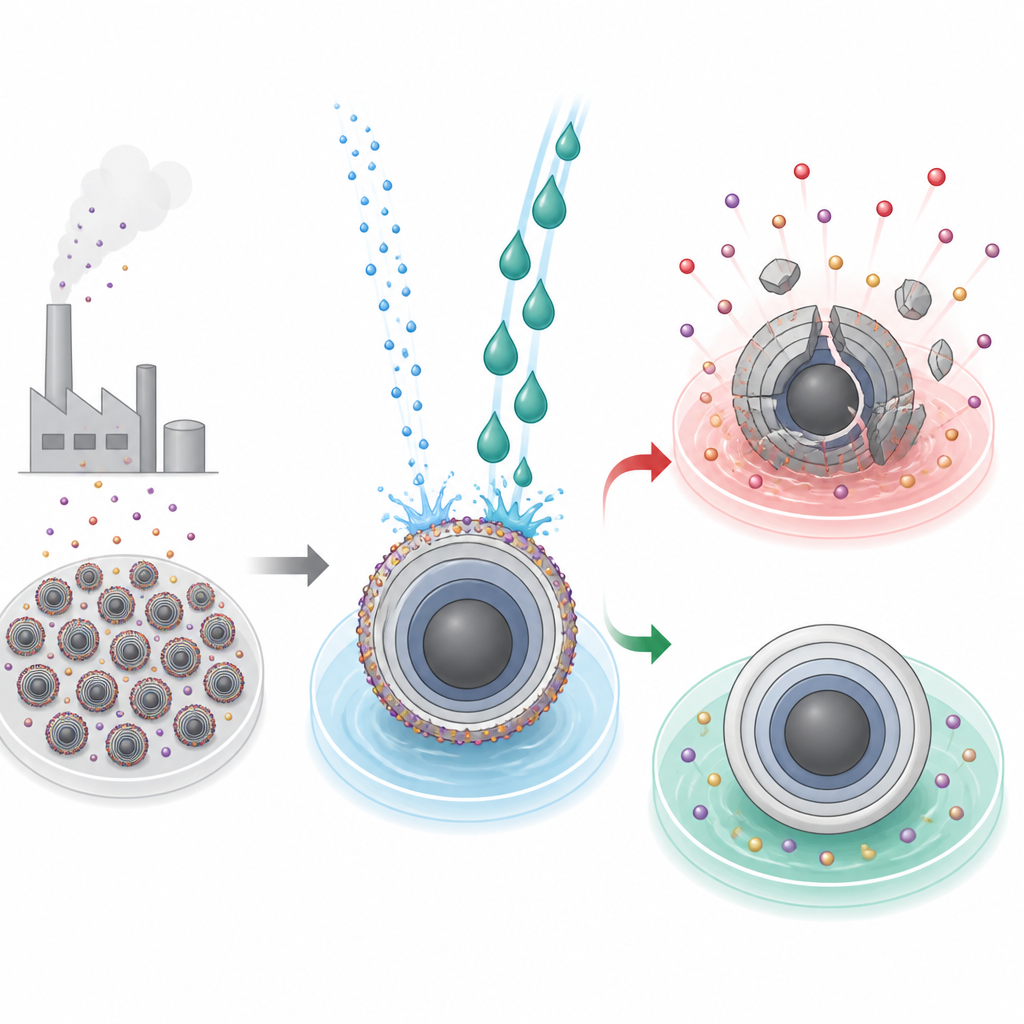
La saleté cachée sur les particules de batterie
Les batteries modernes à haute énergie s’appuient sur des particules d’oxyde en couches dans l’électrode positive, où les ions s’insèrent et se retirent pendant la charge et la décharge. Pour fabriquer ces matériaux, les industriels utilisent des conditions fortement alcalines qui laissent un croûte indésirable de composés alcalins résiduels à la surface des particules. Dans les matériaux à base de lithium, cette croûte peut être éliminée par lavage à l’eau grâce à des procédés industriels établis. Pour les équivalents sodiques, cependant, le même lavage peut être catastrophique : l’eau n’enlève pas seulement le résidu, elle extrait aussi des ions sodium actifs et déstabilise le réseau cristallin, entraînant fissures, effondrement structurel et perte brutale de capacité.
Deux liquides, deux issues très différentes
Les chercheurs se sont concentrés sur un oxyde en couches sodique typique, NaNi1/3Fe1/3Mn1/3O2, déjà utilisé dans des prototypes de batteries sodium. Ils ont comparé l’eau et l’éthylène glycol, un antigel courant, comme liquides de nettoyage. Les deux solvants dissolvaient efficacement l’alcalinité de surface indésirable, mais leur impact sur les particules sous‑jacentes divergeait. Le matériau traité à l’éthylène glycol présentait des surfaces de particules plus lisses, un meilleur écoulement de la pâte d’électrode pendant la fabrication, une adhérence renforcée au collecteur de courant, une capacité récupérée plus élevée et une meilleure stabilité en cyclage. À l’inverse, les échantillons lavés à l’eau présentaient des fissures profondes, une perte de sodium à l’intérieur des particules, un transport d’ions ralenti et une capacité beaucoup plus faible, ainsi qu’une génération de gaz accrue liée à la dégradation de carbonates résiduels à haute tension.
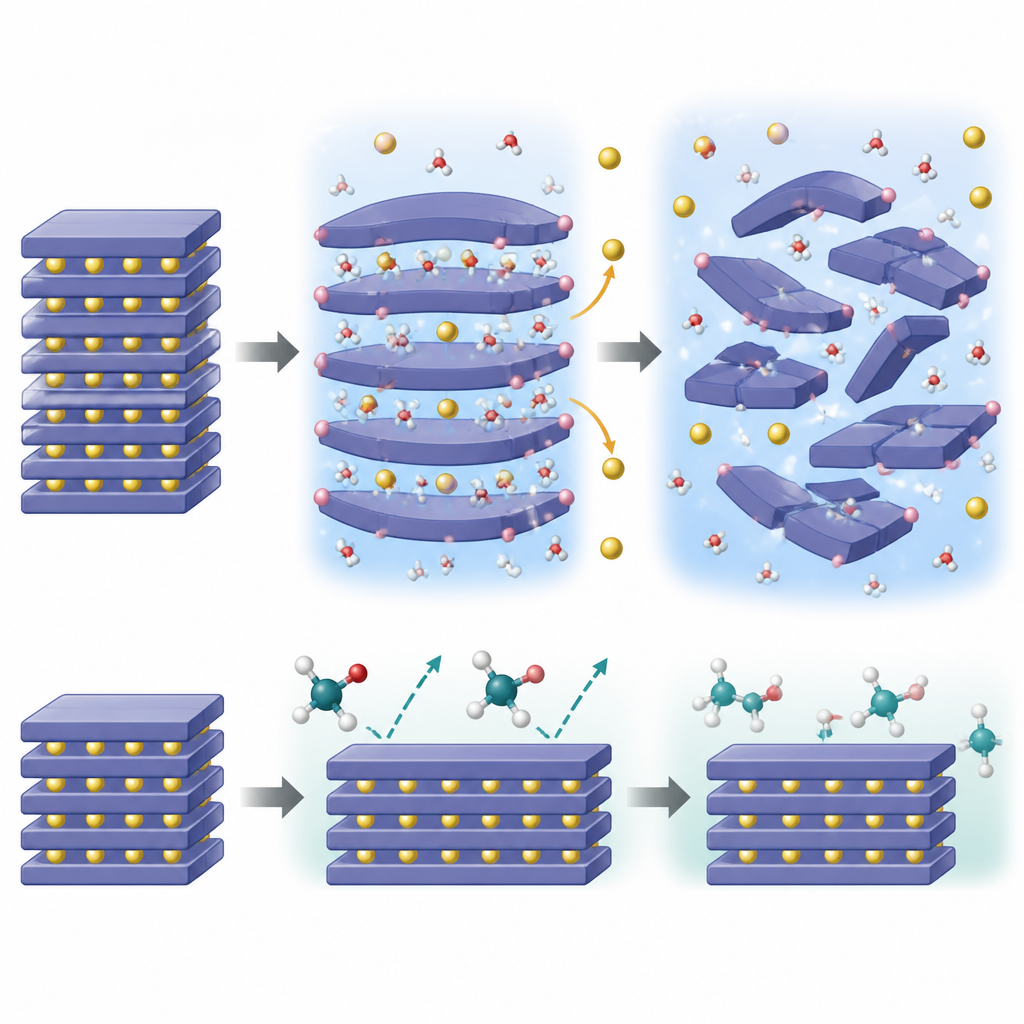
Ce qui se passe à l’intérieur des particules
Pour comprendre pourquoi l’eau est si destructive, l’équipe a combiné imagerie avancée, sondes de chimie de surface, diffraction aux neutrons et mesures X‑ray dépendantes de la température avec des simulations quantum‑mécaniques. Ils ont constaté que les petites molécules d’eau peuvent se glisser entre les couches de sodium à l’intérieur du cristal, élargir l’espacement, puis libérer des protons qui se lient au réseau oxygéné. Cette invasion « auto‑propagatrice » provoque la fuite d’ions sodium pour maintenir l’équilibre de charge, réduisant les couches sodiques et déclenchant une cascade de changements de phase et de distorsions du réseau. Avec le temps, la structure initialement ordonnée se transforme en formes plus désordonnées avec des couches glissées ou prismatiques, perdant finalement sa capacité à stocker et libérer le sodium de façon réversible.
Pourquoi l’éthylène glycol agit plus en douceur
Les calculs montrent que les molécules d’éthylène glycol sont simplement trop volumineuses pour se glisser aisément entre les couches de sodium. Leur insertion dans la structure est énergétiquement défavorable, de sorte que leur action reste confinée près de la surface. Bien que l’éthylène glycol puisse toujours ajuster l’alcalinité de surface et éliminer les composés sodiques résiduels, il ne déclenche pas la même réaction en chaîne interne d’invasion de protons et de perte de sodium. Les mesures confirment que le transfert de masse entre le solide et le liquide glycol est limité, et que le réseau en couches reste largement intact même après traitement. Cet « effet de taille » signifie que l’éthylène glycol peut nettoyer la surface sans entrouvrir la structure de l’intérieur.
D’un matériau à une règle de conception générale
Au‑delà de cet oxyde sodique spécifique, les auteurs ont étendu leur analyse à d’autres cathodes en couches à base de lithium et de sodium. Ils montrent que la capacité des molécules d’eau à s’intercaler spontanément dépend de l’espacement entre les couches d’ions alcalins et de la force de liaison entre ces ions et l’oxygène. Les oxydes de lithium, avec des ions plus petits et des couches plus serrées, résistent à une pénétration profonde d’eau, de sorte que les dommages restent principalement superficiels. Les oxydes de sodium, avec des couches plus larges et des liaisons plus faibles, sont beaucoup plus vulnérables à moins que des métaux de transition spécifiques ne soient substitués pour renforcer la liaison. L’équipe propose un indicateur simple de stabilité basé sur la perte d’ions alcalins actifs, qui peut servir à comparer comment différents matériaux et solvants réagissent lors du traitement liquide.
Ce que cela signifie pour les batteries de demain
En termes simples, ce travail montre que tous les liquides de nettoyage ne se valent pas pour la préparation de matériaux de batteries sensibles. L’eau, bon marché et pratique, peut creuser silencieusement les oxydes en couches sodiques depuis l’intérieur, leur volant les ions nécessaires au stockage d’énergie. L’éthylène glycol, en revanche, peut éliminer les résidus de surface nuisibles tout en laissant la structure interne largement intacte. En reliant ces effets à la taille moléculaire, la force de liaison et l’espacement des couches, l’étude fournit des lignes directrices pratiques pour choisir et concevoir des traitements liquides qui protègent la performance plutôt que de la compromettre, aidant ainsi les batteries sodium à se rapprocher d’une utilisation fiable à grande échelle.
Citation: Zhang, W., Zhu, J., Song, A. et al. Deciphering the liquid-solid interactions in dealkalization of O3 layered oxides. Nat Commun 17, 4166 (2026). https://doi.org/10.1038/s41467-026-70581-2
Mots-clés: batteries sodium, matériaux de cathode, chimie de surface, effets des solvants, stockage d’énergie