Clear Sky Science · it
Decifrare le interazioni liquido-solido nella de-alkalizzazione degli ossidi stratificati O3
Perché questo studio sulle batterie è importante
Mentre il mondo cerca modi più puliti ed economici per immagazzinare l'energia rinnovabile, le batterie a base di sodio emergono come un partner promettente alle celle agli ioni di litio odierne. Tuttavia, un sottile problema di chimica superficiale rende alcuni dei materiali per batterie al sodio più attraenti instabili quando incontrano liquidi durante la produzione. Questo studio approfondisce quell'interazione nascosta tra particelle solide della batteria e i liquidi usati per pulirle, e mostra come scegliere il solvente giusto possa fare la differenza tra una batteria robusta e una che si disfa prima ancora di arrivare alla rete.
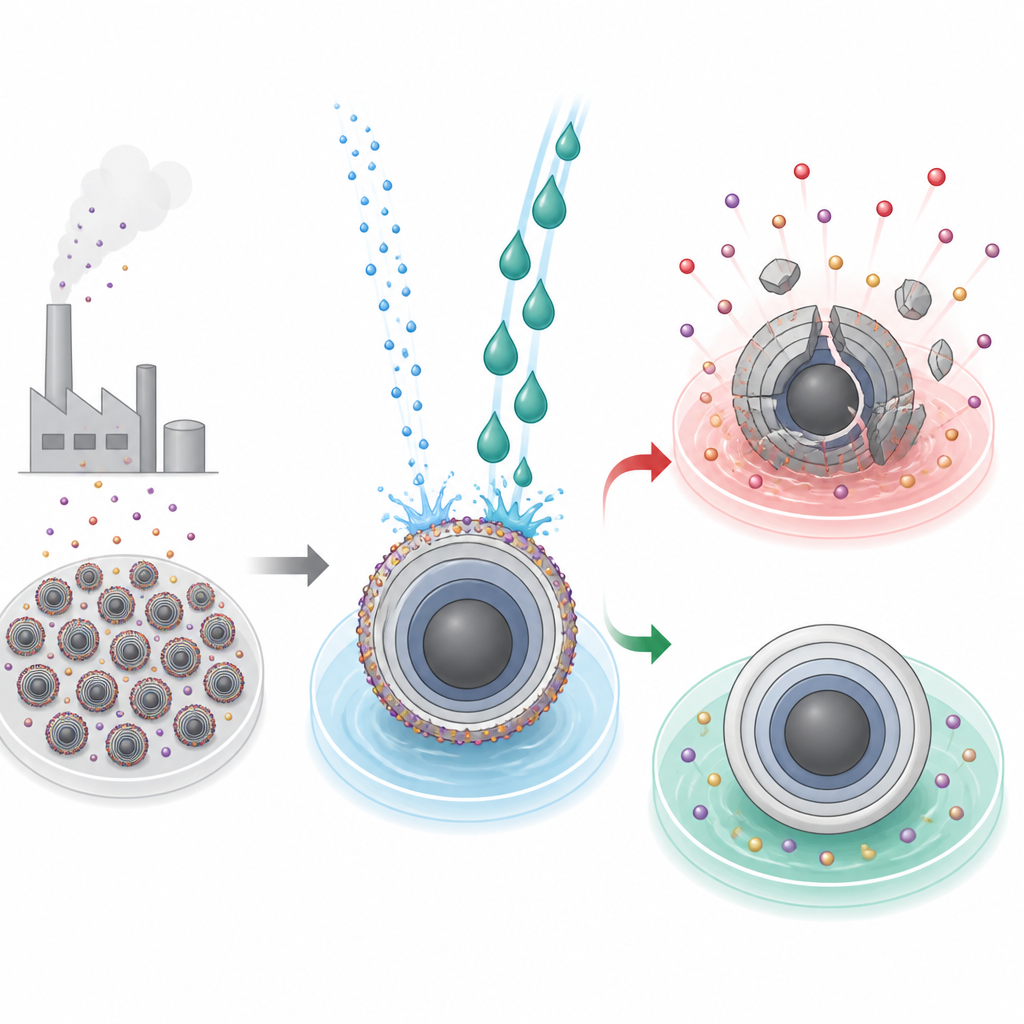
La sporcizia nascosta sulle particelle della batteria
Le batterie moderne ad alta energia si basano su particelle di ossidi stratificati nell’elettrodo positivo, dove gli ioni si muovono dentro e fuori durante la carica e la scarica. Per produrre questi materiali, i produttori impiegano condizioni fortemente alcaline che lasciano uno strato indesiderato di composti alcalini residui sulla superficie delle particelle. Nei materiali a base di litio questo strato può essere lavato via con acqua tramite processi industriali consolidati. Per i corrispettivi a base di sodio, però, lo stesso lavaggio può essere disastroso: l’acqua non solo rimuove il residuo ma estrae anche ioni sodio attivi e destabilizza il reticolo cristallino, provocando crepe, collasso strutturale e una forte perdita di capacità della batteria.
Due liquidi, due esiti molto diversi
I ricercatori si sono concentrati su un tipico ossido stratificato di sodio, NaNi1/3Fe1/3Mn1/3O2, già impiegato in batterie pilota su scala industriale. Hanno confrontato l’acqua con l’etilenglicole, un comune liquido refrigerante automobilistico, come liquidi di pulizia. Entrambi i solventi dissolvono efficientemente l’alcalinità superficiale indesiderata, ma il loro impatto sulle particelle sottostanti diverge. Il materiale trattato con etilenglicole mostrava superfici delle particelle più lisce, migliore scorrevolezza della pasta elettrodica durante la lavorazione, adesione più forte ai collettori di corrente, capacità recuperata superiore e stabilità di ciclo migliorata. Al contrario, i campioni lavati con acqua presentavano crepe profonde, perdita di sodio in tutto il volume della particella, trasporto ionico rallentato e una capacità molto inferiore, insieme a una maggiore generazione di gas collegata alla decomposizione di carbonati residui ad alto voltaggio.
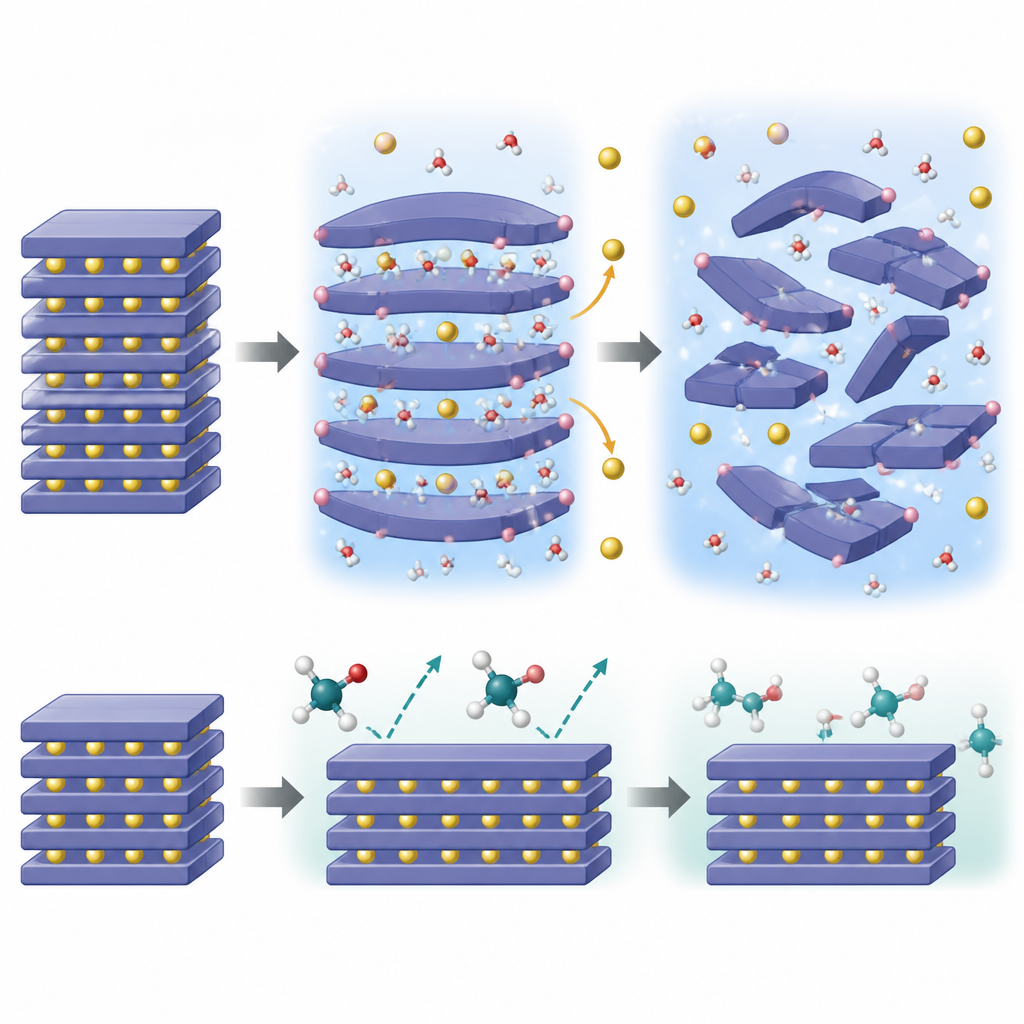
Cosa succede all'interno delle particelle
Per capire perché l’acqua sia così distruttiva, il team ha combinato imaging avanzato, sonde per la chimica superficiale, diffrazione di neutroni e misure di raggi X dipendenti dalla temperatura con simulazioni quantomeccaniche. Hanno scoperto che le piccole molecole d’acqua possono infilarsi tra gli strati di sodio all’interno del cristallo, aumentare la distanza tra gli strati e quindi rilasciare protoni che si legano al framework ossigeno. Questa invasione “auto-propagante” porta gli ioni sodio a fuoriuscire per mantenere l’equilibrio di carica, riducendo gli strati di sodio e innescando una cascata di cambiamenti di fase e distorsioni del reticolo. Col tempo, la struttura una volta ordinata si trasforma in forme più disordinate con strati scivolati o prismatici, perdendo infine la capacità di immagazzinare e rilasciare sodio in modo reversibile.
Perché l’etilenglicole si comporta più delicatamente
I calcoli mostrano che le molecole di etilenglicole sono semplicemente troppo ingombranti per insinuarsi facilmente tra gli strati di sodio. La loro inserzione nella struttura è energeticamente sfavorevole, quindi la loro azione rimane confinata vicino alla superficie. Sebbene l’etilenglicole possa comunque aiutare a regolare l’alcalinità superficiale e rimuovere i composti di sodio residui, non scatena la stessa reazione a catena interna di invasione protonica e perdita di sodio. Le misure confermano che il trasferimento di massa tra il solido e il liquido glicolico è limitato e che il framework stratificato rimane in gran parte intatto anche dopo il trattamento. Questo “effetto dimensione” significa che l’etilenglicole può detergere la superficie senza forzare l’apertura della struttura dall’interno.
Da un materiale a una regola di progetto generale
Oltre a questo specifico ossido di sodio, gli autori hanno esteso la loro analisi ad altri catodi stratificati a base di litio e sodio. Hanno mostrato che la capacità delle molecole d’acqua di intercalarsi spontaneamente dipende dalla distanza tra gli strati degli ioni alcalini e dalla forza del legame tra quegli ioni e l’ossigeno. Gli ossidi di litio, con ioni più piccoli e strati più compatti, resistono a una penetrazione profonda dell’acqua, per cui i danni rimangono per lo più limitati alla superficie. Gli ossidi di sodio, con strati più ampi e legami più deboli, sono molto più vulnerabili a meno che non vengano sostituiti metalli di transizione specifici per rafforzare il legame. Il team propone un semplice metro di stabilità basato sulla perdita di ioni alcalini attivi, che può essere usato per confrontare come diversi materiali e solventi si comportano durante la lavorazione liquida.
Cosa significa questo per le batterie del futuro
In termini concreti, questo lavoro mostra che non tutti i liquidi di pulizia sono uguali quando si tratta di preparare materiali di batterie sensibili. L’acqua, sebbene economica e comoda, può svuotare silenziosamente gli ossidi stratificati di sodio dall’interno, privandoli proprio degli ioni di cui hanno bisogno per immagazzinare energia. L’etilenglicole, al contrario, può rimuovere residui superficiali dannosi mantenendo in gran parte intatta la struttura interna. Collegando questi esiti alla dimensione molecolare, alla forza del legame e alla spaziatura degli strati, lo studio offre linee guida pratiche per scegliere e progettare trattamenti liquidi che proteggano le prestazioni anziché comprometterle, aiutando le batterie al sodio ad avvicinarsi a un uso affidabile su larga scala.
Citazione: Zhang, W., Zhu, J., Song, A. et al. Deciphering the liquid-solid interactions in dealkalization of O3 layered oxides. Nat Commun 17, 4166 (2026). https://doi.org/10.1038/s41467-026-70581-2
Parole chiave: batterie al sodio, materiali del catodo, chimica della superficie, effetti del solvente, stoccaggio di energia