Clear Sky Science · es
Descifrando las interacciones líquido-sólido en la desalcalinización de óxidos en capas O3
Por qué importa este estudio sobre baterías
Mientras el mundo busca formas más limpias y económicas de almacenar energía renovable, las baterías a base de sodio emergen como una alternativa prometedora a las celdas de ion-litio actuales. Pero un problema sutil de química de superficie vuelve inestables algunos de los materiales de sodio más atractivos cuando entran en contacto con líquidos durante la fabricación. Este estudio explora esa interacción oculta entre las partículas sólidas de la batería y los líquidos usados para limpiarlas, y muestra cómo elegir el disolvente adecuado puede marcar la diferencia entre una batería robusta y otra que se desintegra antes de llegar a la red.
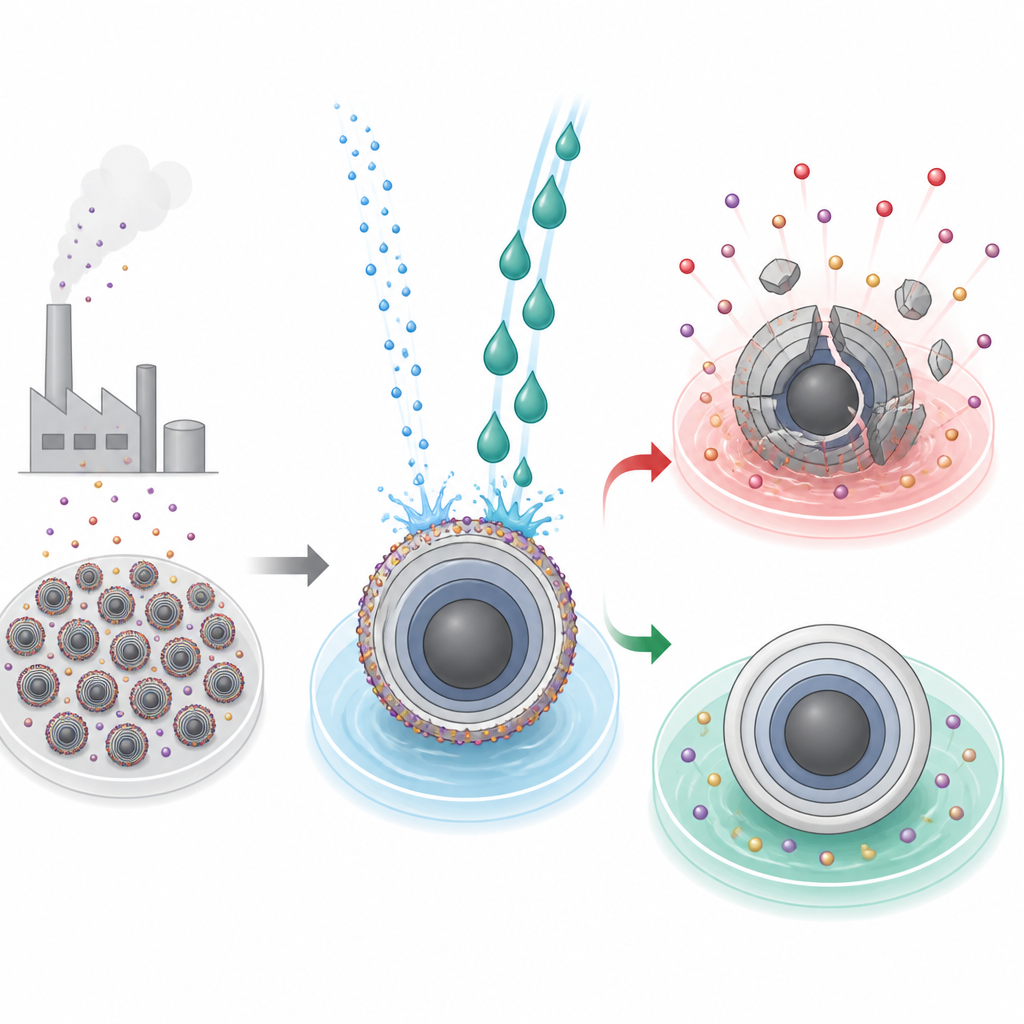
La suciedad oculta en las partículas de la batería
Las baterías modernas de alta energía dependen de partículas de óxido en capas en el electrodo positivo, donde los iones entran y salen durante la carga y descarga. Para fabricar estos materiales, los productores usan condiciones fuertemente alcalinas que dejan una corteza indeseada de compuestos alcalinos residuales en las superficies de las partículas. En materiales basados en litio, esa corteza puede lavarse con agua mediante procesos industriales establecidos. Sin embargo, para las contrapartes a base de sodio, el mismo lavado puede ser desastroso: el agua no solo elimina el residuo, sino que también arranca iones de sodio activos y desestabiliza la red cristalina, provocando grietas, colapso estructural y una caída brusca de la capacidad de la batería.
Dos líquidos, dos resultados muy diferentes
Los investigadores se centraron en un óxido en capas típico de sodio, NaNi1/3Fe1/3Mn1/3O2, ya usado en baterías de escala piloto. Compararon el agua con el etilenglicol, un anticongelante automotriz común, como líquidos de limpieza. Ambos disolventes disolvieron eficazmente el alcali superficial no deseado, pero su impacto sobre las partículas subyacentes divergió. El material tratado con etilenglicol mostró superficies de partícula más lisas, mejor fluidez de la pasta de electrodo durante la fabricación, mayor adherencia a los colectores de corriente, mayor capacidad recuperada y mejor estabilidad en ciclos. En contraste, las muestras lavadas con agua presentaron grietas profundas, pérdida de sodio a lo largo de la partícula, transporte iónico más lento y una capacidad mucho menor, junto con una mayor generación de gas vinculada a la descomposición de carbonatos residuales a alto voltaje.
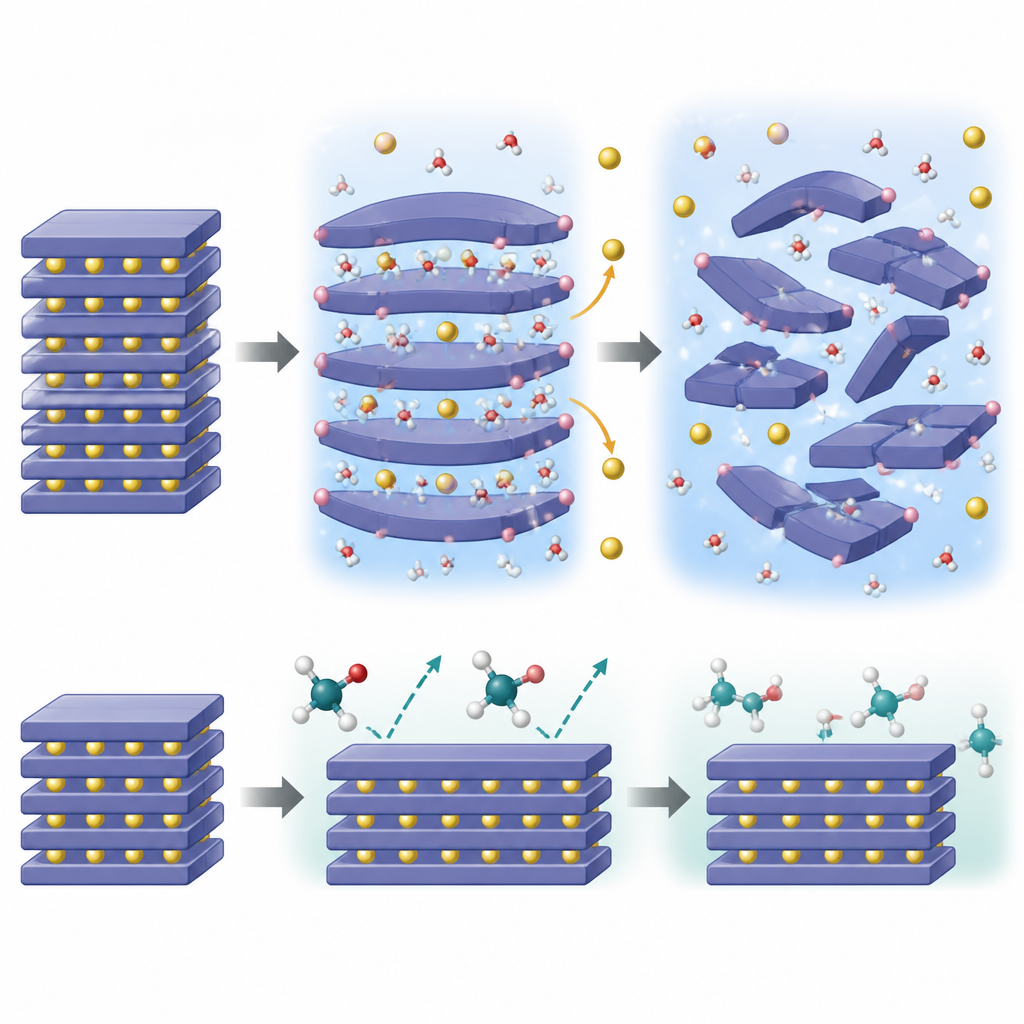
Qué ocurre dentro de las partículas
Para entender por qué el agua es tan destructiva, el equipo combinó imágenes avanzadas, sondas de química de superficie, difracción de neutrones y medidas de rayos X dependientes de la temperatura con simulaciones cuántico-mecánicas. Encontraron que las pequeñas moléculas de agua pueden colarse entre las capas de sodio dentro del cristal, expandir el espaciado y luego liberar protones que se unen al entramado de oxígeno. Esta invasión “autopropagadora” provoca que iones de sodio salgan para mantener el balance de carga, encogiendo las capas de sodio y desencadenando una cascada de cambios de fase y distorsiones de la red. Con el tiempo, la estructura ordenada en capas se transforma en formas más desordenadas con capas desplazadas o prismáticas, perdiendo finalmente su capacidad para almacenar y liberar sodio de forma reversible.
Por qué el etilenglicol actúa con más suavidad
Los cálculos muestran que las moléculas de etilenglicol son simplemente demasiado voluminosas para intercalarse fácilmente entre las capas de sodio. Su inserción en la estructura es energéticamente desfavorable, por lo que su acción queda confinada cerca de la superficie. Aunque el etilenglicol puede aún ayudar a ajustar la alcalinidad superficial y eliminar compuestos residuales de sodio, no desencadena la misma reacción en cadena interna de invasión protónica y pérdida de sodio. Las medidas confirman que el intercambio de masa entre el sólido y el líquido de glicol es limitado, y que la estructura en capas permanece en gran medida intacta incluso después del tratamiento. Este “efecto tamaño” significa que el etilenglicol puede limpiar la superficie sin forzar la apertura de la estructura desde el interior.
De un material a una regla de diseño general
Más allá de este óxido de sodio específico, los autores extendieron su análisis a otros cátodos en capas basados en litio y sodio. Mostraron que la capacidad de las moléculas de agua para intercalar espontáneamente depende del espaciado entre las capas de iones alcalinos y de la fuerza del enlace entre esos iones y el oxígeno. Los óxidos de litio, con iones más pequeños y capas más compactas, resisten la penetración profunda de agua, por lo que el daño permanece mayormente en la superficie. Los óxidos de sodio, con capas más anchas y enlaces más débiles, son mucho más vulnerables a menos que se sustituyan metales de transición específicos para fortalecer el enlace. El equipo propone un sencillo índice de estabilidad basado en la pérdida de iones alcalinos activos, que puede usarse para comparar cómo distintos materiales y disolventes se comportan durante el procesado líquido.
Qué significa esto para las baterías del futuro
En términos sencillos, este trabajo muestra que no todos los líquidos de limpieza son iguales al preparar materiales sensibles para baterías. El agua, aunque barata y conveniente, puede vaciar silenciosamente los óxidos en capas a base de sodio desde el interior, robándoles los mismos iones que necesitan para almacenar energía. El etilenglicol, en cambio, puede eliminar los residuos superficiales dañinos mientras deja la estructura interna mayormente intacta. Al vincular estos resultados con el tamaño molecular, la fuerza de enlace y el espaciado de capas, el estudio ofrece pautas prácticas para elegir y diseñar tratamientos líquidos que protejan el rendimiento en lugar de socavarlo, acercando las baterías de sodio a un uso fiable a gran escala.
Cita: Zhang, W., Zhu, J., Song, A. et al. Deciphering the liquid-solid interactions in dealkalization of O3 layered oxides. Nat Commun 17, 4166 (2026). https://doi.org/10.1038/s41467-026-70581-2
Palabras clave: baterías de sodio, materiales de cátodo, química de superficie, efectos de disolvente, almacenamiento de energía