Clear Sky Science · pl
Rozszyfrowanie oddziaływań ciecz-stan stały podczas odalkalizowania tlenków warstwowych O3
Dlaczego to badanie baterii ma znaczenie
W miarę jak świat poszukuje czystszych i tańszych sposobów magazynowania energii odnawialnej, baterie oparte na sodzie jawią się jako obiecujące uzupełnienie dla obecnych ogniw litowo-jonowych. Jednak subtelny problem chemii powierzchniowej sprawia, że niektóre z najatrakcyjniejszych materiałów sodowych stają się niestabilne w kontakcie z cieczami stosowanymi podczas produkcji. To badanie zagłębia się w tę ukrytą interakcję między stałymi cząstkami baterii a płynami używanymi do ich oczyszczania i pokazuje, jak wybór odpowiedniego rozpuszczalnika może przesądzić o tym, czy bateria będzie trwała, czy rozpadnie się, zanim trafi do sieci.
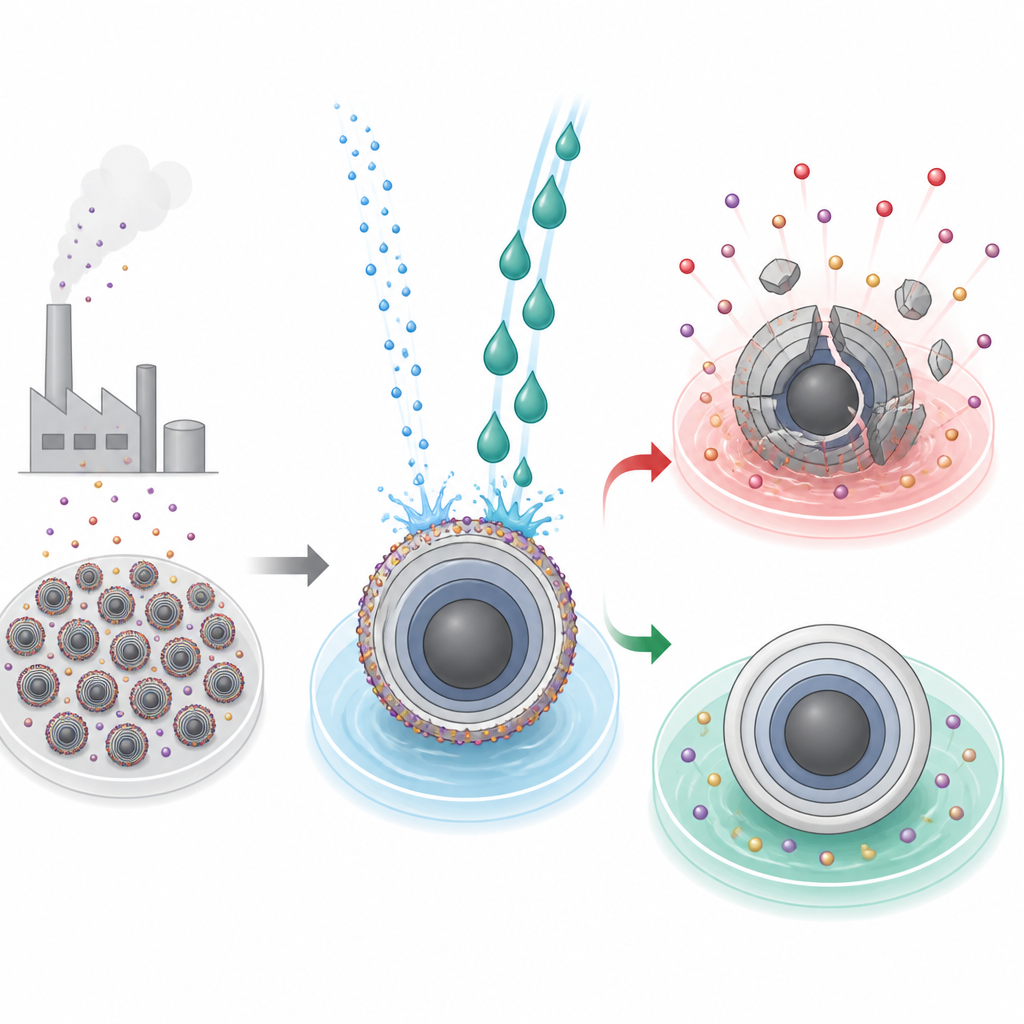
Ukryty brud na cząstkach baterii
Nowoczesne baterie o wysokiej gęstości energii wykorzystują warstwowe tlenki w elektroodzie dodatniej, gdzie jony przemieszczają się w trakcie ładowania i rozładowania. Przy wytwarzaniu tych materiałów stosuje się silnie zasadowe warunki, które pozostawiają na powierzchniach cząstek niepożądaną warstwę pozostałych związków alkalicznych. W materiałach na bazie litu tę skorupę można zmyć wodą przy użyciu sprawdzonych procesów przemysłowych. Dla odpowiedników sodowych jednak takie czyszczenie może być katastrofalne: woda nie tylko usuwa resztki, lecz także wypłukuje aktywne jony sodu i destabilizuje strukturę krystaliczną, prowadząc do pęknięć, zapadania struktury i gwałtownej utraty pojemności baterii.
Dwa płyny, dwa różne rezultaty
Naukowcy skupili się na typowym tlenku warstwowym sodu NaNi1/3Fe1/3Mn1/3O2, już wykorzystywanym w pilotażowych bateriach sodowych. Porównali wodę z glikolem etylenowym, powszechnym płynem chłodzącym w motoryzacji, jako płynami czyszczącymi. Oba rozpuszczalniki skutecznie rozpuszczały niepożądaną alkaliczną powłokę powierzchniową, ale ich wpływ na podłoże cząstek okazał się odmienny. Materiał traktowany glikolem etylenowym pokazywał gładsze powierzchnie cząstek, lepsze przepływanie masy pasty elektrody podczas produkcji, silniejsze przywieranie do kolektorów prądu, wyższą odzyskaną pojemność i poprawioną stabilność cykli. Natomiast próbki płukane wodą cierpiały na głębokie pęknięcia, utratę sodu w całej objętości cząstek, wolniejszy transport jonów i znacznie niższą pojemność, a także większe wytwarzanie gazów związane z rozkładem pozostałych węglanów przy wysokim napięciu.
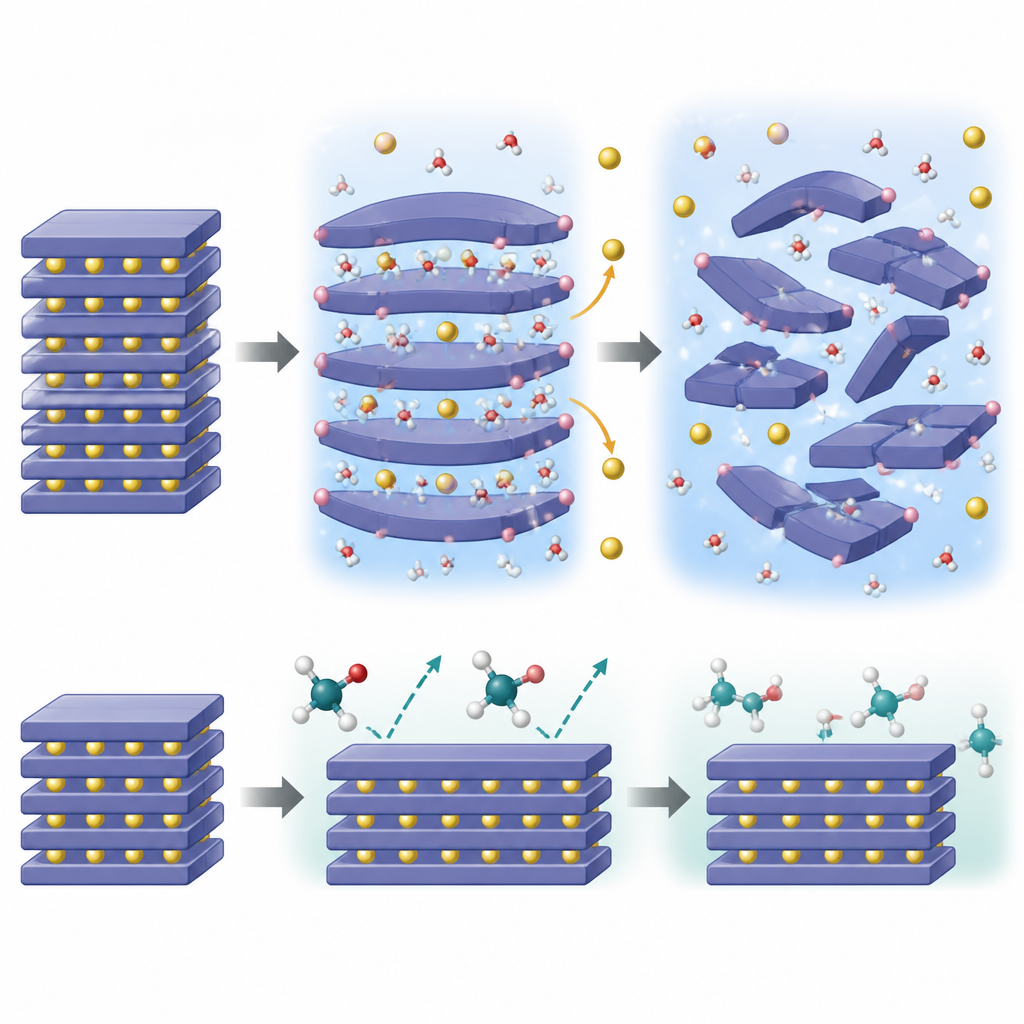
Co dzieje się wewnątrz cząstek
Aby zrozumieć, dlaczego woda jest tak destrukcyjna, zespół połączył zaawansowane obrazowanie, sondy chemii powierzchni, dyfrakcję neutronów i pomiary rentgenowskie zależne od temperatury z symulacjami kwantowo-mechanicznymi. Odkryli, że małe cząsteczki wody mogą wślizgiwać się między warstwy sodu w krysztale, rozszerzać odstępy między nimi, a następnie uwalniać protony, które wiążą się z układem tlenowym. Ta „samopodtrzymująca się” inwazja powoduje wyciek jonów sodu na zewnątrz, by zachować równowagę ładunku, kurczenie się warstw sodu i uruchomienie kaskady przemian fazowych oraz deformacji sieci. Z czasem uporządkowana struktura warstwowa przekształca się w bardziej nieuporządkowane formy ze przesuniętymi lub pryzmatycznymi warstwami, ostatecznie tracąc zdolność odwracalnego magazynowania i oddawania sodu.
Dlaczego glikol etylenowy działa łagodniej
Obliczenia pokazują, że cząsteczki glikolu etylenowego są po prostu zbyt masywne, by łatwo wcisnąć się między warstwy sodu. Ich wnikanie w strukturę jest energetycznie niekorzystne, więc ich działanie ogranicza się do powierzchni. Chociaż glikol etylenowy nadal może pomóc w regulacji zasadowości powierzchni i usuwaniu pozostałych związków sodu, nie wywołuje tej samej wewnętrznej reakcji łańcuchowej z inwazją protonów i utratą sodu. Pomiary potwierdzają, że transport masy między ciałem stałym a cieczą glikolu jest ograniczony, a warstwowy szkielet pozostaje w dużej mierze nienaruszony nawet po zabiegu. Ten „efekt rozmiaru” oznacza, że glikol etylenowy może oczyścić powierzchnię, nie rozchylając struktury od wewnątrz.
Od jednego materiału do ogólnej zasady projektowej
Poza tym konkretnym tlenkiem sodu autorzy rozszerzyli analizę na inne warstwowe katody na bazie litu i sodu. Pokazali, że to, czy cząsteczki wody mogą spontanicznie interkalować się, zależy od odstępu między warstwami jonów alkalicznych oraz siły wiązania tych jonów z tlenem. Tlenki litu, z mniejszymi jonami i ciaśniejszymi warstwami, stawiają opór głębokiej penetracji wody, więc uszkodzenia pozostają głównie na powierzchni. Tlenki sodu, o szerszych warstwach i słabszych wiązaniach, są znacznie bardziej podatne, chyba że określone metale przejściowe zostaną podstawione, by wzmocnić wiązania. Zespół proponuje prostą miarę stabilności opartą na utracie aktywnych jonów alkalicznych, którą można zastosować do porównywania, jak różne materiały i rozpuszczalniki zachowują się podczas obróbki ciekłej.
Co to oznacza dla przyszłych baterii
Mówiąc prosto, ta praca pokazuje, że nie wszystkie płyny czyszczące są równoważne przy przygotowywaniu wrażliwych materiałów baterii. Woda, choć tania i wygodna, może cicho wydrążać warstwowe tlenki sodu od środka, pozbawiając je jonów niezbędnych do magazynowania energii. Glikol etylenowy, w przeciwieństwie do tego, może usunąć szkodliwe resztki powierzchniowe, pozostawiając strukturę wewnętrzną w dużej mierze nienaruszoną. Łącząc te obserwacje z rozmiarem cząsteczek, siłą wiązań i odstępami warstwowymi, badanie dostarcza praktycznych wskazówek dotyczących wyboru i zaprojektowania zabiegów ciekłych, które chronią wydajność zamiast ją podkopywać, przybliżając baterie sodowe do niezawodnego zastosowania na dużą skalę.
Cytowanie: Zhang, W., Zhu, J., Song, A. et al. Deciphering the liquid-solid interactions in dealkalization of O3 layered oxides. Nat Commun 17, 4166 (2026). https://doi.org/10.1038/s41467-026-70581-2
Słowa kluczowe: baterie sodowe, materiały katodowe, chemia powierzchni, wpływ rozpuszczalników, magazynowanie energii