Clear Sky Science · pt
Decifrando as interações líquido-sólido na desalcificação de óxidos em camadas O3
Por que este estudo sobre baterias importa
À medida que o mundo busca formas mais limpas e econômicas de armazenar energia renovável, baterias à base de sódio surgem como parceiras promissoras das células íon-lítio atuais. Mas um problema sutil de química de superfície torna alguns dos materiais de bateria de sódio mais atrativos instáveis ao contato com líquidos durante a fabricação. Este estudo investiga essa interação oculta entre partículas sólidas da bateria e os líquidos usados para limpá-las, mostrando como a escolha do solvente pode ser a diferença entre uma bateria robusta e uma que se desfaz antes mesmo de chegar à rede elétrica.
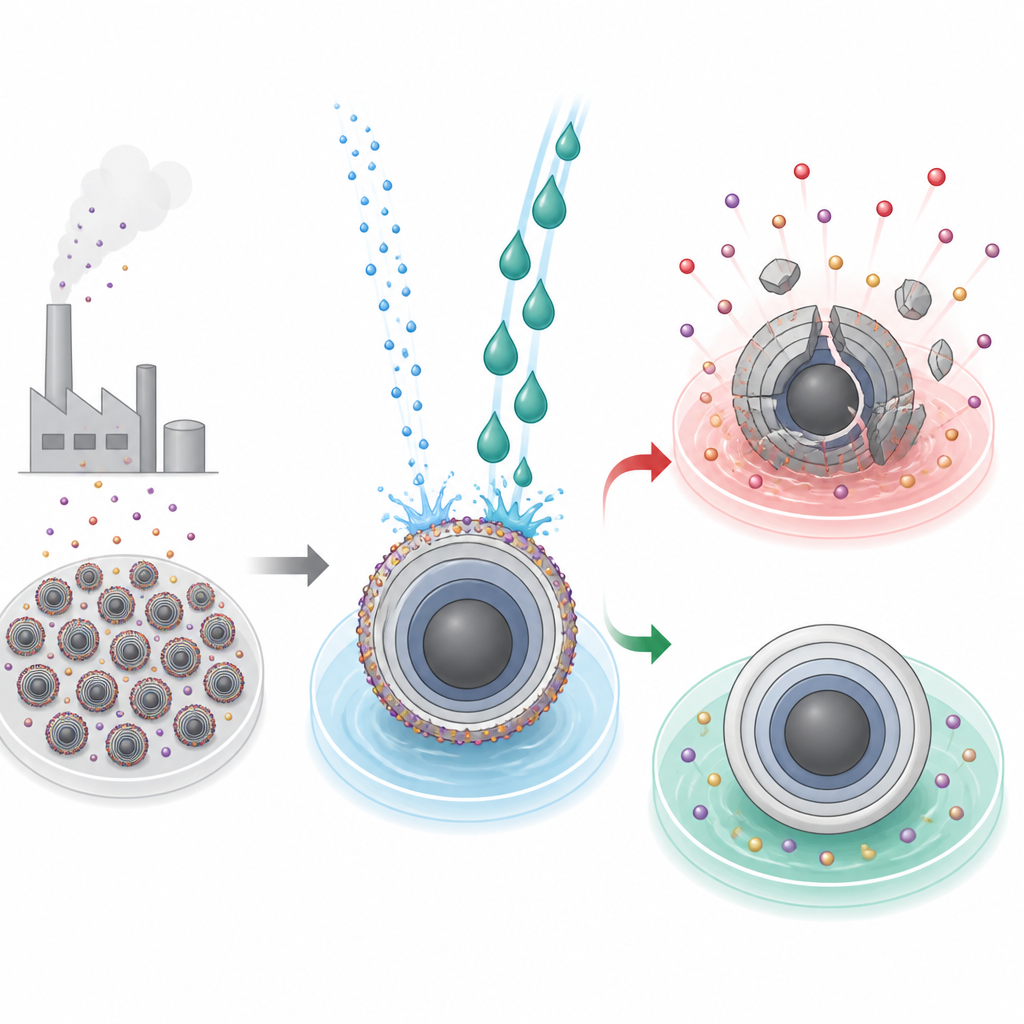
A sujeira oculta nas partículas da bateria
Baterias modernas de alta energia dependem de partículas de óxidos em camadas no eletrodo positivo, onde íons entram e saem durante carga e descarga. Para fabricar esses materiais, os produtores usam condições fortemente alcalinas que deixam uma crosta indesejada de compostos alcalinos residuais na superfície das partículas. Em materiais à base de lítio, essa crosta pode ser lavada com água usando processos industriais estabelecidos. Nos equivalentes à base de sódio, no entanto, a mesma lavagem pode significar desastre: a água não só remove o resíduo como também arranca íons de sódio ativos e desestabiliza a estrutura cristalina, levando a fissuras, colapso estrutural e perda acentuada de capacidade da bateria.
Dois líquidos, dois resultados muito diferentes
Os pesquisadores se concentraram em um óxido em camadas típico de sódio, NaNi1/3Fe1/3Mn1/3O2, já utilizado em baterias de escala piloto. Compararam água com etilenoglicol, um anticongelante automotivo comum, como líquidos de limpeza. Ambos os solventes dissolveram eficientemente o excesso alcalino superficial, mas seu impacto nas partículas subjacentes divergiu. O material tratado com etilenoglicol apresentou superfícies de partícula mais lisas, melhor fluidez da pasta eletrodica durante a fabricação, maior adesão aos coletores de corrente, maior capacidade recuperada e estabilidade de ciclo melhorada. Em contraste, amostras lavadas com água sofreram fissuras profundas, perda de sódio por toda a partícula, transporte iônico mais lento e capacidade muito menor, além de maior geração de gases associada à degradação de carbonatos remanescentes em alta tensão.
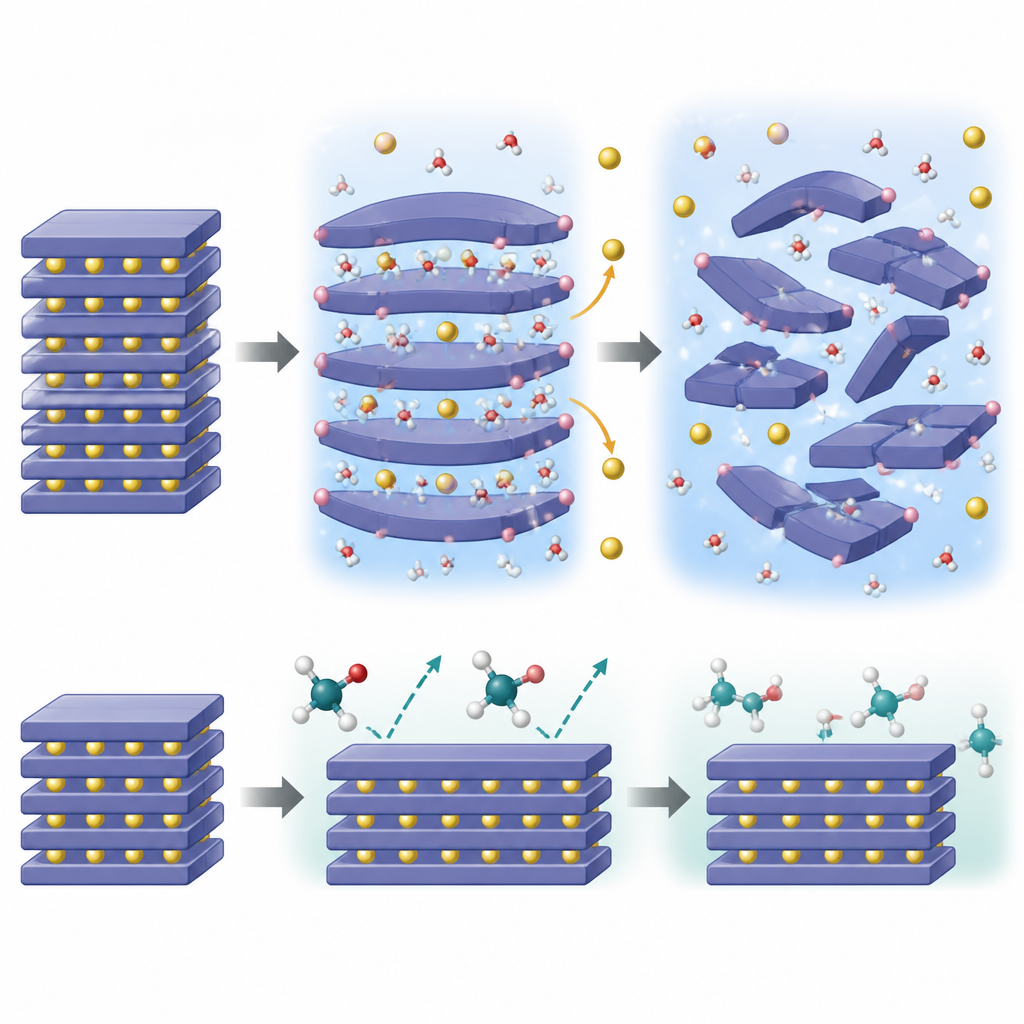
O que acontece dentro das partículas
Para entender por que a água é tão destrutiva, a equipe combinou imagens avançadas, sondas de química de superfície, difração de nêutrons e medidas de raios X dependentes de temperatura com simulações quântico-mecânicas. Descobriram que pequenas moléculas de água podem se infiltrar entre as camadas de sódio dentro do cristal, expandir o espaçamento e então liberar prótons que se ligam à rede de oxigênio. Essa invasão “auto-propagadora” leva ao vazamento de íons de sódio para manter o balanço de carga, encolhendo as camadas de sódio e desencadeando uma cascata de mudanças de fase e distorções de rede. Com o tempo, a estrutura ordenada em camadas transforma-se em formas mais desordenadas, com camadas deslocadas ou prismáticas, perdendo eventualmente a capacidade de armazenar e liberar sódio de forma reversível.
Por que o etilenoglicol age com mais brandura
Os cálculos mostram que as moléculas de etilenoglicol são simplesmente volumosas demais para se enfiar facilmente entre as camadas de sódio. Sua inserção na estrutura é energeticamente desfavorável, de modo que sua ação fica confinada à superfície. Embora o etilenoglicol ainda possa ajudar a ajustar a alcalinidade superficial e remover compostos residuais de sódio, ele não dispara a mesma reação em cadeia interna de invasão por prótons e perda de sódio. Medidas confirmam que a transferência de massa entre o sólido e o líquido de glicol é limitada, e a estrutura em camadas permanece em grande parte intacta mesmo após o tratamento. Esse “efeito de tamanho” significa que o etilenoglicol pode limpar a superfície sem abrir a estrutura por dentro.
De um material a uma regra geral de projeto
Além deste óxido específico de sódio, os autores estenderam sua análise a outros cátodos em camadas à base de lítio e de sódio. Mostraram que a possibilidade de moléculas de água se intercalarem espontaneamente depende do espaçamento entre camadas de íons alcalinos e da força da ligação entre esses íons e o oxigênio. Óxidos de lítio, com íons menores e camadas mais apertadas, resistem à penetração profunda da água, de modo que o dano permanece em grande parte na superfície. Óxidos de sódio, com camadas mais largas e ligações mais fracas, são muito mais vulneráveis, a menos que metais de transição específicos sejam substituídos para fortalecer a ligação. A equipe propõe um indicador simples de estabilidade baseado na perda de íons alcalinos ativos, que pode ser usado para comparar como diferentes materiais e solventes se comportam durante o processamento em líquido.
O que isso significa para baterias futuras
Em termos simples, este trabalho mostra que nem todos os líquidos de limpeza são iguais ao preparar materiais sensíveis de bateria. A água, embora barata e prática, pode silenciosamente corroer óxidos em camadas de sódio por dentro, roubando-os dos íons de que precisam para armazenar energia. O etilenoglicol, por contraste, pode remover resíduos superficiais nocivos deixando a estrutura interna amplamente intacta. Ao relacionar esses resultados ao tamanho molecular, força de ligação e espaçamento das camadas, o estudo oferece diretrizes práticas para escolher e projetar tratamentos líquidos que protejam o desempenho em vez de miná-lo, ajudando baterias de sódio a avançarem para uso confiável em larga escala.
Citação: Zhang, W., Zhu, J., Song, A. et al. Deciphering the liquid-solid interactions in dealkalization of O3 layered oxides. Nat Commun 17, 4166 (2026). https://doi.org/10.1038/s41467-026-70581-2
Palavras-chave: baterias de sódio, materiais de cátodo, química de superfície, efeitos de solvente, armazenamento de energia