Clear Sky Science · de
Entschlüsselung der Flüssig-Feststoff-Wechselwirkungen bei der Entalkalisierung von O3-Schichtoxiden
Warum diese Batterie-Studie wichtig ist
Während die Welt nach saubereren und günstigeren Möglichkeiten zur Speicherung erneuerbarer Energie sucht, zeichnen sich natriumbasierte Batterien als vielversprechende Ergänzung zu heutigen Lithium-Ionen-Zellen ab. Ein subtiler Oberflächenchemie-Effekt macht jedoch einige der attraktivsten Natrium-Batteriematerialien instabil, wenn sie während der Fertigung mit Flüssigkeiten in Berührung kommen. Diese Studie untersucht genau diese versteckte Wechselwirkung zwischen festen Batteriepartikeln und den Flüssigkeiten, die zu ihrer Reinigung verwendet werden, und zeigt, wie die Wahl des richtigen Lösungsmittels den Unterschied ausmachen kann zwischen einer robusten Batterie und einer, die auseinanderfällt, bevor sie jemals das Netz erreicht.
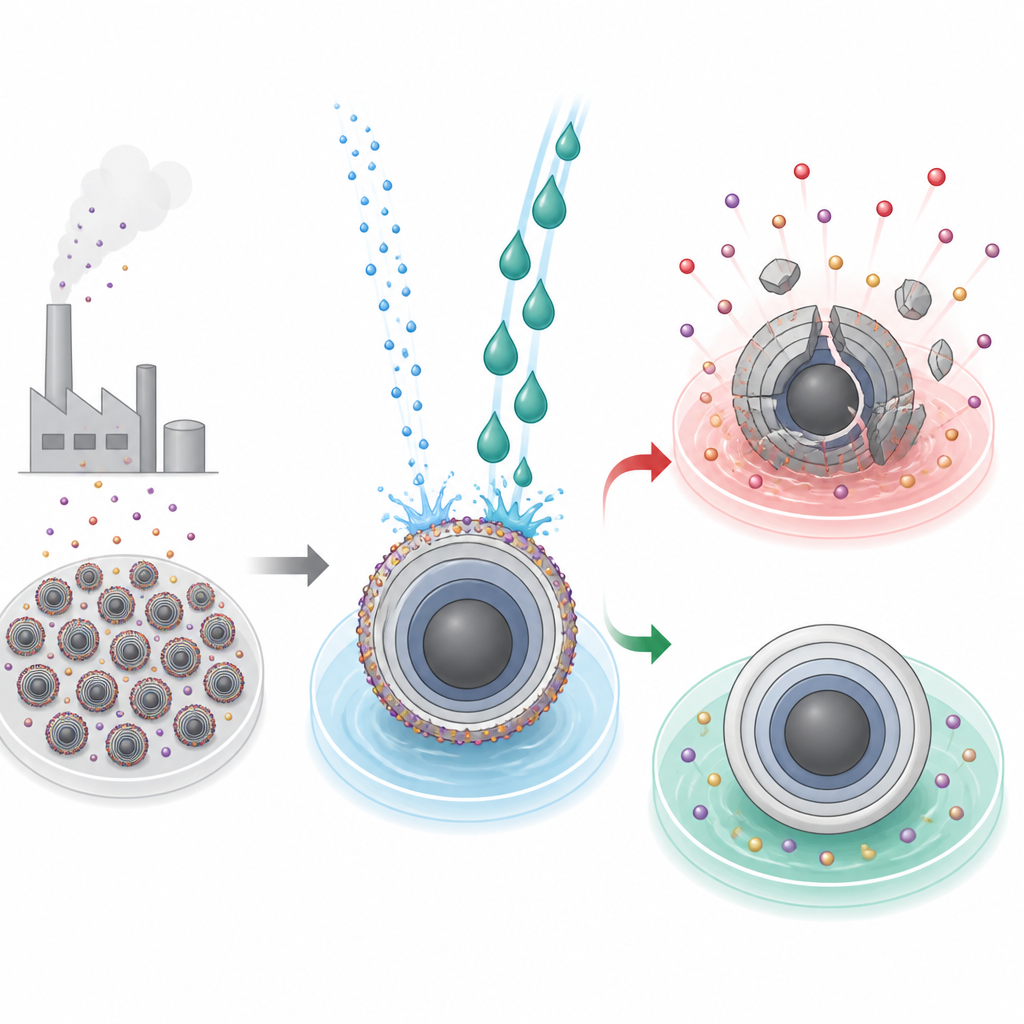
Der verborgene Belag auf Batteriepartikeln
Moderne Hochenergie-Batterien basieren auf Schichtoxid-Partikeln in der positiven Elektrode, in denen Ionen beim Laden und Entladen hinein- und herauswandern. Zur Herstellung dieser Materialien verwenden Hersteller stark alkalische Bedingungen, die eine unerwünschte Kruste aus zurückgebliebenen Alkali-Verbindungen auf den Partikeloberflächen hinterlassen. Bei lithiumbasierten Materialien kann diese Kruste mit Wasser und etablierten Industrieprozessen abgewaschen werden. Für natriumbasierte Gegenstücke kann dieselbe Wäsche jedoch katastrophal sein: Wasser entfernt nicht nur das Residuum, sondern entzieht auch aktive Natriumionen und destabilisiert das Kristallgerüst, was zu Rissen, strukturellem Kollaps und einem starken Kapazitätsverlust der Batterie führt.
Zwei Flüssigkeiten, zwei sehr unterschiedliche Ergebnisse
Die Forscher konzentrierten sich auf ein typisches natriumhaltiges Schichtoxid, NaNi1/3Fe1/3Mn1/3O2, das bereits in Pilotmaßstab in Natriumbatterien verwendet wird. Sie verglichen Wasser mit Ethylenglykol, einem gängigen Kältemittel in der Automobiltechnik, als Reinigungsflüssigkeiten. Beide Lösungsmittel lösten die unerwünschte Oberflächenalkali effizient, doch ihre Auswirkungen auf die zugrundeliegenden Partikel gingen auseinander. Das mit Ethylenglykol behandelte Material zeigte glattere Partikeloberflächen, bessere Fließeigenschaften der Elektrodenmischpaste während der Fertigung, stärkere Haftung am Stromsammler, höhere wiedergewonnene Kapazität und verbesserte Zyklusstabilität. Im Gegensatz dazu litten wassergewaschene Proben unter tiefen Rissen, Natriumverlust über das gesamte Partikel hinweg, langsamerem Ionentransport und deutlich geringerer Kapazität sowie verstärkter Gasbildung, die mit dem Abbau verbliebener Carbonate bei hohen Spannungen verbunden ist.
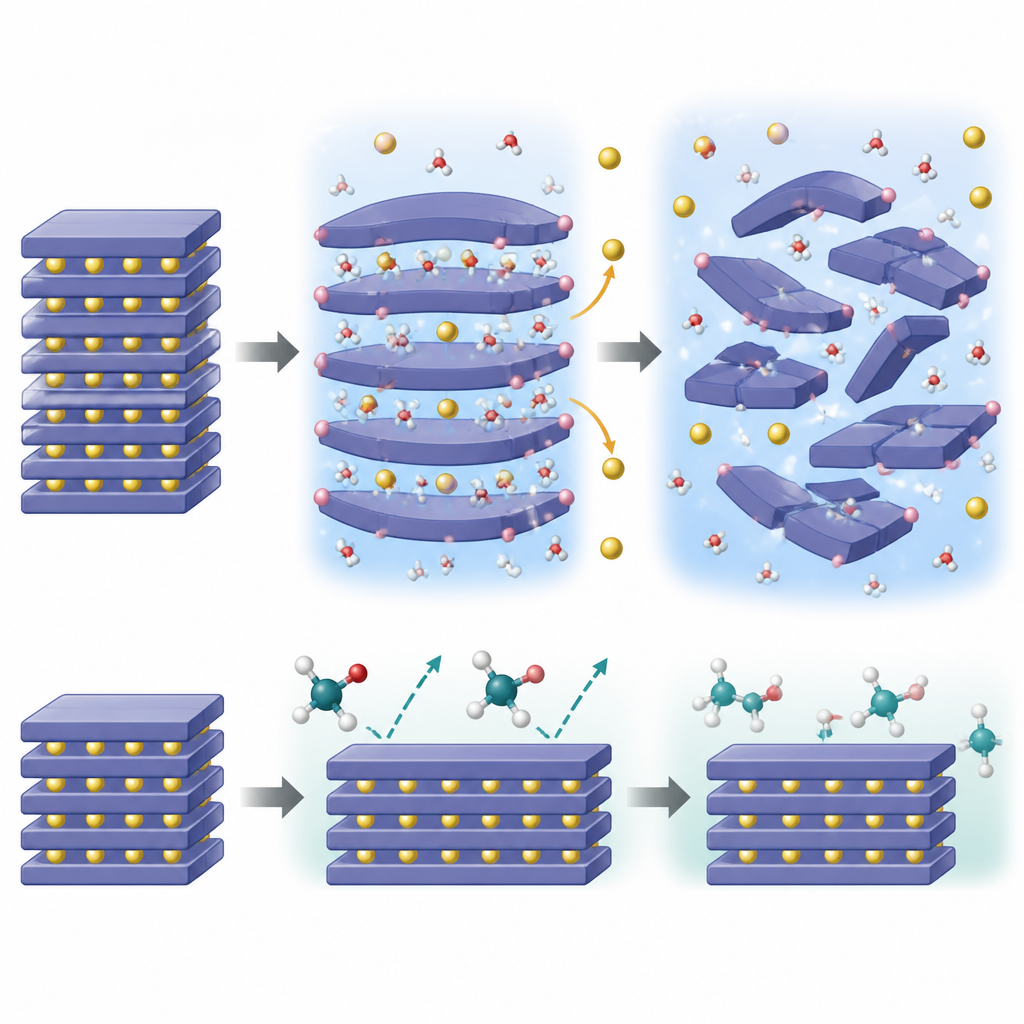
Was sich im Inneren der Partikel abspielt
Um zu verstehen, warum Wasser so zerstörerisch ist, kombinierten die Forscher fortgeschrittene Bildgebung, Oberflächenchemie-Analysen, Neutronenbeugung und temperaturabhängige Röntgenmessungen mit quantenmechanischen Simulationen. Sie fanden heraus, dass kleine Wassermoleküle zwischen die Natriumlagen im Kristall schlüpfen, den Abstand vergrößern und dann Protonen freisetzen, die sich an das Sauerstoffgerüst binden. Diese „selbstverstärkende“ Invasion führt dazu, dass Natriumionen auslaufen, um die Ladungsbilanz zu erhalten, wodurch die Natriumlagen schrumpfen und eine Kaskade von Phasenübergängen und Gitterverzerrungen ausgelöst wird. Im Laufe der Zeit verwandelt sich die einst geordnete Schichtstruktur in stärker ungeordnete Formen mit verschobenen oder prismatischen Lagen und verliert schließlich die Fähigkeit, Natrium reversibel zu speichern und freizusetzen.
Warum Ethylenglykol sanfter reagiert
Die Berechnungen zeigen, dass Ethylenglykolmoleküle schlicht zu voluminös sind, um sich leicht zwischen die Natriumlagen zu zwängen. Ihre Einlagerung in die Struktur ist energetisch ungünstig, sodass ihre Wirkung auf die Oberfläche beschränkt bleibt. Obwohl Ethylenglykol die Oberflächenalkalität anpassen und verbliebene Natriumverbindungen entfernen kann, löst es nicht die gleiche interne Kettenreaktion aus, die durch Protoneneinwanderung und Natriumverlust entsteht. Messungen bestätigen, dass der Massentransfer zwischen Feststoff und Glykolflüssigkeit begrenzt ist und das Schichtgerüst auch nach der Behandlung weitgehend intakt bleibt. Dieser „Größeneffekt“ bedeutet, dass Ethylenglykol die Oberfläche reinigen kann, ohne die Struktur von innen aufzubrechen.
Von einem Material zu einer allgemeinen Gestaltungsregel
Über dieses spezifische Natriumoxid hinaus erweiterten die Autoren ihre Analyse auf andere lithium- und natriumbasierte Schichtkathoden. Sie zeigten, dass die spontane Interkalation von Wassermolekülen davon abhängt, wie groß der Abstand zwischen den Alkali-Ionen-Lagen ist und wie stark die Bindung zwischen diesen Ionen und dem Sauerstoff ist. Lithiumoxide mit kleineren Ionen und engeren Lagen widerstehen einer tiefen Wasserpenetration, sodass der Schaden größtenteils an der Oberfläche bleibt. Natriumoxide mit größeren Lagen und schwächeren Bindungen sind deutlich verwundbarer, es sei denn, spezifische Übergangsmetalle werden substituiert, um die Bindung zu stärken. Das Team schlägt eine einfache Stabilitätskennzahl vor, basierend auf dem Verlust aktiver Alkali-Ionen, die verwendet werden kann, um zu vergleichen, wie verschiedene Materialien und Lösungsmittel bei der Flüssigverarbeitung abschneiden.
Was das für zukünftige Batterien bedeutet
Kurz gesagt zeigt diese Arbeit, dass nicht alle Reinigungsflüssigkeiten gleich sind, wenn es um die Vorbereitung empfindlicher Batteriematerialien geht. Wasser, zwar billig und praktisch, kann natriumbasierte Schichtoxide leise von innen aushöhlen und ihnen die Ionen rauben, die sie zur Energiespeicherung benötigen. Ethylenglykol hingegen kann schädliche Oberflächenrückstände entfernen, ohne die innere Struktur wesentlich zu beeinträchtigen. Indem diese Ergebnisse mit Molekülgröße, Bindungsstärke und Schichtabstand verknüpft werden, liefert die Studie praktische Leitlinien für die Auswahl und Gestaltung von Flüssigbehandlungen, die die Leistung schützen statt sie zu untergraben, und hilft so, Natrium-Batterien der zuverlässigen großtechnischen Nutzung näherzubringen.
Zitation: Zhang, W., Zhu, J., Song, A. et al. Deciphering the liquid-solid interactions in dealkalization of O3 layered oxides. Nat Commun 17, 4166 (2026). https://doi.org/10.1038/s41467-026-70581-2
Schlüsselwörter: Natrium-Batterien, Kathodenmaterialien, Oberflächenchemie, Lösmitteleffekte, Energiespeicherung