Clear Sky Science · nl
Het ontcijferen van vloeistof–vaststofinteracties bij de de-alkalisatie van O3-laagachtige oxiden
Waarom dit batterijonderzoek ertoe doet
Nu de wereld op zoek is naar schonere en goedkopere manieren om hernieuwbare energie op te slaan, komen natrium gebaseerde batterijen naar voren als veelbelovende partners voor de huidige lithium-ioncellen. Een subtiel oppervlaktechemisch probleem maakt echter dat sommige van de meest aantrekkelijke natrium-batterijmaterialen onstabiel worden wanneer ze tijdens de fabricage met vloeistoffen in aanraking komen. Deze studie gaat die verborgen wisselwerking tussen vaste batterijdeeltjes en de gebruikte reinigingsvloeistoffen na en laat zien hoe de keuze van het juiste oplosmiddel het verschil kan maken tussen een robuuste batterij en een die uit elkaar valt voordat hij het net bereikt.
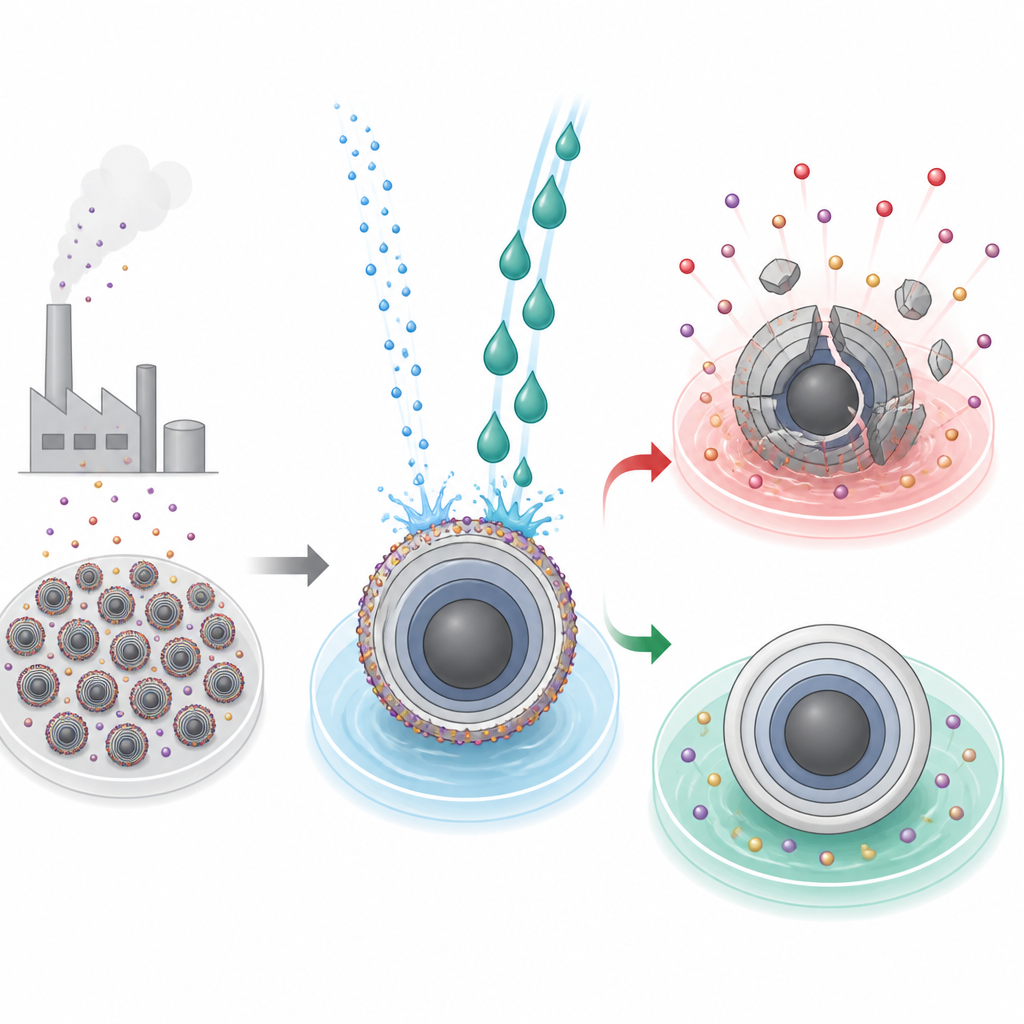
Het verborgen vuil op batterijdeeltjes
Moderne hoogenergetische batterijen vertrouwen op laagachtige oxide-deeltjes in de positieve elektrode, waar ionen in- en uitbewegen tijdens laden en ontladen. Bij de productie van deze materialen gebruiken fabrikanten sterk alkalische omstandigheden die een ongewenste korst van resterende alkaliën op de deeltjesoppervlakken achterlaten. Bij lithium gebaseerde materialen kan deze korst met water worden weggespoeld met gevestigde industriële processen. Voor natrium-analogen kan dezelfde wasbeurt echter een ramp betekenen: water verwijdert niet alleen het residu maar onttrekt ook actieve natriumionen en destabiliseert het kristalrooster, wat leidt tot scheuren, structurele instorting en een scherpe vermindering van de batterijcapaciteit.
Twee vloeistoffen, twee heel verschillende uitkomsten
De onderzoekers richtten zich op een typisch natrium-laagoxide, NaNi1/3Fe1/3Mn1/3O2, dat al wordt gebruikt in pilot-schaal natriumbatterijen. Ze vergeleken water met ethyleenglycol, een veelgebruikt autokoelmiddel, als reinigingsvloeistoffen. Beide oplosmiddelen losten de ongewenste oppervlakte-alkali efficiënt op, maar hun effect op de onderliggende deeltjes verschilden sterk. Met ethyleenglycol behandeld materiaal vertoonde gladdere deeltjesoppervlakken, betere stroom-eigenschappen van de electrode slurry tijdens de productie, sterkere hechting aan stroomverzamelaars, hogere herwonnen capaciteit en verbeterde cyclusstabiliteit. Watergewassen monsters daarentegen leden aan diepe scheuren, verlies van natrium door het hele deeltje, tragere ionentransport en veel lagere capaciteit, samen met verhoogde gasvorming die verband houdt met afbraak van achtergebleven carbonaten bij hoge spanning.
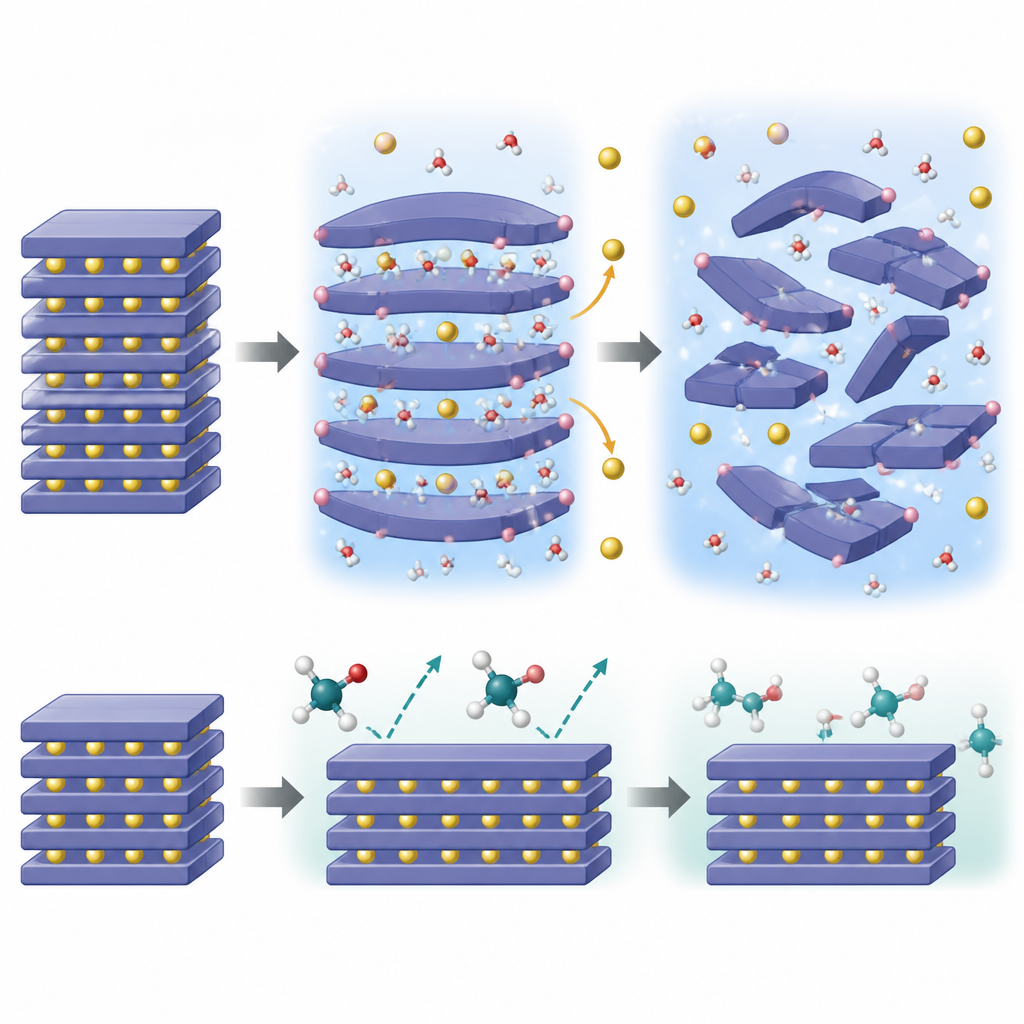
Wat er binnenin de deeltjes gebeurt
Om te begrijpen waarom water zo destructief is, combineerde het team geavanceerde beeldvorming, oppervlaktechemie-onderzoeken, neutronendiffractie en temperatuurafhankelijke röntgenmetingen met kwantummechanische simulaties. Ze ontdekten dat kleine watermoleculen tussen de natriumlagen in het kristal kunnen schuiven, de tussenlagen kunnen vergroten en vervolgens protonen afgeven die binden aan het zuurstofraamwerk. Deze “zelfvermenigvuldigende” invasie leidt ertoe dat natriumionen weg lekken om de lading in evenwicht te houden, waardoor de natriumlagen krimpen en een keten van faseveranderingen en roostervervormingen wordt getriggerd. In de loop van de tijd transformeert de ooit geordende laagstructuur in meer gedesoriënteerde vormen met verschoven of prismatische lagen, en verliest uiteindelijk het vermogen om natrium reversibel op te slaan en vrij te geven.
Waarom ethyleenglycol zich milder gedraagt
De berekeningen tonen aan dat ethyleenglycolmoleculen simpelweg te omvangrijk zijn om zich gemakkelijk tussen de natriumlagen te wringen. Hun insertie in de structuur is energetisch ongunstig, waardoor hun werking beperkt blijft tot het oppervlak. Hoewel ethyleenglycol nog steeds kan bijdragen aan het aanpassen van de oppervlakte-alkaliteit en het verwijderen van resterende natriumverbindingen, zet het niet dezelfde interne kettingreactie van protoneninvasie en natriumverlies in gang. Metingen bevestigen dat massatransfer tussen de vaste stof en de glycolvloeistof beperkt is en dat het laagachtige raamwerk grotendeels intact blijft, zelfs na behandeling. Dit “size-effect” betekent dat ethyleenglycol het oppervlak kan reinigen zonder de structuur van binnenuit open te wrikken.
Van één materiaal naar een algemene ontwerprichtlijn
Voorbij dit specifieke natriumoxide breidden de auteurs hun analyse uit naar andere lithium- en natriumgebaseerde laagachtige kathoden. Ze toonden aan dat of watermoleculen spontaan kunnen intercaleren afhangt van de afstand tussen alkali-ionlagen en de sterkte van de binding tussen die ionen en zuurstof. Lithiumoxiden, met kleinere ionen en strakkere lagen, weerstaan diepe waterpenetratie, waardoor schade grotendeels aan het oppervlak blijft. Natriumoxiden, met bredere lagen en zwakkere bindingen, zijn veel kwetsbaarder, tenzij specifieke overgangsmetalen worden ingebracht om de binding te versterken. Het team stelt een eenvoudige stabiliteitsmaatstaf voor op basis van het verlies van actieve alkali-ionen, die kan worden gebruikt om te vergelijken hoe verschillende materialen en oplosmiddelen presteren tijdens vloeistofverwerking.
Wat dit betekent voor toekomstige batterijen
In eenvoudige bewoordingen laat dit werk zien dat niet alle reinigingsvloeistoffen gelijk zijn bij de voorbereiding van gevoelige batterijmaterialen. Water, hoewel goedkoop en handig, kan stilletjes natrium-gebaseerde laagoxiden van binnenuit uithollen en ze beroven van de ionen die ze nodig hebben om energie op te slaan. Ethyleenglycol daarentegen kan schadelijk oppervlakresidu verwijderen terwijl de interne structuur grotendeels onaangetast blijft. Door deze uitkomsten te koppelen aan molecuulgrootte, bindingssterkte en laagscheiding, biedt de studie praktische richtlijnen voor het kiezen en ontwerpen van vloeistofbehandelingen die prestaties beschermen in plaats van ondermijnen, en helpt zo natriumbatterijen dichter bij betrouwbare grootschalige inzet te brengen.
Bronvermelding: Zhang, W., Zhu, J., Song, A. et al. Deciphering the liquid-solid interactions in dealkalization of O3 layered oxides. Nat Commun 17, 4166 (2026). https://doi.org/10.1038/s41467-026-70581-2
Trefwoorden: natriumbatterijen, kathodematerialen, oppervlaktechemie, oplosmiddeleffecten, energieopslag