Clear Sky Science · ru
Генетическая диагностика ВПР, связанной с CYP21A2: адаптивное секвенирование длинных чтений — точное и масштабируемое решение
Почему это важно для семей и врачей
Многих новорождённых сейчас скринируют на врождённую гиперплазию надпочечников (ВПН) — гормональное расстройство, которое при пропуске может представлять угрозу для жизни. Подтвердить диагноз на уровне ДНК при этом оказывается неожиданно сложно, потому что ключевой ген расположен в запутанном участке нашего генома рядом с почти идентичным «обманным» геном‑двойником. В этом исследовании показано, что новый способ чтения ДНК — адаптивное секвенирование длинных чтений — способен преодолеть эту путаницу и дать пациентам и их семьям более быстрые и надёжные ответы.
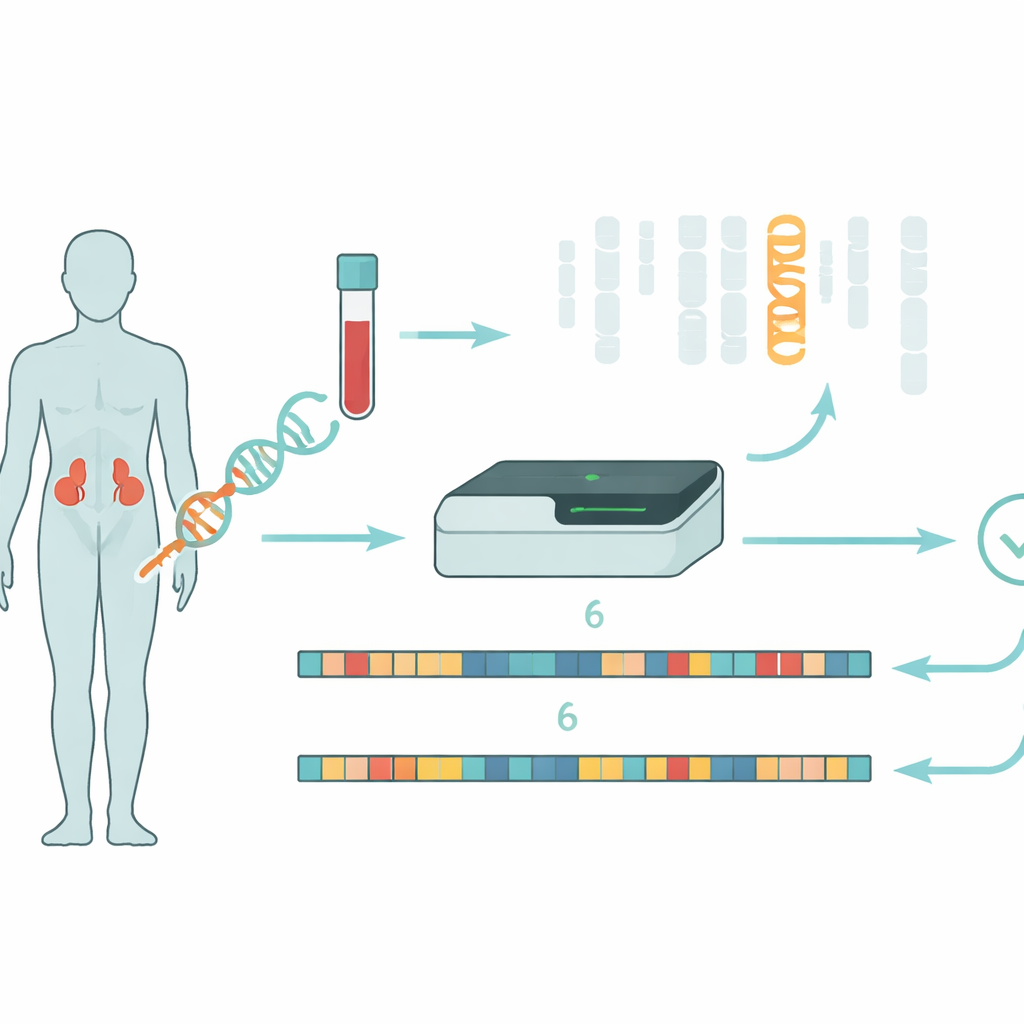
Гормональное заболевание с генетическими нюансами
Врожденная гиперплазия надпочечников (ВПН) нарушает синтез важнейших гормонов надпочечниками, которые регулируют водно‑солевой баланс, реакции на стресс и уровень половых гормонов. Примерно в 95 % случаев причина кроется в изменениях одного гена — CYP21A2, кодирующего 21‑гидроксилазу. При отсутствии или сниженной активности этого фермента организм не может вырабатывать достаточное количество кортизола и альдостерона и вместо этого избыточно производит андрогены, что проявляется как salt‑wasting кризы у новорождённых или повышенным оволосением и проблемами с фертильностью в более позднем возрасте. У большинства пациентов на каждой копии гена встречаются разные патогенные варианты, и сочетание этих вариантов существенно влияет на тяжесть заболевания.
Ген, прячущийся рядом со своим двойником
Основная проблема в том, что CYP21A2 находится в сложном участке на хромосоме 6 рядом с почти идентичным «псевдогеном» CYP21A1P, который утратил функцию. Их последовательности ДНК примерно на 98 % совпадают, а регион склонен к перерасположениям, при которых фрагменты рабочего гена и псевдогена обмениваются местами, сливаются или удаляются. Традиционные методы тестирования опираются на амплификацию отдельных участков ДНК методом ПЦР с последующим прочтением по Сэнгеру, иногда в сочетании с MLPA для подсчёта копий гена. Эти методы медленные, трудоёмкие и могут не справляться с обнаружением крупных реаранжировок или с определением, находятся ли несколько вариантов на одной хромосоме или на разных — информация, критически важная для оценки риска у пациента и родственников.
Новый способ читать проблемный участок
Исследователи опробовали иной подход, используя длинное секвенирование на платформе Oxford Nanopore. Вместо разрезания ДНК на очень короткие фрагменты эта технология читает значительно большие отрезки, что помогает связать удалённые особенности на хромосоме. Они применили «адаптивную выборку», когда секвенсор в реальном времени направляют на выбранный регион — в данном случае хромосому 6 — повышая покрытие без сложных лабораторных процедур. ДНК из 34 пациентов с клиническим диагнозом ВПН секвенировали без ПЦР, избегая искажений, при которых один из вариантов гена может исчезнуть из анализа. Чтобы справиться с экстремальным сходством CYP21A2 и его псевдогена, команда создала специализированный софт NanoCAH, который внимательно анализирует, как каждое длинное чтение выравнивается, решает, действительно ли оно принадлежит рабочему гену или «обманке», и реконструирует две версии участка у каждого пациента.
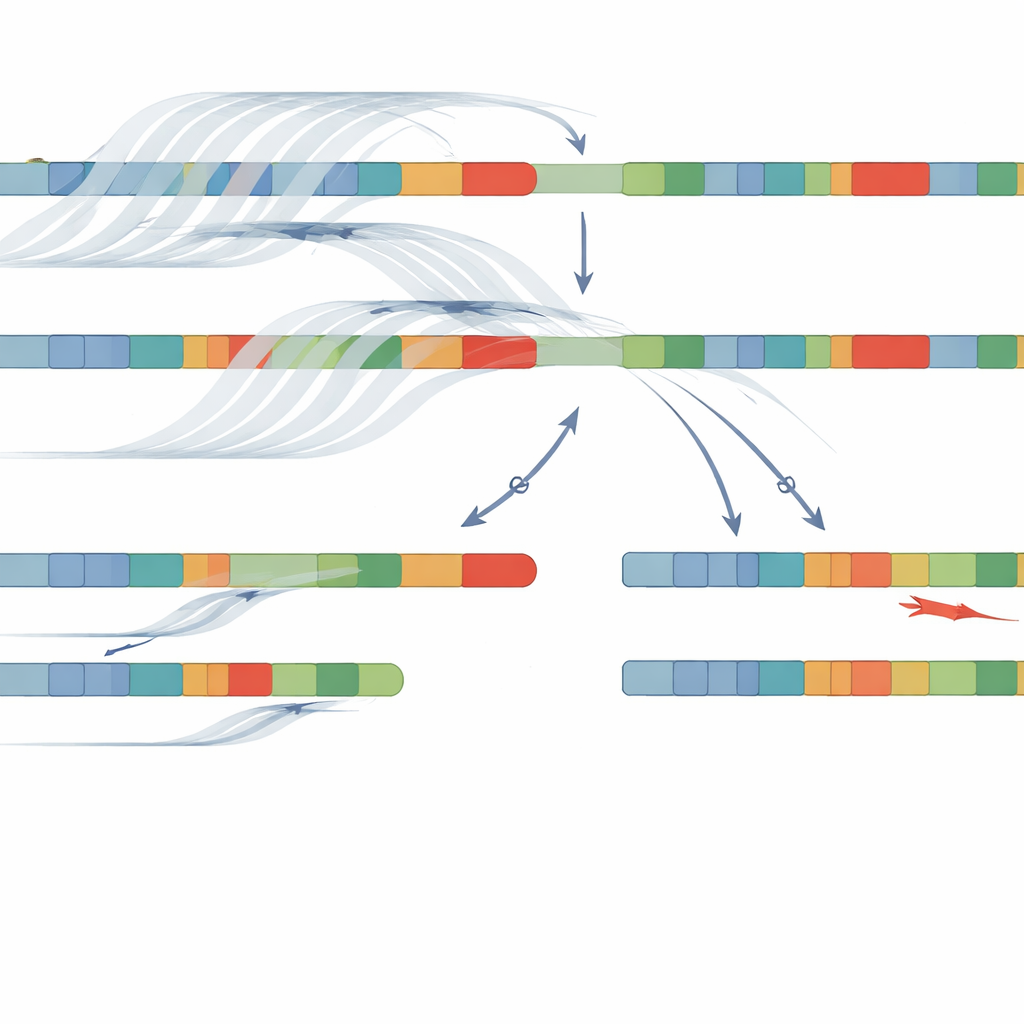
Более чёткие ответы у большинства пациентов
Сочетание адаптивного секвенирования длинных чтений и NanoCAH позволило команде выявить патогенные изменения у 32 из 34 пациентов, что соответствует 94 % успешности. Они не только подтвердили почти все находки старых методов, но и обнаружили важные детали, ранее пропущенные или ошибочно классифицированные. У некоторых пациентов предыдущие тесты ошибочно отмечали вариант как «гомозиготный», то есть будто обе хромосомы несли одно и то же повреждение; новый метод показал, что на одной хромосоме на самом деле была делеция или сложный фьюжн между геном и псевдогеном. У других были выявлены ранее незамеченные точечные замены, поскольку новый подход читает весь регион, а не фиксированный набор распространённых «горячих» участков. И что важно, длинные чтения позволили пропхить варианты — показать, какие изменения находятся вместе на одной хромосоме — без необходимости иметь ДНК родителей.
Что это значит для будущего тестирования
Авторы приходят к выводу, что адаптивное секвенирование длинных чтений в сочетании со специализированным аналитическим ПО может обеспечить более быстрое, масштабируемое и точное генетическое тестирование при ВПН по сравнению с текущими стандартными методами. Давая более ясную картину сложных реаранжировок генов и надёжно разделяя реальный ген и его близкий двойник, этот подход может улучшить диагностику, помочь в выборе лечения и поддержать более точное обследование носителей и пренатальную диагностику в семьях. Поскольку многие другие гены, связанные с заболеваниями, также локализованы в запутанных, повторяющихся участках ДНК, та же стратегия может помочь разрешить сложные генетические вопросы далеко за пределами ВПН.
Цитирование: Lildballe, D.L., Huno, M.R., Ridder, L.O.R. et al. Genetic diagnosis of CYP21A2-related CAH: adaptive sampling long-read sequencing is an accurate and scalable solution. Eur J Hum Genet 34, 535–542 (2026). https://doi.org/10.1038/s41431-026-02019-8
Ключевые слова: врожденная гиперплазия надпочечников, CYP21A2, длинное секвенирование, генетическая диагностика, адаптивная выборка