Clear Sky Science · pt
Diagnóstico genético da HAC relacionada ao CYP21A2: sequenciamento de leitura longa com amostragem adaptativa é uma solução precisa e escalável
Por que isso importa para famílias e médicos
Muitos recém‑nascidos hoje são triados ao nascer para hiperplasia adrenal congênita, um distúrbio hormonal que pode ser fatal se não for detectado. Ainda assim, confirmar o diagnóstico ao nível do DNA é surpreendentemente difícil, porque o gene-chave está em um trecho confuso do nosso genoma com um gene “isca” quase idêntico. Este estudo mostra que um novo tipo de leitura de DNA, chamado sequenciamento de leitura longa com amostragem adaptativa, pode cortar essa confusão, oferecendo respostas mais rápidas e confiáveis para pacientes e suas famílias.
Um distúrbio hormonal com voltas genéticas
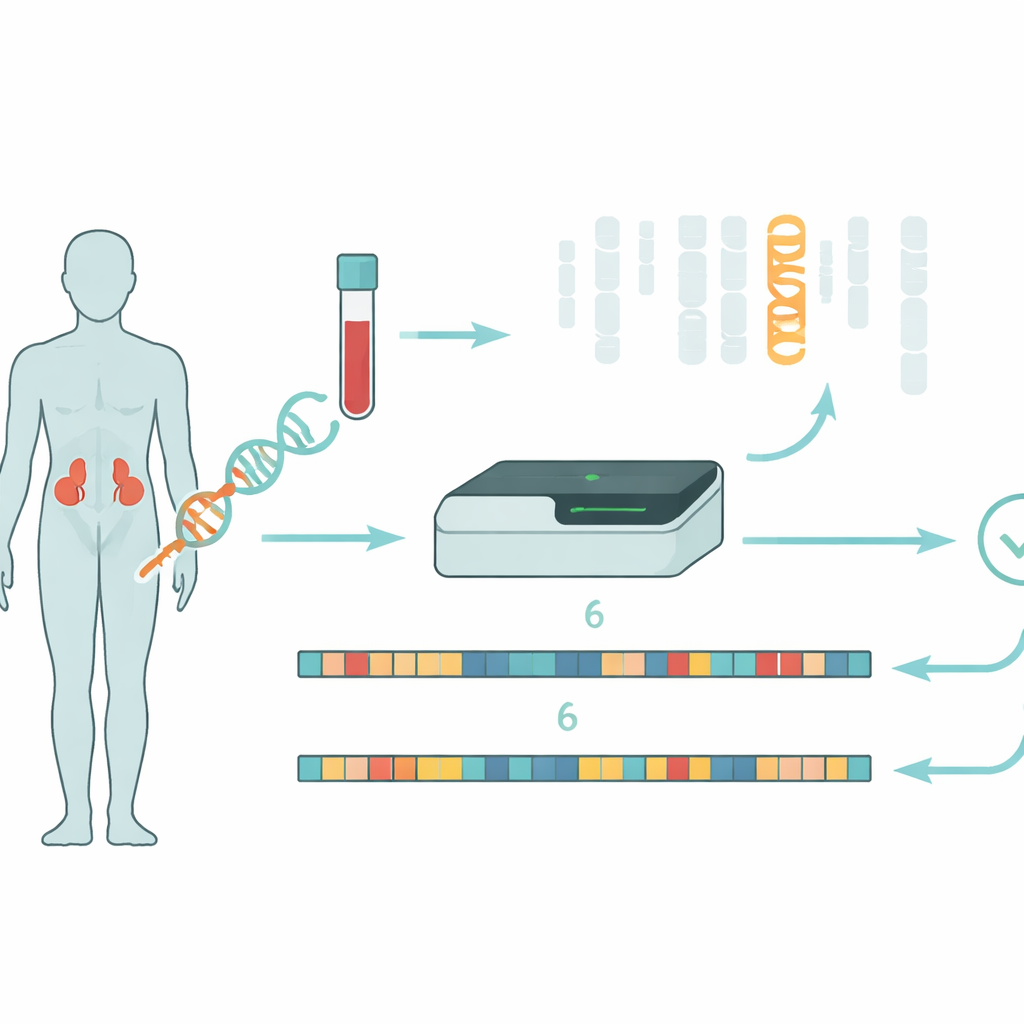
A hiperplasia adrenal congênita (HAC) afeta como as glândulas adrenais produzem hormônios vitais que controlam o equilíbrio de sais, respostas ao estresse e níveis de hormônios sexuais. Em cerca de 95% dos casos, o problema remete a alterações em um único gene, CYP21A2, que ajuda a produzir a enzima 21‑hidroxilase. Se essa enzima falta ou é deficiente, o corpo não consegue produzir cortisol e aldosterona suficientes e, em vez disso, superproduz andrógenos, levando a sintomas que variam de crises de perda de sal em recém‑nascidos até excesso de pelos e problemas de fertilidade mais tarde na vida. A maioria dos pacientes carrega alterações causadoras de doença diferentes em cada cópia do gene, e a combinação dessas alterações influencia fortemente a gravidade da doença.
Um gene escondido ao lado de seu sósia
O verdadeiro desafio é que o CYP21A2 está em um bairro complicado no cromossomo 6 ao lado de um “pseudogene” quase idêntico, CYP21A1P, que não funciona mais. O código de DNA deles é cerca de 98% igual, e a região é propensa a eventos de reordenação nos quais pedaços do gene funcional e do pseudogene trocam de lugar, se fundem ou são deletados. Métodos tradicionais dependem de amplificar trechos específicos de DNA por PCR e em seguida lê‑los com sequenciamento Sanger, às vezes combinados com uma técnica chamada MLPA para contar cópias do gene. Esses métodos são lentos, trabalhosos e podem ter dificuldade em detectar grandes rearranjos ou em dizer se várias alterações estão no mesmo cromossomo ou em cromossomos diferentes — informação crucial para entender o risco de doença em pacientes e parentes.
Uma nova maneira de ler a região complicada
Os pesquisadores exploraram uma estratégia diferente usando sequenciamento de leitura longa na plataforma Oxford Nanopore. Em vez de fragmentar o DNA em pedaços muito curtos, essa tecnologia lê trechos muito mais longos, o que ajuda a conectar características distantes ao longo do cromossomo. Eles usaram “amostragem adaptativa”, onde o sequenciador é instruído em tempo real a focar em uma região escolhida — neste caso o cromossomo 6 — aumentando a cobertura sem etapas laboratoriais complexas. De 34 pacientes com diagnóstico clínico de HAC, o DNA foi sequenciado sem PCR, evitando vieses que podem fazer uma versão do gene desaparecer da visualização. Para lidar com a extrema similaridade entre CYP21A2 e seu pseudogene, a equipe desenvolveu uma ferramenta de software personalizada chamada NanoCAH, que examina cuidadosamente como cada leitura longa de DNA se alinha, decide se ela realmente vem do gene funcional ou do engodo, e reconstrói as duas versões da região de cada paciente.
Respostas mais claras na maioria dos pacientes
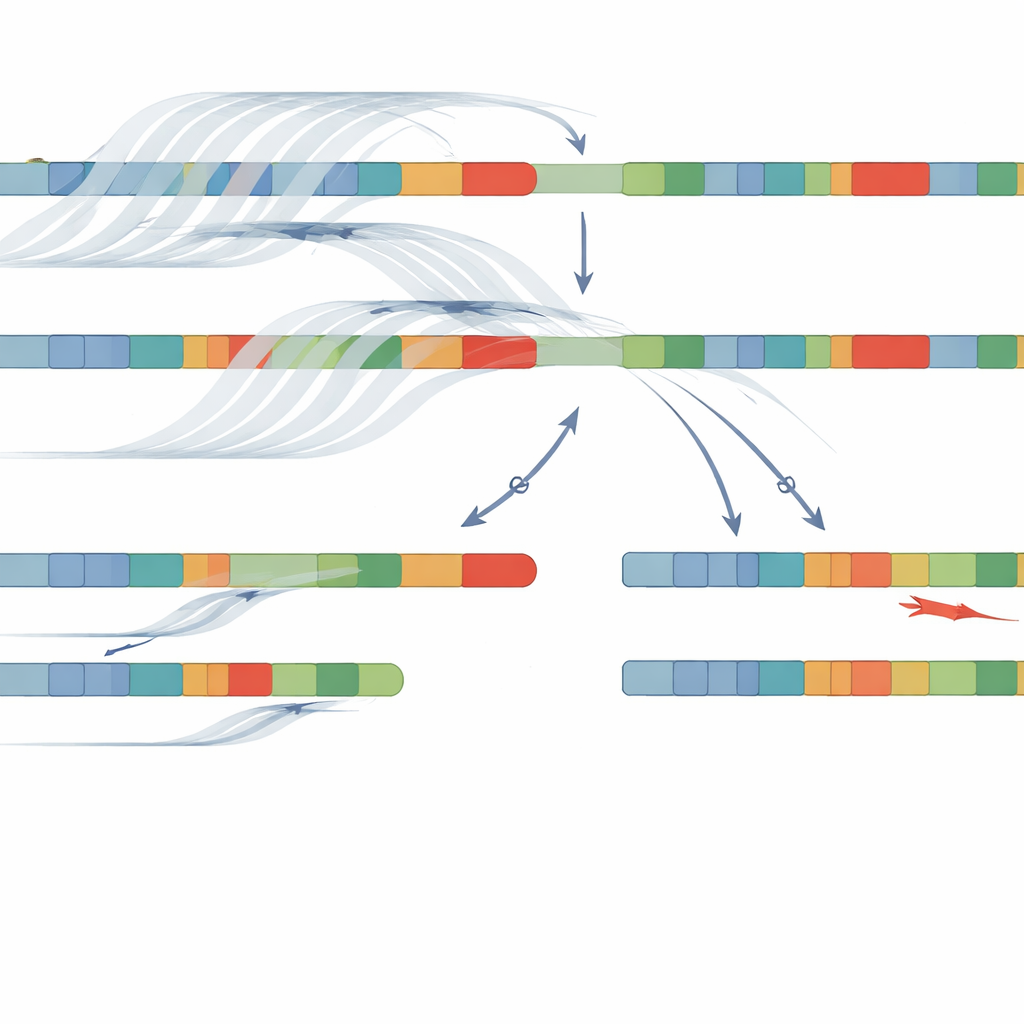
Usando essa combinação de sequenciamento de leitura longa com amostragem adaptativa e o NanoCAH, a equipe identificou alterações genéticas causadoras da doença em 32 dos 34 pacientes, uma taxa de sucesso de 94%. Eles não apenas confirmaram quase todos os achados dos métodos antigos, como também descobriram detalhes importantes que haviam sido perdidos ou classificados erroneamente. Em alguns pacientes, testes anteriores haviam chamado uma alteração de “homozigótica”, como se ambos os cromossomos carregassem o mesmo erro; o novo método revelou que um cromossomo na verdade continha uma deleção ou uma fusão complexa entre o gene e o pseudogene. Em outros, erros de escrita (missense) previamente não vistos no gene foram identificados porque a nova abordagem lê toda a região em vez de um conjunto fixo de pontos quentes comuns. Crucialmente, as leituras longas permitiram à equipe “fasear” variantes — mostrando quais alterações estão juntas no mesmo cromossomo — sem precisar do DNA dos pais.
O que isso significa para testes futuros
O estudo conclui que o sequenciamento de leitura longa com amostragem adaptativa, aliado a softwares de análise especializados, pode oferecer diagnósticos genéticos para HAC mais rápidos, escaláveis e precisos do que os testes padrão atuais. Ao fornecer uma imagem mais clara de rearranjos complexos do gene e separar de forma confiável o gene real de seu quase‑gêmeo, essa abordagem pode melhorar o diagnóstico, orientar decisões de tratamento e apoiar testes de portadores e pré‑natal mais precisos em famílias afetadas. Como muitos outros genes relacionados a doenças também estão localizados em trechos emaranhados e repetitivos do nosso DNA, a mesma estratégia pode ajudar a desvendar questões genéticas difíceis muito além da HAC.
Citação: Lildballe, D.L., Huno, M.R., Ridder, L.O.R. et al. Genetic diagnosis of CYP21A2-related CAH: adaptive sampling long-read sequencing is an accurate and scalable solution. Eur J Hum Genet 34, 535–542 (2026). https://doi.org/10.1038/s41431-026-02019-8
Palavras-chave: hiperplasia adrenal congênita, CYP21A2, sequenciamento de leitura longa, diagnóstico genético, amostragem adaptativa