Clear Sky Science · es
Diagnóstico genético de la HSC relacionada con CYP21A2: el secuenciamiento de lectura larga con muestreo adaptativo es una solución precisa y escalable
Por qué esto importa para familias y médicos
Hoy en día muchos recién nacidos se analizan al nacer para detectar la hiperplasia suprarrenal congénita, un trastorno hormonal que puede poner en riesgo la vida si pasa desapercibido. Sin embargo, confirmar el diagnóstico a nivel del ADN resulta sorprendentemente difícil, porque el gen clave se encuentra en un tramo confuso de nuestro genoma junto a un gen “señuelo” casi idéntico. Este estudio demuestra que un nuevo tipo de lectura del ADN, denominado secuenciación de lectura larga con muestreo adaptativo, puede atravesar esa confusión y proporcionar respuestas más rápidas y fiables para los pacientes y sus familias.
Un trastorno hormonal con giros genéticos
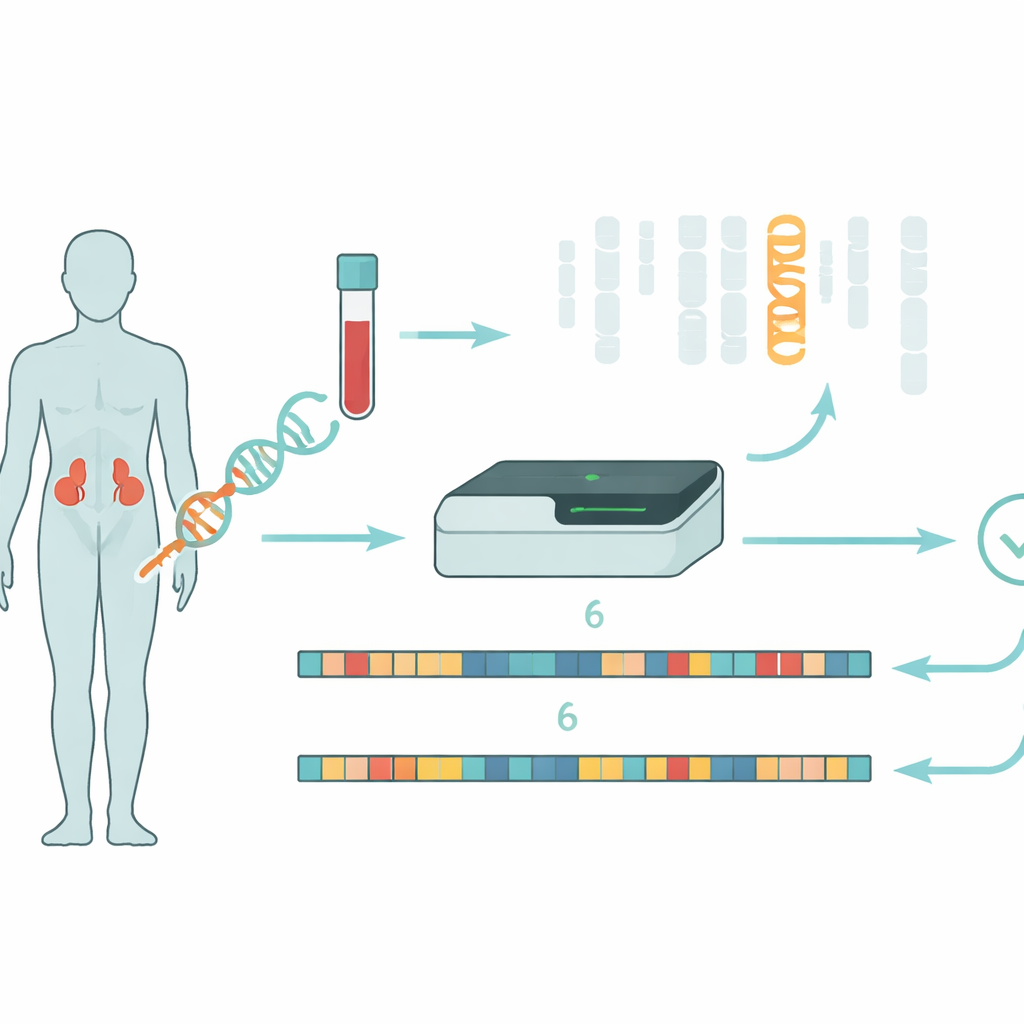
La hiperplasia suprarrenal congénita (HSC) afecta la forma en que las glándulas suprarrenales producen hormonas vitales que regulan el equilibrio de sal, las respuestas al estrés y los niveles de hormonas sexuales. En aproximadamente el 95 por ciento de los casos, el problema se remonta a alteraciones en un único gen, CYP21A2, que participa en la producción de la enzima 21‑hidroxilasa. Si esa enzima falta o es débil, el organismo no puede producir suficiente cortisol y aldosterona y, en cambio, sobreproduce andrógenos, lo que provoca síntomas que van desde crisis de pérdida de sal en recién nacidos hasta aumento del vello corporal y problemas de fertilidad en etapas posteriores de la vida. La mayoría de los pacientes portan cambios patogénicos diferentes en cada copia del gen, y la combinación de esos cambios influye en gran medida en la severidad de la enfermedad.
Un gen que se esconde junto a su doble parecido
El verdadero desafío es que CYP21A2 se sitúa en un vecindario complejo del cromosoma 6 junto a un “pseudogen” casi idéntico, CYP21A1P, que ya no funciona. Su secuencia de ADN es aproximadamente un 98 por ciento igual, y la región es proclive a eventos de reorganización en los que fragmentos del gen funcional y del pseudogen se intercambian, se fusionan o se eliminan. Los métodos de prueba tradicionales se basan en amplificar tramos específicos de ADN por PCR y luego leerlos con secuenciación Sanger, a veces combinados con una técnica llamada MLPA para cuantificar copias génicas. Estos métodos son lentos, requieren mucho trabajo y pueden tener dificultades para detectar reordenamientos grandes o para determinar si múltiples cambios están en el mismo cromosoma o en los opuestos —información crucial para comprender el riesgo genético en pacientes y familiares.
Una nueva forma de leer la región difícil
Los investigadores exploraron una estrategia distinta usando secuenciación de lectura larga en la plataforma Oxford Nanopore. En lugar de fragmentar el ADN en trozos muy cortos, esta tecnología lee tramos mucho más largos, lo que ayuda a conectar características distantes a lo largo del cromosoma. Emplearon “muestreo adaptativo”, donde el secuenciador recibe instrucciones en tiempo real para centrarse en una región seleccionada —en este caso el cromosoma 6— aumentando la cobertura sin pasos laboratoriales complejos. A partir de 34 pacientes con diagnóstico clínico de HSC, el ADN se secuenció sin PCR, evitando sesgos que pueden hacer que una versión del gen desaparezca de la vista. Para manejar la extrema similitud entre CYP21A2 y su pseudogen, el equipo desarrolló una herramienta de software personalizada llamada NanoCAH, que examina cuidadosamente cómo se alinea cada lectura larga de ADN, decide si realmente procede del gen funcional o del señuelo, y reconstruye las dos versiones de la región en cada paciente.
Respuestas más claras en la mayoría de los pacientes
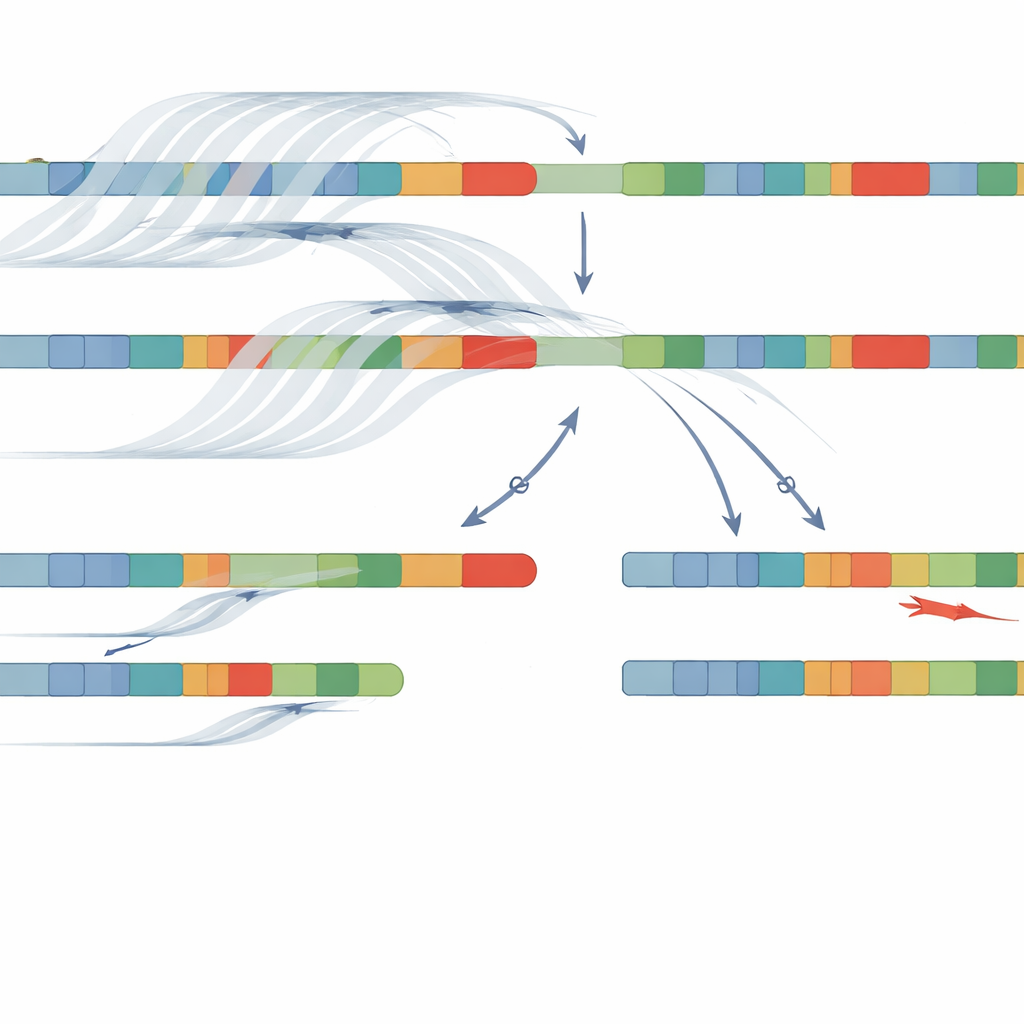
Usando esta combinación de secuenciación de lectura larga con muestreo adaptativo y NanoCAH, el equipo identificó cambios patogénicos en el ADN en 32 de los 34 pacientes, una tasa de éxito del 94 por ciento. No solo confirmaron casi todos los hallazgos de métodos anteriores, sino que también descubrieron detalles importantes que habían pasado desapercibidos o habían sido mal clasificados. En algunos pacientes, pruebas anteriores habían etiquetado un cambio como “homocigoto”, como si ambos cromosomas llevaran el mismo error; el nuevo método reveló que un cromosoma en realidad presentaba una deleción o una fusión compleja entre el gen y el pseudogen. En otros, se identificaron errores de lectura (missense) no detectados previamente porque el nuevo enfoque lee toda la región en lugar de un conjunto fijo de puntos calientes comunes. De manera crucial, las lecturas largas permitieron al equipo «fasear» las variantes —mostrar qué cambios están juntos en el mismo cromosoma— sin necesitar ADN de los progenitores.
Qué significa esto para las pruebas futuras
El estudio concluye que la secuenciación de lectura larga con muestreo adaptativo, junto con software de análisis especializado, puede ofrecer diagnósticos genéticos para HSC más rápidos, escalables y precisos que las pruebas estándar actuales. Al proporcionar una imagen más clara de los reordenamientos complejos de genes y separar de manera fiable el gen real de su casi gemelo, este enfoque puede mejorar el diagnóstico, orientar decisiones terapéuticas y facilitar pruebas de portadores y prenatales más precisas en familias afectadas. Dado que muchos otros genes relacionados con enfermedades también se encuentran en tramos enredados y repetitivos de nuestro ADN, la misma estrategia podría ayudar a despejar preguntas genéticas complejas mucho más allá de la HSC.
Cita: Lildballe, D.L., Huno, M.R., Ridder, L.O.R. et al. Genetic diagnosis of CYP21A2-related CAH: adaptive sampling long-read sequencing is an accurate and scalable solution. Eur J Hum Genet 34, 535–542 (2026). https://doi.org/10.1038/s41431-026-02019-8
Palabras clave: hiperplasia suprarrenal congénita, CYP21A2, secuenciación de lectura larga, diagnóstico genético, muestreo adaptativo