Clear Sky Science · pt
Divergência transcricional precoce subjaz a viés de destino celular em embriões bovinos
Como as primeiras escolhas da vida podem moldar um bezerro
Todo mamífero, incluindo humanos e bovinos, começa a vida como uma única célula que se divide repetidamente. Por décadas, biólogos presumiram que as primeiras células nessa pequena esfera eram todas iguais, cada uma com o mesmo potencial para se tornar qualquer parte do corpo futuro ou seus tecidos de suporte. Este estudo em embriões de bovino desafia essa visão simplista, mostrando que algumas células começam a tender para futuros específicos bem antes de parecerem diferentes ao microscópio.
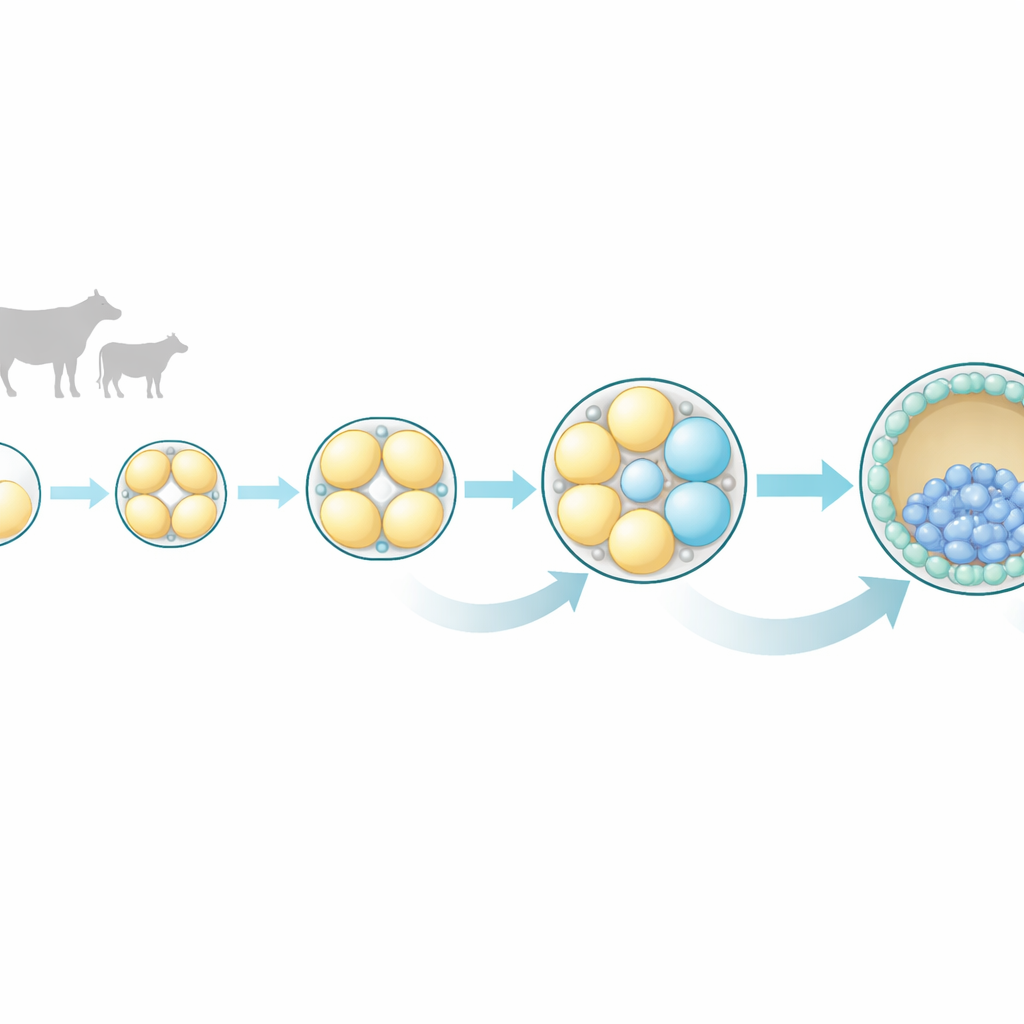
As divisões celulares iniciais não são tão iguais quanto parecem
Os pesquisadores focaram em embriões bovinos porque seu desenvolvimento inicial se assemelha ao humano em timing e padrão. Recolheram embriões em quatro estágios muito precoces: o zigoto unicelular e os estágios de 2, 4 e 8 células. De cada embrião, separaram cuidadosamente todas as células individuais e mediram quais genes estavam ativos em cada uma usando sequenciamento de RNA de célula única, uma técnica que revela a “lista de afazeres” molecular de uma célula. Essa abordagem permitiu comparar células-irmãs do mesmo embrião e perguntar quão similares ou diferentes elas realmente eram à medida que o desenvolvimento progredia.
Diferenças crescentes surgem nos estágios de 4 e 8 células
No estágio de 2 células, as duas células-irmãs pareciam quase idênticas em sua atividade gênica, apoiando a visão tradicional de potencial igual nesse ponto. Mas já no estágio de 4 células começaram a surgir diferenças sutis, e no estágio de 8 células essas diferenças tornaram-se marcantes. Células do mesmo embrião de 8 células deixaram de se agrupar com base em seus perfis de expressão gênica; em vez disso, cada célula seguiu seu próprio caminho molecular. Muitos dos genes que mais variaram estavam ligados a vias de comunicação intracelular, especialmente um conjunto conhecido como MAPK, junto com as vias de sinalização Ras e Wnt relacionadas. Essas vias já são conhecidas em outras espécies por orientar se uma célula se tornará parte do embrião propriamente dito ou da camada externa que forma a placenta.
Sugestões de papéis futuros nas camadas externa versus interna
A equipe prestou atenção especial a um gene chamado CDX2, um marcador clássico da camada externa (trofectoderme) que eventualmente ajudará a formar a placenta. No estágio de 8 células, algumas células apresentavam níveis mais altos de CDX2 do que suas irmãs. Essas células com CDX2 elevado também mostraram maior atividade de genes relacionados à via MAPK, e a ligação entre CDX2 e esses genes de sinalização tornou-se mais forte do estágio de 4 células para o de 8 células. Esse padrão sugere que, mesmo antes do embrião se compactar em uma esfera lisa e posicionar células externamente ou internamente, algumas células já estão inclinadas a se tornar parte da camada externa formadora da placenta.
Tamanho celular pende a balança para tecidos de suporte
Curiosamente, diferenças físicas entre as células corresponderam a esses vieses moleculares. Dentro do mesmo embrião, alguns blastômeros eram maiores que outros tanto nos estágios de 4 quanto de 8 células. Células maiores tendiam a expressar mais CDX2 e genes relacionados à MAPK. Também mostraram maiores quantidades de uma proteína chamada YAP em seus núcleos, um conhecido indutor de identidade de camada externa em embriões precoces. Quando os cientistas acompanharam células únicas grandes ou pequenas em cultura, embriões derivados de blastômeros maiores compactaram mais cedo, passaram por uma rodada extra de divisão antes da compactação e formaram cavidades preenchidas por líquido de forma mais confiável e estável. Quando embriões reconstruídos foram feitos inteiramente a partir das maiores ou das menores células, os formados a partir das maiores desenvolveram-se de forma mais robusta e produziram mais células da camada externa, mantendo ainda as células internas formadoras do embrião.
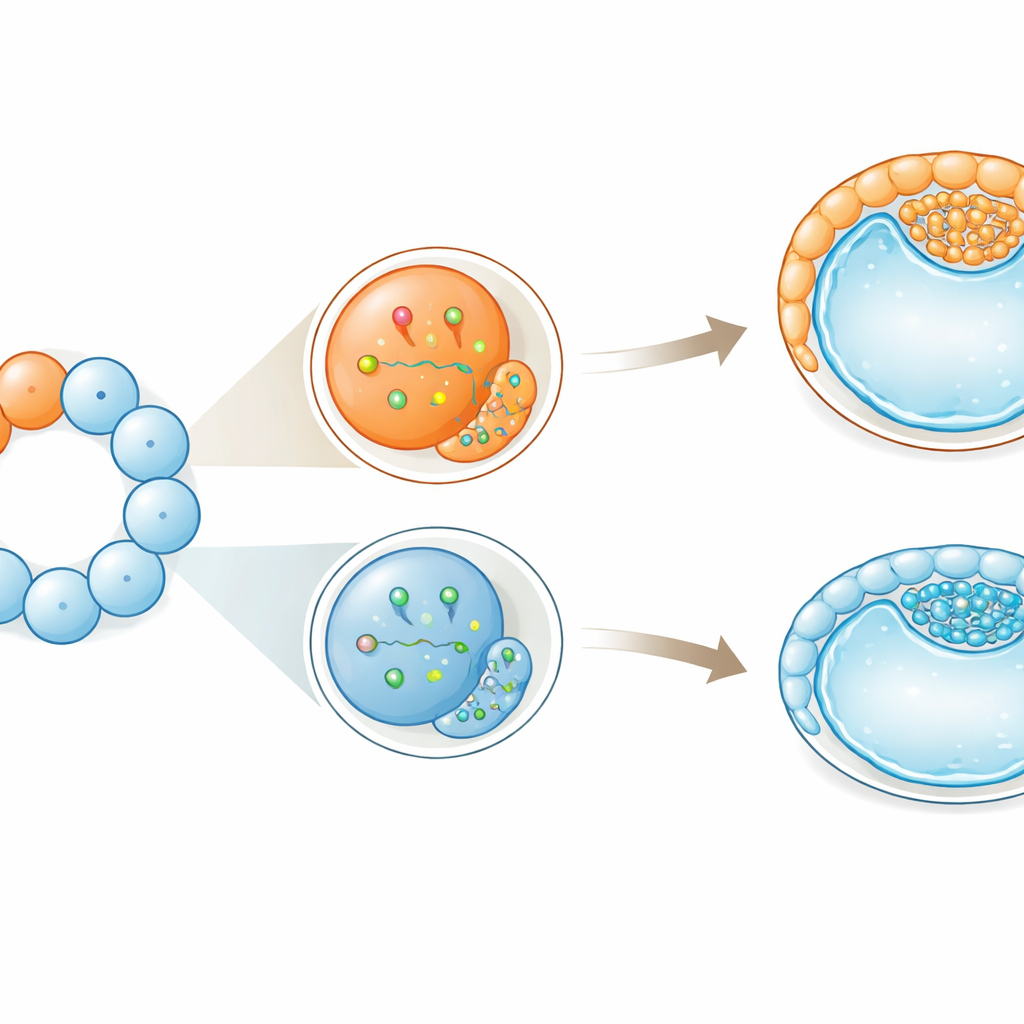
Viés precoce sem perda de flexibilidade
Apesar dessas inclinações iniciais para papéis particulares, as células não perderam totalmente sua flexibilidade. Mesmo as células maiores, mais inclinadas à camada externa, ainda podiam contribuir tanto para o embrião quanto para os tecidos de suporte. Os autores propõem que essas diferenças iniciais atuam como empurrões suaves em vez de ordens rígidas: elas enviesam as probabilidades de um destino sem torná-lo irrevogável. Em bovinos, cujo desenvolvimento inicial se assemelha mais ao humano do que ao do camundongo, isso sugere que a quebra de simetria — pequenas distribuições desiguais de moléculas e comportamentos celulares — começa mais cedo do que estruturas visíveis revelam. Para reprodução assistida e biópsia embrionária, tanto em animais de produção quanto potencialmente em humanos, o trabalho ressalta que nem todas as primeiras células são intercambiáveis, e que sondá-las ou removê-las nesses estágios pode influenciar sutilmente como as primeiras decisões de destino celular do embrião se desenrolam.
Citação: Koyama, H., Mashiko, D., Ferré-Pujol, P. et al. Early transcriptional divergence underlies cell fate bias in bovine embryos. Commun Biol 9, 625 (2026). https://doi.org/10.1038/s42003-026-10198-9
Palavras-chave: desenvolvimento de embrião bovino, viés de destino celular, sequenciamento de RNA de célula única, linhagem trofectoderme, embriogênese precoce