Clear Sky Science · de
Frühe transkriptionelle Divergenz als Grundlage für Zellschicksals-Bias in bovinen Embryonen
Wie die ersten Entscheidungen des Lebens ein Kalb prägen können
Jedes Säugetier, einschließlich Menschen und Rinder, beginnt sein Leben als einzelne Zelle, die sich wiederholt teilt. Jahrzehntelang gingen Biologen davon aus, dass die frühesten Zellen in dieser winzigen Kugel alle gleich seien und jede das gleiche Potenzial habe, Teil des späteren Körpers oder seiner Stützgewebe zu werden. Diese Studie an Rinderembryonen hinterfragt dieses einfache Bild und zeigt, dass einige Zellen bereits deutlich früher in Richtung bestimmter Zukünfte tendieren, lange bevor sie unter dem Mikroskop anders aussehen.
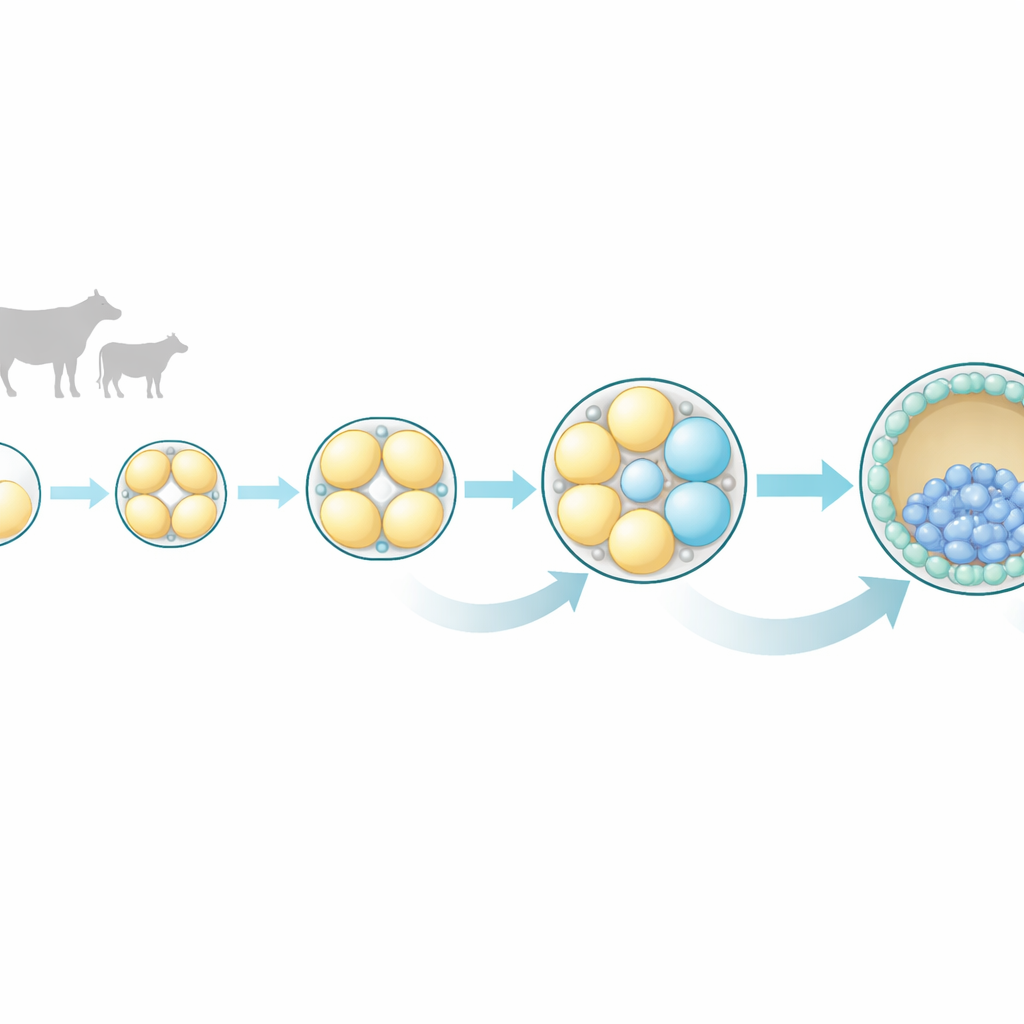
Frühe Zellteilungen sind nicht so gleich, wie sie scheinen
Die Forschenden konzentrierten sich auf bovine Embryonen, weil deren frühe Entwicklung in Timing und Muster der des Menschen ähnlich ist. Sie sammelten Embryonen in vier sehr frühen Stadien: die Einzell-Zygote sowie die 2-, 4- und 8-Zell-Stadien. Aus jedem Embryo trennten sie sorgfältig alle Einzelzellen und bestimmten, welche Gene in jeder einzelnen aktiv waren, mithilfe der Einzelzell-RNA-Sequenzierung — einer Technik, die die molekulare „To-do-Liste“ einer Zelle offenlegt. Dieser Ansatz erlaubte es ihnen, Schwesterzellen desselben Embryos zu vergleichen und zu untersuchen, wie ähnlich oder unterschiedlich sie sich im Verlauf der Entwicklung tatsächlich verhielten.
Wachsende Unterschiede zeigen sich bereits im 4- und 8-Zell-Stadium
Im 2-Zell-Stadium wirkten die beiden Schwesterzellen in ihrer Genaktivität nahezu identisch, was die traditionelle Sicht der gleichen Potenziale zu diesem Zeitpunkt stützt. Im 4-Zell-Stadium traten jedoch subtile Unterschiede auf, und im 8-Zell-Stadium wurden diese Unterschiede deutlich ausgeprägter. Zellen desselben 8-Zell-Embryos gruppierten sich nicht mehr nach ähnlichen Expressionsprofilen; stattdessen schlug jede Zelle ihren eigenen molekularen Weg ein. Viele der Gene mit den stärksten Unterschieden standen im Zusammenhang mit intrazellulären Kommunikationswegen, insbesondere einer Gruppe, die als MAPK bekannt ist, sowie den verwandten Ras- und Wnt-Signalwegen. Diese Pfade sind in anderen Spezies bereits dafür bekannt, zu steuern, ob eine Zelle zum Embryo selbst oder zur äußeren Schicht beiträgt, die die Plazenta bildet.
Hinweise auf künftige Rollen in äußeren gegenüber inneren Zellschichten
Das Team richtete besondere Aufmerksamkeit auf ein Gen namens CDX2, einen klassischen Marker der äußeren Schicht (Trophektoderm), die später an der Plazentabildung beteiligt ist. Im 8-Zell-Stadium wiesen einige Zellen höhere CDX2-Spiegel als ihre Schwestern auf. Diese CDX2-starken Zellen zeigten auch eine stärkere Aktivität von MAPK-bezogenen Genen, und die Verbindung zwischen CDX2 und diesen Signalgene wurde vom 4- zum 8-Zell-Stadium enger. Dieses Muster legt nahe, dass einige Zellen bereits bevor der Embryo zur kompakten Kugel wird und Zellen außen oder innen positioniert sind, eine Neigung haben, Teil der äußeren, plazentabildenden Schicht zu werden.
Zellgröße verschiebt das Gleichgewicht zugunsten der Stützgewebe
Interessanterweise korrespondierten physische Unterschiede zwischen Zellen mit diesen molekularen Tendenzen. Innerhalb desselben Embryos waren einige Blastomeren in den 4- und 8-Zell-Stadien größer als andere. Größere Zellen neigten dazu, mehr CDX2 und MAPK-bezogene Gene zu exprimieren. Sie zeigten außerdem höhere Mengen eines Proteins namens YAP im Zellkern, ein bekannter Treiber der Außenschicht-Identität in frühen Embryonen. Als die Forschenden einzelne große oder kleine Zellen in Kultur verfolgten, verdichteten sich Embryonen, die von größeren Blastomeren abstammten, früher, durchliefen vor der Verdichtung noch eine zusätzliche Teilungsrunde und bildeten verlässlichere und stabilere flüssigkeitsgefüllte Hohlräume. Als rekonstruierte Embryonen vollständig aus den größten oder kleinsten Zellen zusammengesetzt wurden, entwickelten sich die aus größeren Zellen gebildeten Embryonen robuster und erzeugten mehr Außenschichtzellen, während sie gleichzeitig innere, embryo-bildende Zellen beibehielten.
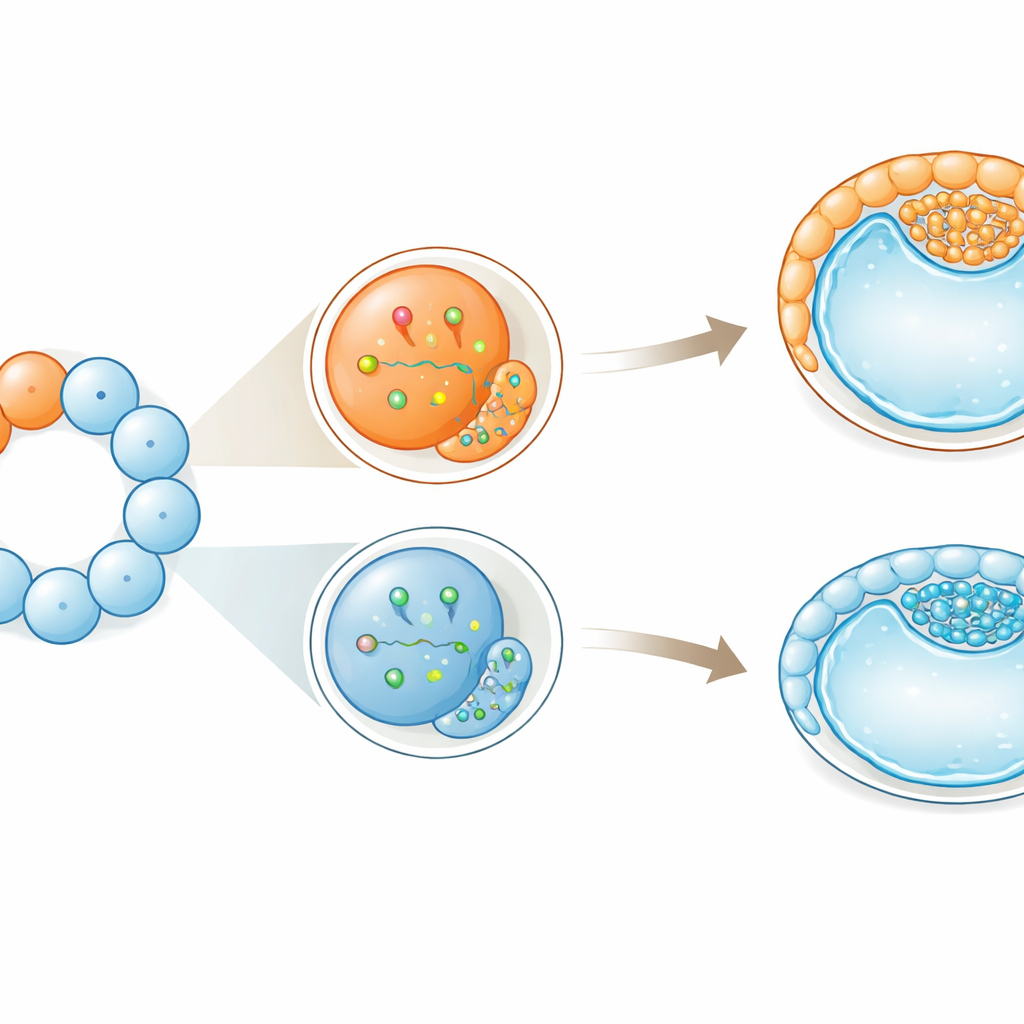
Frühe Tendenz ohne Verlust der Flexibilität
Trotz dieser frühen Neigungen zu bestimmten Rollen verloren die Zellen nicht vollständig ihre Flexibilität. Selbst die stärker „außen geneigten" großen Zellen konnten weiterhin sowohl zum Embryo als auch zu den unterstützenden Geweben beitragen. Die Autoren schlagen vor, dass diese frühen Unterschiede eher wie sanfte Stupser wirken als wie strikte Befehle: Sie verschieben die Wahrscheinlichkeiten eines bestimmten Schicksals, ohne ihn unumkehrbar festzulegen. Bei Rindern, deren frühe Entwicklung der des Menschen näher kommt als der der Maus, deutet dies darauf hin, dass die Symmetriebrechung — kleine, ungleiche Verteilungen von Molekülen und Zellverhalten — früher beginnt, als sichtbare Strukturen vermuten lassen. Für die assistierte Reproduktion und Embryonenbiopsien sowohl bei Nutztieren als auch möglicherweise beim Menschen unterstreichen die Ergebnisse, dass nicht alle frühen Zellen austauschbar sind und dass das Untersuchen oder Entfernen dieser Zellen in diesen Stadien die ersten Zellschicksalsentscheidungen des Embryos subtil beeinflussen könnte.
Zitation: Koyama, H., Mashiko, D., Ferré-Pujol, P. et al. Early transcriptional divergence underlies cell fate bias in bovine embryos. Commun Biol 9, 625 (2026). https://doi.org/10.1038/s42003-026-10198-9
Schlüsselwörter: Entwicklung boviner Embryonen, Zellschicksals-Bias, Einzelzell-RNA-Sequenzierung, Trophektoderm-Linie, frühe Embryogenese