Clear Sky Science · fr
La divergence transcriptionnelle précoce sous-tend le biais des destinées cellulaires dans les embryons bovins
Comment les premiers choix de la vie peuvent façonner un veau
Chaque mammifère, y compris les humains et les bovins, commence la vie comme une seule cellule qui se divise à plusieurs reprises. Pendant des décennies, les biologistes ont supposé que les premières cellules de cette petite masse étaient toutes équivalentes, chacune ayant le même potentiel pour devenir n’importe quelle partie du futur organisme ou de ses tissus de soutien. Cette étude sur des embryons de vache remet en question cette image simpliste, montrant que certaines cellules commencent à basculer vers des avenirs particuliers bien avant qu’elles ne paraissent différentes au microscope.
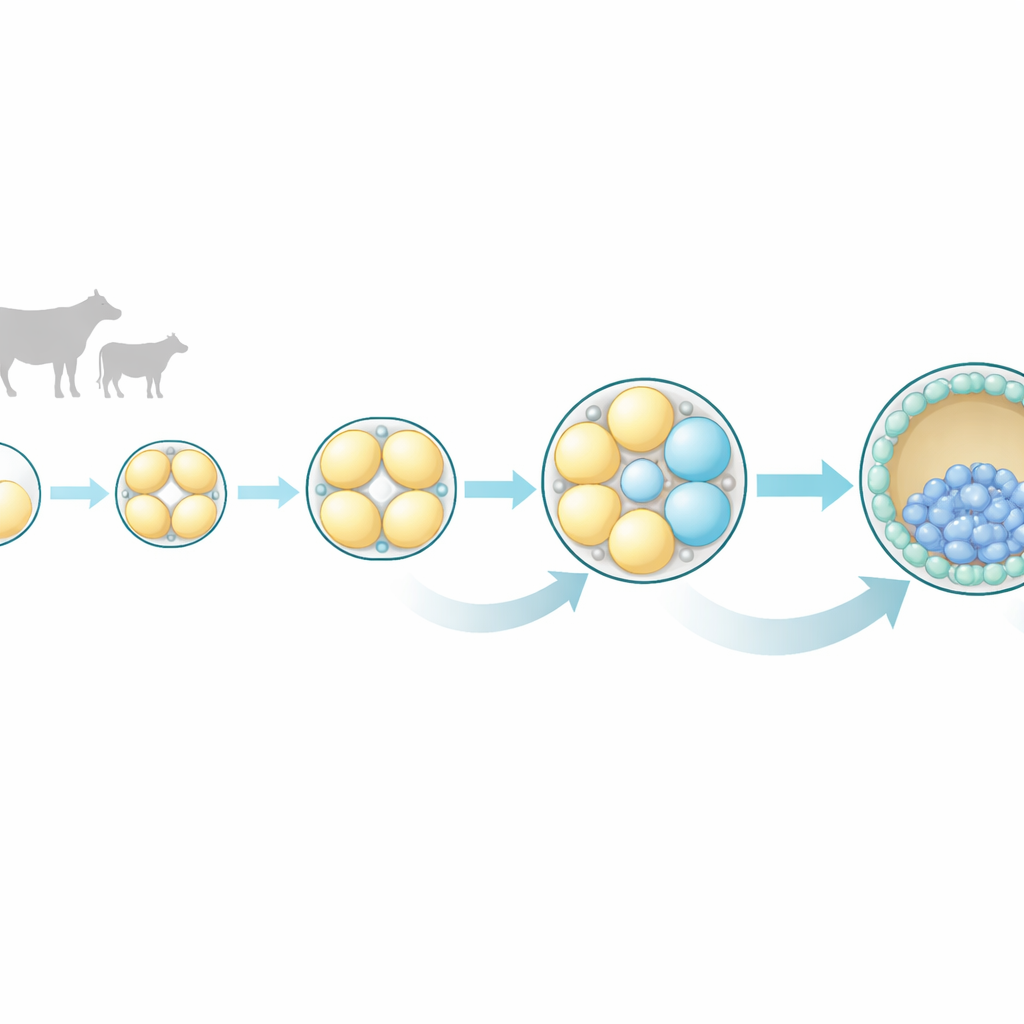
Les premières divisions cellulaires ne sont pas aussi égales qu’elles en ont l’air
Les chercheurs se sont concentrés sur les embryons bovins parce que leur développement précoce ressemble étroitement à celui des humains en termes de rythme et de schéma. Ils ont collecté des embryons à quatre stades très précoces : le zygote unicellulaire, puis les stades 2 cellules, 4 cellules et 8 cellules. Pour chaque embryon, ils ont séparé soigneusement toutes les cellules individuelles et mesuré les gènes actifs dans chacune à l’aide du séquençage ARN unicellulaire, une technique qui révèle la « liste de tâches » moléculaire d’une cellule. Cette approche leur a permis de comparer des cellules sœurs issues du même embryon et de mesurer à quel point elles étaient vraiment semblables ou différentes au fil du développement.
Des différences croissantes apparaissent aux stades 4 et 8 cellules
Au stade 2 cellules, les deux cellules sœurs présentaient une activité génique presque identique, soutenant la vision traditionnelle d’un potentiel égal à ce stade. Mais au stade 4 cellules, des différences subtiles ont commencé à émerger, et au stade 8 cellules ces différences sont devenues marquées. Les cellules d’un même embryon de 8 cellules ne se regroupaient plus selon leurs profils d’expression génique ; chacune suivait plutôt son propre chemin moléculaire. Beaucoup des gènes les plus variables étaient liés à des voies de communication intracellulaire, en particulier un ensemble connu sous le nom de MAPK, ainsi que des voies de signalisation Ras et Wnt associées. Ces voies sont déjà connues chez d’autres espèces pour guider la décision d’une cellule de faire partie de l’embryon proprement dit ou de la couche externe qui formera le placenta.
Indices de futurs rôles dans les couches externes versus internes
L’équipe a porté une attention particulière à un gène appelé CDX2, marqueur classique de la couche externe (trophectoderme) qui contribuera à la formation du placenta. Au stade 8 cellules, certaines cellules présentaient des niveaux de CDX2 plus élevés que leurs sœurs. Ces cellules à haute expression de CDX2 montraient également une activité renforcée des gènes liés à MAPK, et le lien entre CDX2 et ces gènes de signalisation s’est resserré du stade 4 au stade 8 cellules. Ce schéma suggère que, même avant que l’embryon ne se compacte en une boule lisse et ne positionne des cellules à l’extérieur ou à l’intérieur, certaines cellules sont déjà biaisées vers devenir partie de la couche externe formant le placenta.
La taille cellulaire incline la balance vers les tissus de soutien
De façon intrigante, des différences physiques entre les cellules reflétaient ces biais moléculaires. Au sein d’un même embryon, certains blastomères étaient plus grands que d’autres aux stades 4 et 8 cellules. Les cellules plus grandes avaient tendance à exprimer davantage de CDX2 et de gènes liés à MAPK. Elles présentaient également des quantités plus élevées d’une protéine appelée YAP dans leurs noyaux, un acteur connu de l’identité de la couche externe dans les premiers embryons. Lorsque les scientifiques ont suivi des cellules individuelles grandes ou petites en culture, les embryons issus de blastomères plus gros se compactionnaient plus tôt, effectuaient un tour de division supplémentaire avant la compaction, et formaient des cavités remplies de liquide de manière plus fiable et stable. Lorsqu’on a reconstitué des embryons uniquement à partir des plus grandes ou des plus petites cellules, ceux construits à partir des plus grandes se sont développés de façon plus robuste et ont produit davantage de cellules de la couche externe tout en conservant des cellules internes capables de former l’embryon.
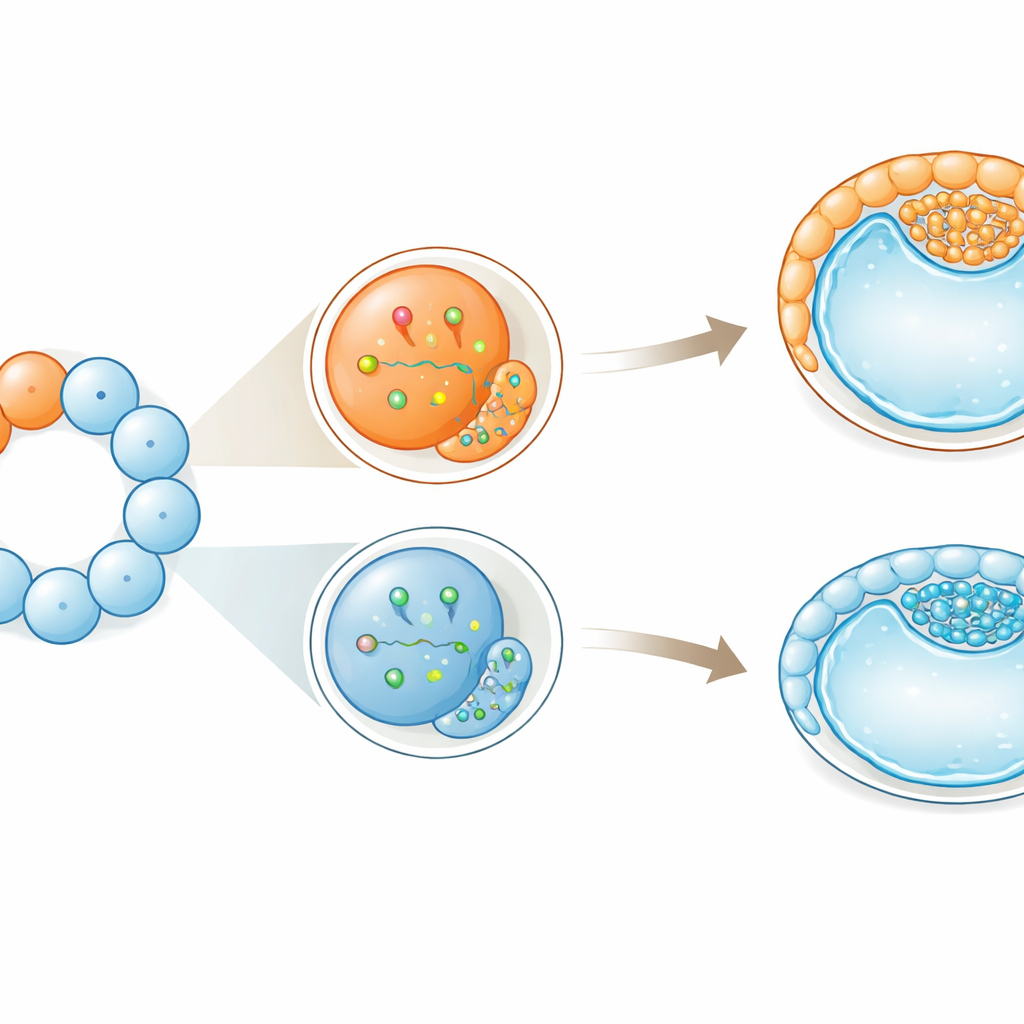
Un biais précoce sans perte de plasticité
Malgré ces inclinaisons précoces vers des rôles particuliers, les cellules ne perdaient pas leur plasticité de façon irréversible. Même les grandes cellules plus « prédisposées » à devenir externes pouvaient encore contribuer à la fois à l’embryon et aux tissus de soutien. Les auteurs proposent que ces différences précoces agissent comme des impulsions douces plutôt que comme des ordres stricts : elles biaisent les probabilités d’un destin donné sans l’enfermer. Chez le bovin, dont le développement précoce ressemble davantage à celui de l’humain qu’à celui de la souris, cela suggère que la rupture de symétrie — de petites distributions inégales de molécules et de comportements cellulaires — commence plus tôt que ne le laissent voir les structures visibles. Pour la reproduction assistée et la biopsie embryonnaire, tant en élevage que potentiellement chez l’humain, ces travaux soulignent que toutes les premières cellules ne sont pas interchangeables, et que les sonder ou les retirer à ces stades pourrait influencer subtilement la manière dont se déroulent les premières décisions de destinée cellulaire de l’embryon.
Citation: Koyama, H., Mashiko, D., Ferré-Pujol, P. et al. Early transcriptional divergence underlies cell fate bias in bovine embryos. Commun Biol 9, 625 (2026). https://doi.org/10.1038/s42003-026-10198-9
Mots-clés: développement des embryons bovins, biais du destin cellulaire, séquençage ARN unicellulaire, lignée du trophectoderme, embryogenèse précoce