Clear Sky Science · it
La prima divergenza trascrizionale sottostante il bias del destino cellulare negli embrioni bovini
Come le prime scelte della vita possono plasmare un vitello
Ogni mammifero, compresi gli esseri umani e il bestiame, inizia la vita come una singola cellula che si divide ripetutamente. Per decenni, i biologi hanno assunto che le cellule iniziali di questa piccola sfera fossero tutte uguali, ognuna con lo stesso potenziale di diventare qualsiasi parte del futuro corpo o dei suoi tessuti di supporto. Questo studio sugli embrioni di bovino mette in discussione quell'immagine semplificata, mostrando che alcune cellule iniziano a orientarsi verso futuri particolari molto prima di apparire diverse al microscopio.
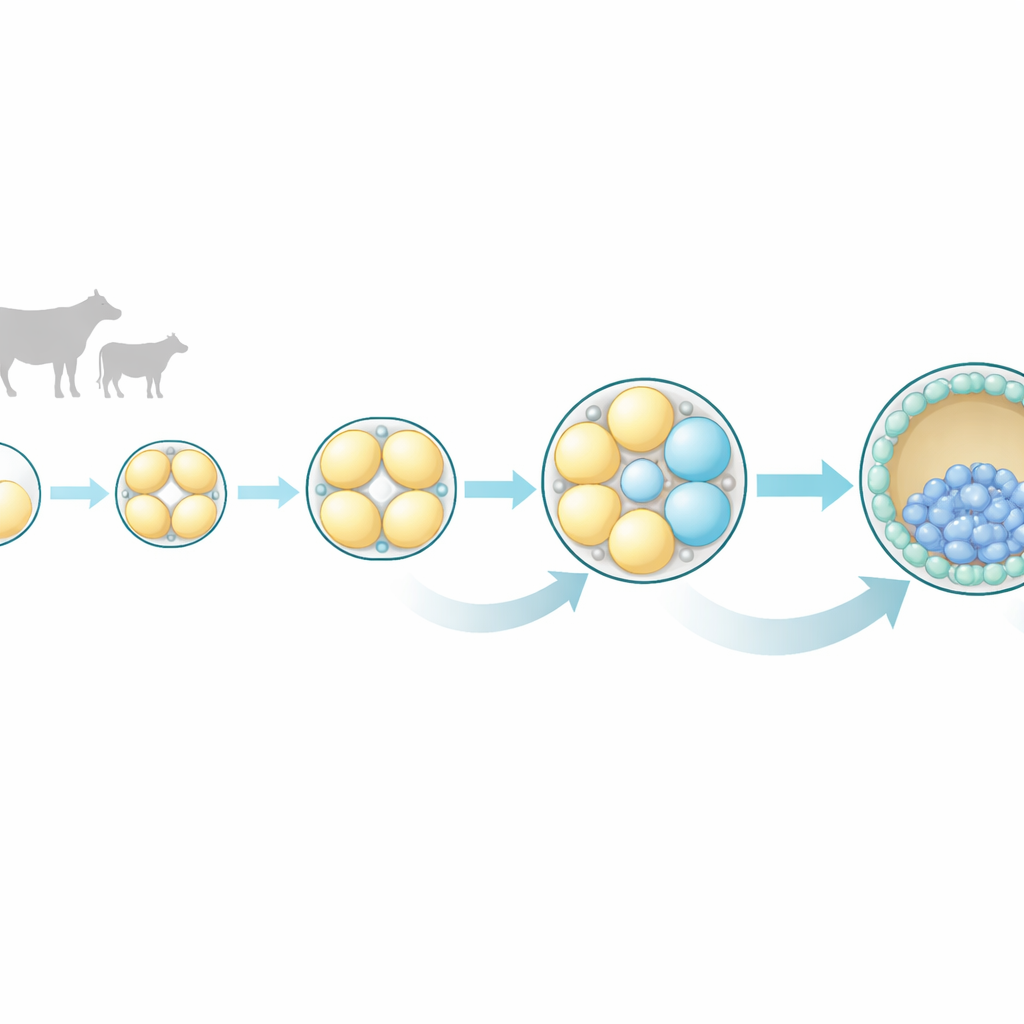
Le prime divisioni cellulari non sono così uguali come sembrano
I ricercatori si sono concentrati sugli embrioni bovini perché il loro sviluppo precoce somiglia molto a quello umano in termini di tempi e schemi. Hanno raccolto embrioni in quattro stadi molto precoci: lo zigote a cellula singola, e gli stadi a 2, 4 e 8 cellule. Da ciascun embrione hanno separato con cura tutte le singole cellule e hanno misurato quali geni erano attivi in ognuna utilizzando il sequenziamento dell'RNA a singola cellula, una tecnica che rivela la “lista delle cose da fare” molecolare di una cellula. Questo approccio ha permesso loro di confrontare cellule sorelle dello stesso embrione e di chiedersi quanto fossero realmente simili o diverse nel corso dello sviluppo.
Le differenze emergono già agli stadi a 4 e 8 cellule
Allo stadio a 2 cellule, le due cellule sorelle apparivano quasi identiche nella loro attività genica, sostenendo la visione tradizionale di potenziale uguale a questo punto. Ma allo stadio a 4 cellule iniziarono a comparire differenze sottili, e allo stadio a 8 cellule quelle differenze divennero marcate. Le cellule del medesimo embrione a 8 cellule non si raggruppavano più insieme in base ai profili di espressione genica; invece, ciascuna cellula seguiva il proprio percorso molecolare. Molti dei geni che variavano maggiormente erano collegati a vie di comunicazione intracellulari, in particolare un insieme noto come MAPK, insieme alle correlate vie di segnalazione Ras e Wnt. Queste vie sono già note in altre specie per guidare la decisione se una cellula diventerà parte dell'embrione vero e proprio o parte dello strato esterno che formerà la placenta.
Indizi di ruoli futuri negli strati esterni rispetto a quelli interni
Il team ha prestato particolare attenzione a un gene chiamato CDX2, un marcatore classico dello strato esterno (trofoblasto) che alla fine contribuirà a formare la placenta. Allo stadio a 8 cellule, alcune cellule avevano livelli di CDX2 più alti rispetto alle loro sorelle. Queste cellule con CDX2 elevato mostravano anche una maggiore attività dei geni correlati a MAPK, e il legame tra CDX2 e questi geni di segnalazione si è rafforzato dal 4-cellulare all'8-cellulare. Questo schema suggerisce che, prima ancora che l'embrione si compatti in una sfera liscia e posizioni le cellule all'esterno o all'interno, alcune cellule siano già sbilanciate verso il diventare parte dello strato esterno che forma la placenta.
La dimensione cellulare inclina la bilancia verso i tessuti di supporto
In modo intrigante, differenze fisiche tra le cellule corrispondevano a questi bias molecolari. All'interno dello stesso embrione, alcuni blastomeri erano più grandi di altri sia allo stadio a 4 cellule sia a quello a 8 cellule. Le cellule più grandi tendevano a esprimere più CDX2 e geni correlati alla via MAPK. Mostravano inoltre maggiori quantità di una proteina chiamata YAP nei loro nuclei, un noto promotore dell'identità dello strato esterno negli embrioni precoci. Quando gli scienziati hanno seguito singole cellule grandi o piccole in coltura, gli embrioni derivati da blastomeri più grandi si compattavano prima, effettuavano un giro extra di divisione prima della compattazione e formavano cavità piene di fluido in modo più affidabile e stabile. Quando embrioni ricostruiti sono stati creati interamente dalle cellule più grandi o più piccole, quelli costruiti con le cellule più grandi si sono sviluppati in modo più robusto e hanno prodotto più cellule dello strato esterno pur mantenendo le cellule interne che formano l'embrione.
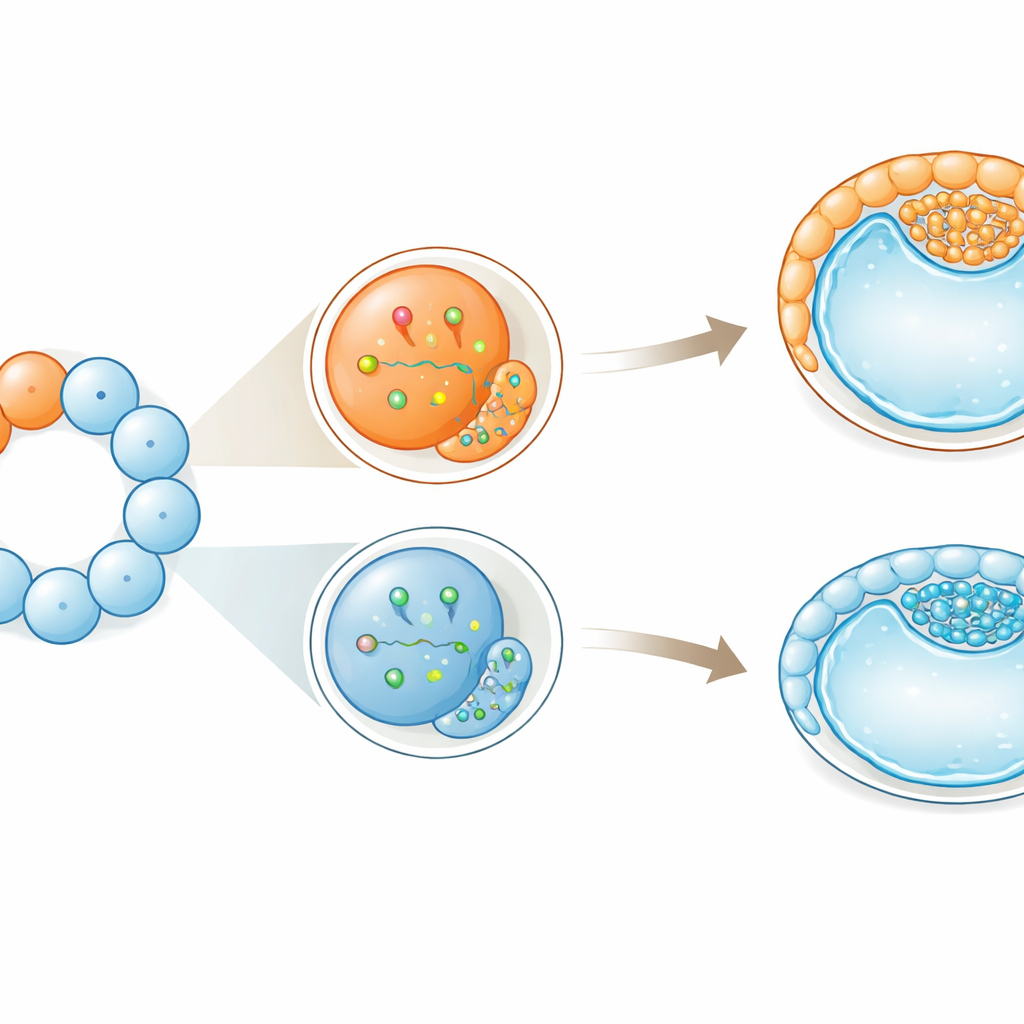
Bias precoci senza perdita di flessibilità
Nonostante questi primi orientamenti verso ruoli particolari, le cellule non perdevano però del tutto la loro flessibilità. Anche le cellule più “propense all'esterno” e di maggiore dimensione potevano ancora contribuire sia all'embrione sia ai tessuti di supporto. Gli autori propongono che queste prime differenze agiscano come spinte leggere piuttosto che come ordini rigidi: inclinano le probabilità di un dato destino senza imprimerlo definitivamente. Nel bovino, il cui sviluppo precoce somiglia più a quello umano che a quello del topo, ciò suggerisce che la rottura della simmetria — piccole distribuzioni non uguali di molecole e comportamenti cellulari — inizi prima di quanto rivelino le strutture visibili. Per la riproduzione assistita e la biopsia embrionale sia nel bestiame che, potenzialmente, negli esseri umani, il lavoro sottolinea che non tutte le prime cellule sono intercambiabili, e che sondare o rimuovere cellule in questi stadi potrebbe influenzare sottilmente come si svolgono le prime decisioni di destino cellulare dell'embrione.
Citazione: Koyama, H., Mashiko, D., Ferré-Pujol, P. et al. Early transcriptional divergence underlies cell fate bias in bovine embryos. Commun Biol 9, 625 (2026). https://doi.org/10.1038/s42003-026-10198-9
Parole chiave: sviluppo dell'embrione bovino, bias del destino cellulare, sequenziamento RNA a singola cellula, linea del trofoblasto, prima embriogenesi