Clear Sky Science · es
La divergencia transcripcional temprana subyace al sesgo de destino celular en embriones bovinos
Cómo las primeras decisiones de la vida pueden moldear un ternero
Cualquier mamífero, incluidos los humanos y el ganado vacuno, comienza la vida como una sola célula que se divide repetidamente. Durante décadas, los biólogos supusieron que las células más tempranas en esta pequeña esfera eran todas iguales, cada una con el mismo potencial para convertirse en cualquier parte del futuro cuerpo o de los tejidos de soporte. Este estudio sobre embriones de vaca cuestiona esa imagen simple, mostrando que algunas células empiezan a inclinarse hacia futuros particulares mucho antes de que se vean diferentes al microscopio.
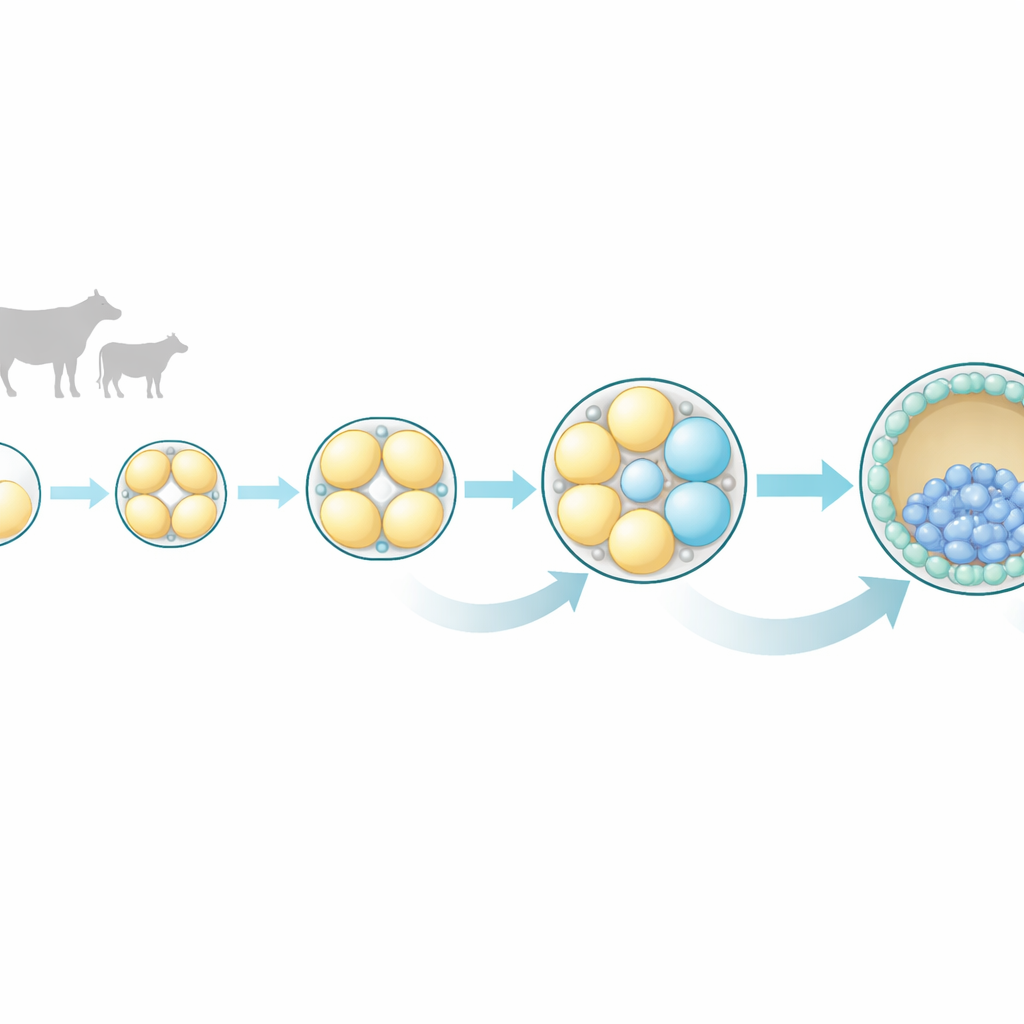
Las divisiones celulares tempranas no son tan iguales como parecen
Los investigadores se centraron en embriones bovinos porque su desarrollo temprano se asemeja al humano en tiempo y patrón. Recolectaron embriones en cuatro etapas muy tempranas: el cigoto de una sola célula, y las etapas de 2, 4 y 8 células. De cada embrión separaron cuidadosamente todas las células individuales y midieron qué genes estaban activos en cada una usando secuenciación de ARN de célula única, una técnica que revela la "lista de tareas" molecular de una célula. Este enfoque les permitió comparar células hermanas del mismo embrión y preguntar cuán similares o diferentes eran realmente a medida que avanzaba el desarrollo.
Las diferencias crecientes aparecen en las etapas de 4 y 8 células
En la etapa de 2 células, las dos células hermanas parecían casi idénticas en su actividad génica, lo que respalda la visión tradicional de potencial igual en ese momento. Pero en la etapa de 4 células empezaron a surgir diferencias sutiles, y en la de 8 células esas diferencias se volvieron notables. Las células del mismo embrión de 8 células ya no se agrupaban según sus perfiles de expresión génica; en cambio, cada célula seguía su propio camino molecular. Muchos de los genes que más variaban estaban vinculados a vías de comunicación intracelular, en especial un conjunto conocido como MAPK, junto con las vías de señalización Ras y Wnt relacionadas. Estas vías ya se conocen en otras especies por guiar si una célula forma parte del embrión propiamente dicho o de la capa externa que formará la placenta.
Pistas de roles futuros en capas celulares externas frente a internas
El equipo prestó atención especial a un gen llamado CDX2, un marcador clásico de la capa externa (trofectodermo) que finalmente ayudará a formar la placenta. En la etapa de 8 células, algunas células tenían niveles de CDX2 más altos que sus hermanas. Estas células con CDX2 alto también mostraron mayor actividad de genes relacionados con MAPK, y el vínculo entre CDX2 y estos genes de señalización se hizo más estrecho desde la etapa de 4 células hasta la de 8 células. Este patrón sugiere que, incluso antes de que el embrión se compacte en una esfera lisa y las células se posicionen en el exterior o el interior, algunas ya están sesgadas hacia convertirse en parte de la capa externa que formará la placenta.
El tamaño celular inclina la balanza hacia tejidos de soporte
De manera intrigante, las diferencias físicas entre células coincidieron con estos sesgos moleculares. Dentro del mismo embrión, algunos blastómeros eran más grandes que otros tanto en las etapas de 4 como de 8 células. Las células más grandes tendían a expresar más CDX2 y genes relacionados con MAPK. También mostraron mayores cantidades de una proteína llamada YAP en sus núcleos, un impulsor conocido de la identidad de la capa externa en embriones tempranos. Cuando los científicos siguieron en cultivo células individuales grandes o pequeñas, los embriones derivados de blastómeros grandes se compactaron antes, experimentaron una ronda adicional de división antes de compactarse y formaron cavidades llenas de fluido con mayor fiabilidad y estabilidad. Cuando se reconstruyeron embriones íntegramente a partir de las células más grandes o más pequeñas, los construidos con células grandes se desarrollaron de forma más robusta y produjeron más células de la capa externa mientras mantenían células internas formadoras del embrión.
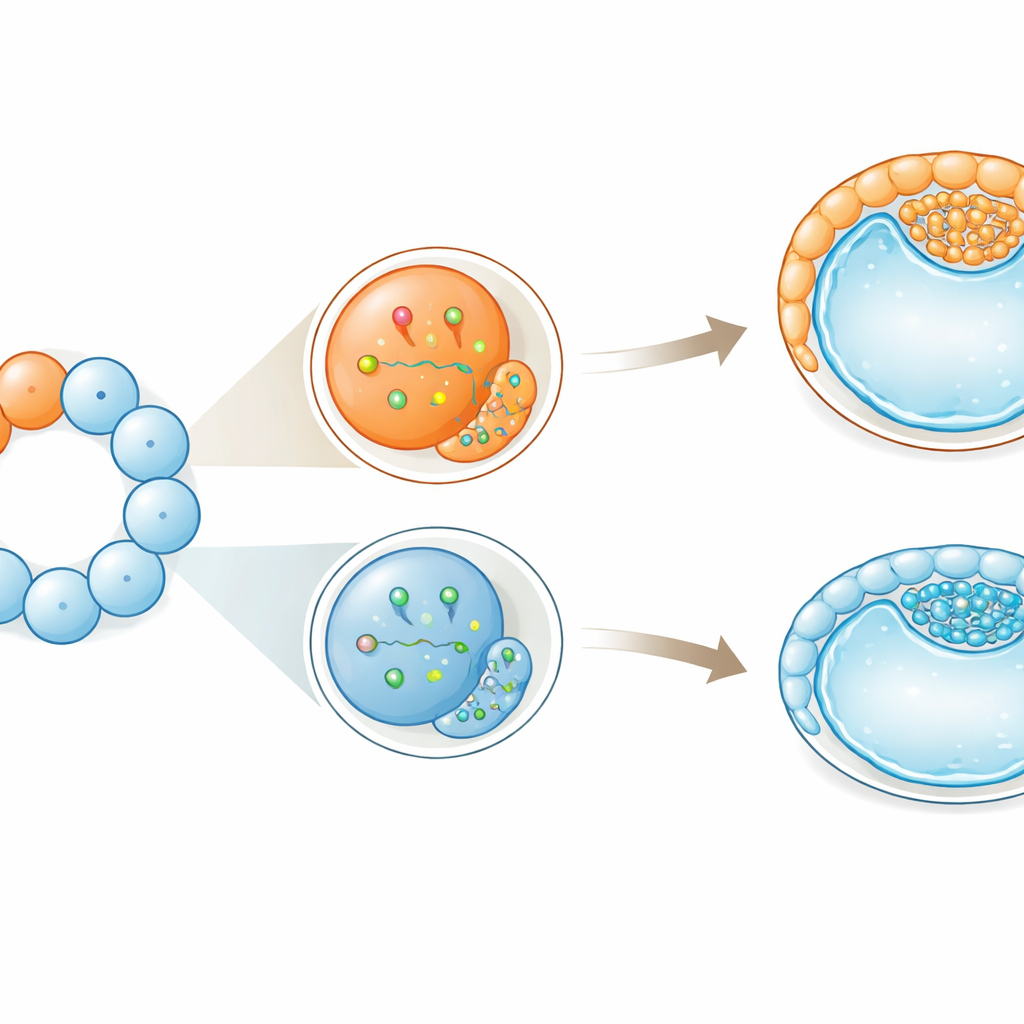
Sesgo temprano sin pérdida de flexibilidad
A pesar de estas inclinaciones tempranas hacia roles concretos, las células no perdieron su flexibilidad por completo. Incluso las células más "propensas a lo externo" podían contribuir tanto al embrión como a los tejidos de soporte. Los autores proponen que estas diferencias tempranas actúan como empujones suaves en lugar de órdenes estrictas: sesgan las probabilidades de un destino dado sin fijarlo de forma irreversible. En el ganado, cuyo desarrollo temprano se parece más al humano que al del ratón, esto sugiere que la ruptura de la simetría —distribuciones pequeñas y desiguales de moléculas y comportamientos celulares— comienza antes de lo que revelan las estructuras visibles. Para la reproducción asistida y la biopsia embrionaria, tanto en ganado como potencialmente en humanos, el trabajo subraya que no todas las células tempranas son intercambiables y que sondearlas o retirarlas en estas etapas podría influir sutilmente en cómo se desarrollan las primeras decisiones de destino celular del embrión.
Cita: Koyama, H., Mashiko, D., Ferré-Pujol, P. et al. Early transcriptional divergence underlies cell fate bias in bovine embryos. Commun Biol 9, 625 (2026). https://doi.org/10.1038/s42003-026-10198-9
Palabras clave: desarrollo del embrión bovino, sesgo de destino celular, secuenciación de ARN de célula única, linaje del trofectodermo, embriogénesis temprana