Clear Sky Science · nl
Vroege transcriptionele divergentie onderliggend aan celnoodzaakbias in boviene embryo's
Hoe de eerste keuzes van het leven een kalf kunnen vormen
Elk zoogdier, inclusief mensen en runderen, begint het leven als een enkele cel die zich herhaaldelijk deelt. Decennialang gingen biologen ervan uit dat de vroegste cellen in dit kleine bolletje allemaal gelijk waren, elk met hetzelfde potentieel om elk deel van het toekomstige lichaam of de ondersteunende weefsels te worden. Deze studie aan koeienembryo's daagt dat eenvoudige beeld uit en toont aan dat sommige cellen al veel eerder naar bepaalde toekomsten beginnen te neigen, nog voordat ze onder de microscoop anders ogen.
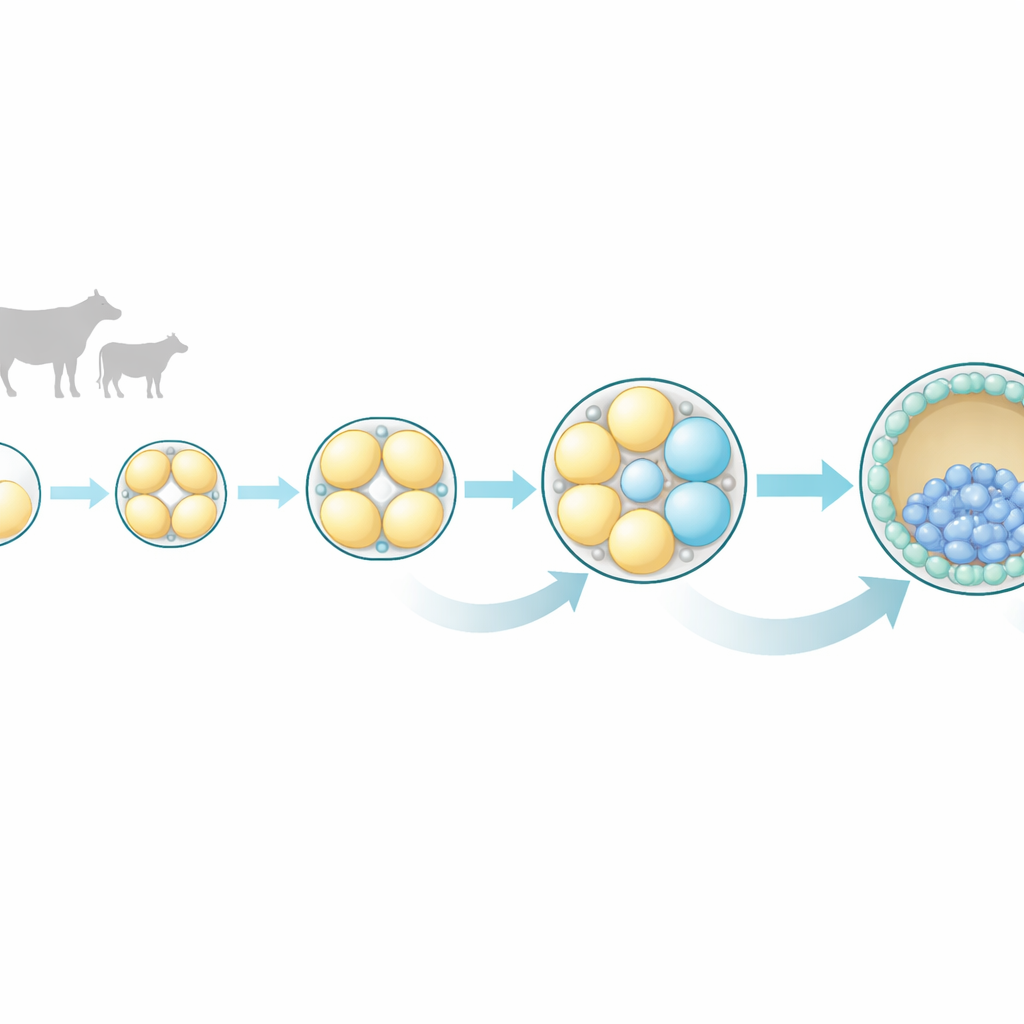
Vroege celdelingen zijn niet zo gelijk als ze lijken
De onderzoekers concentreerden zich op boviene embryo's omdat hun vroege ontwikkeling qua timing en patroon sterk lijkt op die van de mens. Ze verzamelden embryo's in vier zeer vroege stadia: de eencellige zygote en de 2-, 4- en 8-cellige stadia. Van elk embryo scheidden ze zorgvuldig alle individuele cellen en maten ze welke genen in elk van die cellen actief waren met single-cell RNA-sequencing, een techniek die de moleculaire "to‑do‑lijst" van een cel onthult. Deze aanpak stelde hen in staat zusterscellen uit hetzelfde embryo te vergelijken en te onderzoeken hoe gelijk of verschillend ze werkelijk waren naarmate de ontwikkeling vorderde.
Groeiverschillen verschijnen bij de 4- en 8-cellige stadia
In het 2-cellige stadium leken de twee zusterscellen vrijwel identiek in hun genactiviteit, wat de traditionele opvatting van gelijke potentie op dat moment ondersteunt. Maar in het 4-cellige stadium begonnen subtiele verschillen naar voren te komen, en in het 8-cellige stadium werden die verschillen opvallend. Cellen uit hetzelfde 8-cellige embryo groepeerden niet langer op basis van hun genexpressieprofielen; in plaats daarvan volgde elke cel zijn eigen moleculaire pad. Veel van de genen die het meest varieerden, waren gekoppeld aan communicatiepaden binnen cellen, vooral een set bekend als MAPK, samen met verwante Ras- en Wnt-signaleringsroutes. Deze paden zijn in andere soorten al bekend als richtlijnen voor of een cel deel wordt van het embryo zelf of van de buitenste laag die de placenta vormt.
Tekens van toekomstige rollen in buitenste versus binnenste cellagen
Het team besteedde bijzondere aandacht aan een gen dat CDX2 heet, een klassieke marker van de buitenste laag (trophectoderm) die uiteindelijk bijdraagt aan de vorming van de placenta. In het 8-cellige stadium hadden sommige cellen hogere CDX2-niveaus dan hun zusters. Deze CDX2-hoge cellen toonden ook sterkere activiteit van MAPK-gerelateerde genen, en de koppeling tussen CDX2 en deze signaalgenen werd sterker van het 4-cellige naar het 8-cellige stadium. Dit patroon suggereert dat, zelfs voordat het embryo compact wordt tot een glad bolletje en cellen binnen of buiten worden geplaatst, sommige cellen al een voorkeur hebben om deel van de buitenste, placenta-vormende laag te worden.
Celgrootte kantelt de balans richting ondersteunend weefsel
Intrigerend genoeg kwamen fysieke verschillen tussen cellen overeen met deze moleculaire vooringenomenheden. Binnen hetzelfde embryo waren sommige blastomeren zowel in het 4- als in het 8-cellige stadium groter dan andere. Grotere cellen neigden meer CDX2 en MAPK-gerelateerde genen te exprimeren. Ze vertoonden ook hogere hoeveelheden van een eiwit genaamd YAP in hun kernen, een bekende aanjager van buitenlaagidentiteit in vroege embryo's. Wanneer de wetenschappers enkele grote of kleine cellen in cultuur volgden, compacteerden embryo's die van grotere blastomeren afstamden eerder, ondergingen ze één extra delingsronde voordat ze compacter werden, en vormden ze betrouwbaarder en stabieler met vloeistof gevulde holtes. Wanneer gereconstrueerde embryo's volledig uit de grootste of kleinste cellen werden opgebouwd, ontwikkelden die gemaakt van grotere cellen zich steviger en produceerden ze meer buitenlaagcellen, terwijl ze toch binnenste, embryo-vormende cellen behielden.
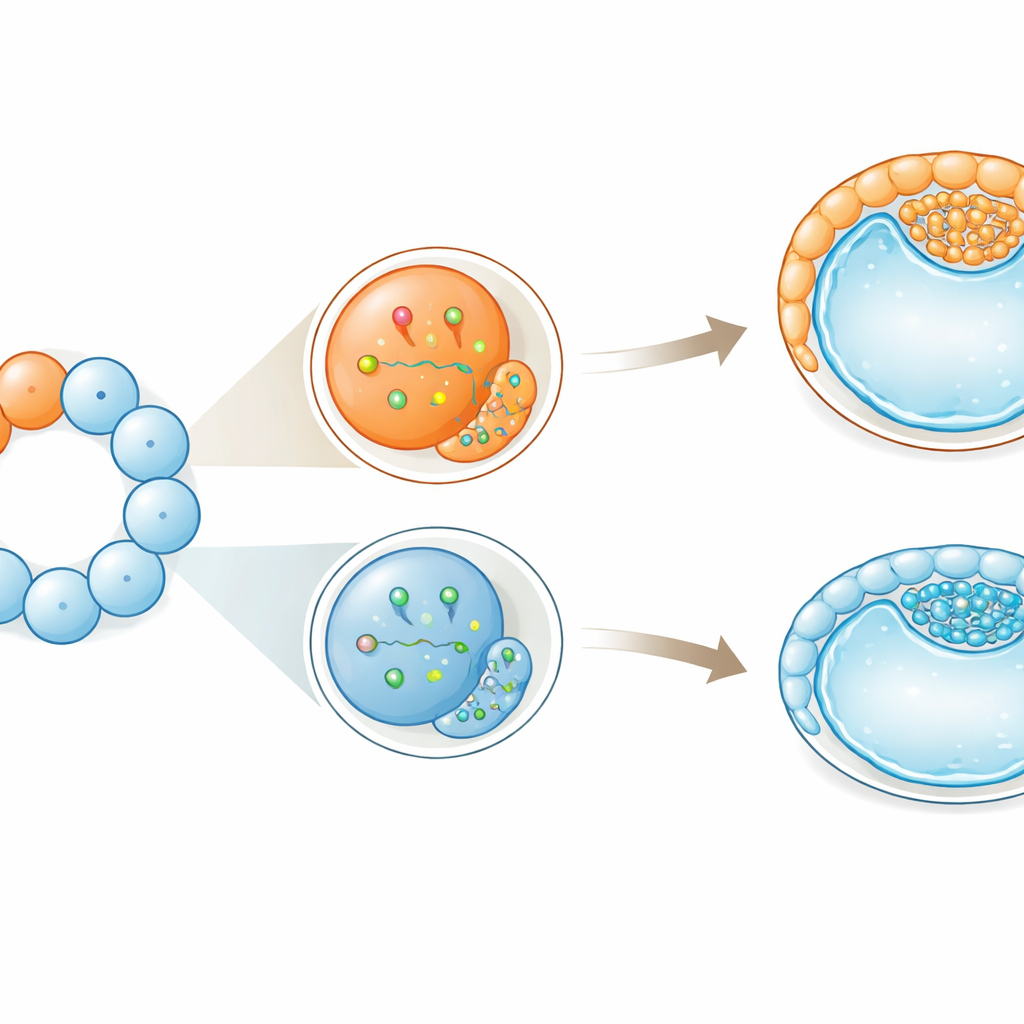
Vroege bias zonder verlies van flexibiliteit
Ondanks deze vroege neigingen naar bepaalde rollen verloren de cellen hun flexibiliteit niet volledig. Zelfs de meer "naar buiten neigende" grote cellen konden nog steeds bijdragen aan zowel het embryo als de ondersteunende weefsels. De auteurs stellen voor dat deze vroege verschillen werken als zachte duwtjes in plaats van strikte opdrachten: ze vertekenen de kansen op een bepaald lot zonder het onherroepelijk vast te leggen. Bij runderen, wiens vroege ontwikkeling meer op die van de mens lijkt dan op die van muizen, suggereert dit dat symmetriebreuk — kleine, ongelijke verdelingen van moleculen en celgedragingen — eerder begint dan zichtbaar wordt uit structuren. Voor kunstmatige voortplanting en embryobiopsie bij zowel vee als mogelijk mensen benadrukt het werk dat niet alle vroege cellen uitwisselbaar zijn, en dat het onderzoeken of verwijderen van deze cellen in deze stadia de eerste cel-lotbeslissingen van het embryo subtiel kan beïnvloeden.
Bronvermelding: Koyama, H., Mashiko, D., Ferré-Pujol, P. et al. Early transcriptional divergence underlies cell fate bias in bovine embryos. Commun Biol 9, 625 (2026). https://doi.org/10.1038/s42003-026-10198-9
Trefwoorden: ontwikkeling van boviene embryo's, celnoodzaakbias, single-cell RNA-sequencing, trophectodermlijn, vroege embryogenese