Clear Sky Science · pt
FAIMS de baixa resolução para maior cobertura de peptídeos em proteômica de baixa carga e de célula única
Ver Mais a Partir de Menos
A biologia moderna frequentemente trabalha com amostras incrivelmente pequenas—às vezes o conteúdo de uma única célula. Para entender o que acontece nesses mundos diminutos, os cientistas dependem de ferramentas capazes de detectar milhares de proteínas diferentes ao mesmo tempo. Este estudo mostra que, ao ajustar de forma sutil o modo de operação de uma dessas ferramentas, chamada FAIMS, os pesquisadores conseguem ver muito mais fragmentos proteicos a partir da mesma quantidade mínima de material, sem comprar novos instrumentos ou reescrever softwares.
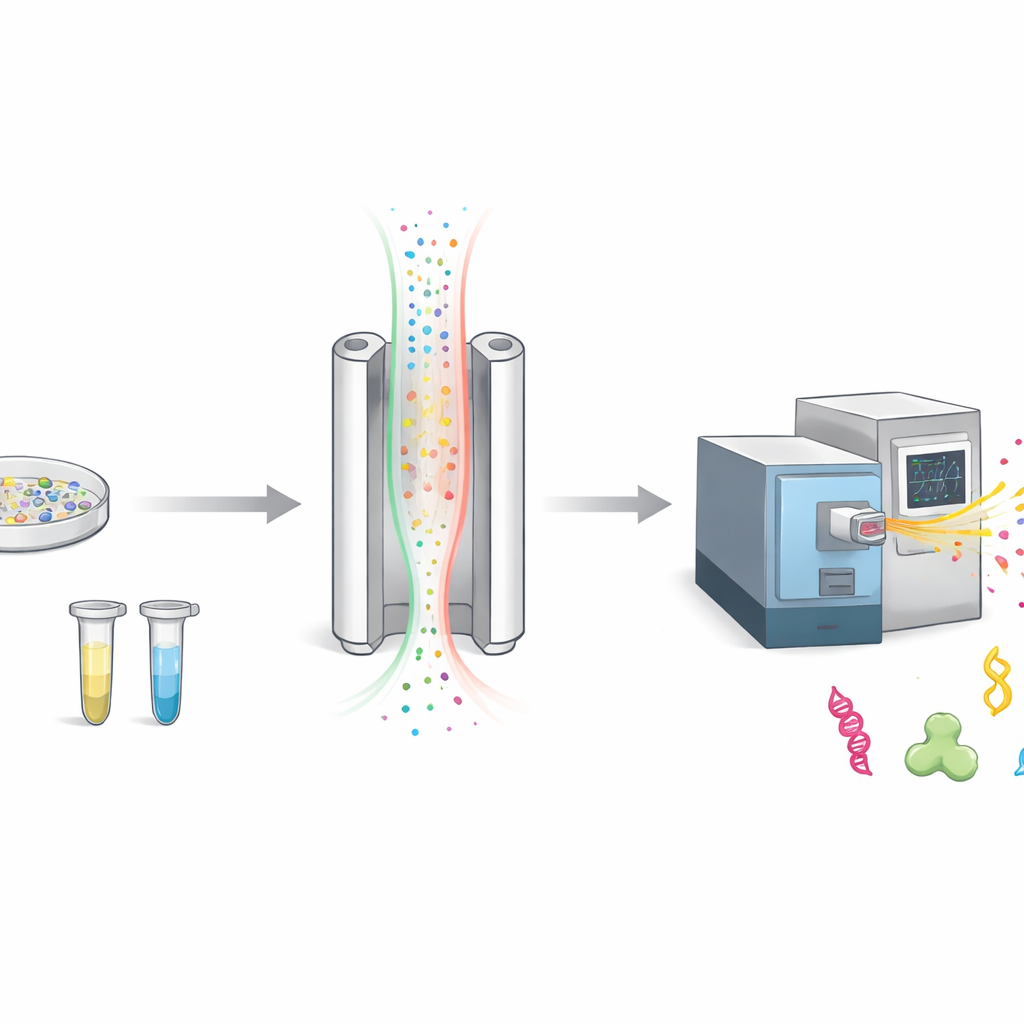
Como Classificamos Moléculas Carregadas no Ar
Quando os cientistas estudam proteínas, geralmente as fragmentam em pedaços menores chamados peptídeos e depois os pesam com um espectrômetro de massas. Antes da pesagem, o FAIMS adiciona uma etapa extra de separação. Ele faz com que moléculas carregadas atravessem uma fenda estreita entre duas placas metálicas enquanto um campo elétrico é alternado rapidamente. Apenas as moléculas cuja movimentação corresponde a um ajuste escolhido passam para o detector; o restante é descartado como ruído de fundo. Isso torna a medição mais limpa, mas também significa que muitas moléculas potencialmente interessantes nunca chegam ao instrumento.
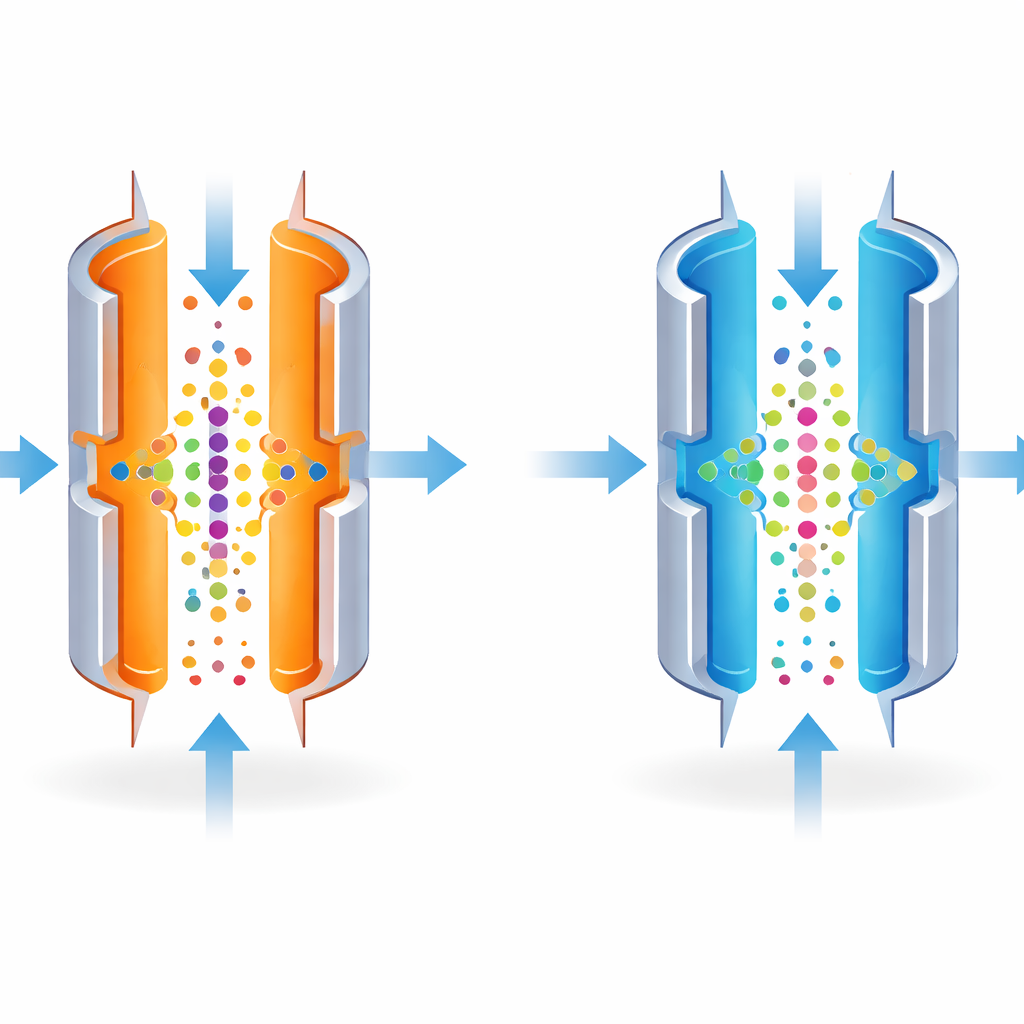
O Compromisso Entre Nitidez e Brilho
O FAIMS pode ser ajustado para separar moléculas com muita precisão, como uma lente de câmera focada em um único ponto. No entanto, as configurações mais nítidas deixam passar apenas uma faixa estreita de moléculas, reduzindo o sinal total. Os autores perceberam que a temperatura das placas metálicas afeta fortemente quão estreita essa faixa é. Resfriando a placa externa em relação à interna, eles tornaram a separação menos rigorosa de propósito. Isso alargou a gama de moléculas que podiam passar por um determinado ajuste, permitindo que mais íons alcançassem o espectrômetro de massas em uma única corrida.
Reduzindo a Temperatura para Revelar Peptídeos Ocultos
A equipe testou a ideia primeiro com misturas padrão de moléculas conhecidas e com quantidades muito pequenas de uma linha celular bem estudada (HeLa). Ao baixar a temperatura da placa externa de 100 °C para 80 °C, a janela de moléculas que passavam pelo FAIMS se expandiu e o número total de íons detectados aumentou. Em termos práticos, isso significou que o instrumento identificou 25–34% mais peptídeos distintos, e um aumento modesto no número de proteínas, a partir da mesma amostra diminuta. Esses ganhos foram maiores nas quantidades de amostra mais baixas, onde cada molécula detectada adicional tem mais importância.
Melhores Perspectivas Dentro de Células Individuais
Os pesquisadores então aplicaram o ajuste a amostras verdadeiramente de célula única de uma linha de câncer de pulmão chamada H460. Usar novamente a configuração mais suave do FAIMS aumentou tanto o número de peptídeos quanto o número de proteínas detectadas em cada célula. A sensibilidade extra melhorou as “impressões digitais” que descrevem a composição proteica de cada célula, tornando as diferenças entre células mais claras. Poços de controle que não continham células também produziram sinais, mas esses refletiam principalmente ruído de fundo e etapas de manuseio. A observação chave foi que simplesmente mudar a temperatura da placa alterou quantas proteínas significativas podiam ser vistas dentro de cada célula individual.
Um Ajuste Simples com Grande Retorno
No conjunto, o estudo mostra que diminuir deliberadamente a resolução do FAIMS—resfriando uma de suas placas—pode aumentar substancialmente quantos fragmentos proteicos são detectados a partir de amostras ultrapequenas, incluindo células únicas. Para não especialistas, a lição é que às vezes afrouxar um filtro permite ver mais do que é importante: aqui, uma separação ligeiramente mais borrada no FAIMS leva a uma imagem geral mais brilhante do panorama proteico da célula. Como essa mudança usa hardware existente e configurações simples, muitos laboratórios podem adotá-la rapidamente para aprofundar sua visão da biologia em escalas mínimas.
Citação: Hoch, D.G., Belford, M., Heil, L.R. et al. Low-resolution FAIMS for increased peptide coverage in low-load and single-cell proteomics. Sci Rep 16, 14454 (2026). https://doi.org/10.1038/s41598-026-45228-3
Palavras-chave: proteômica de célula única, FAIMS, espectrometria de massas, análise de proteínas, mobilidade iônica