Clear Sky Science · it
FAIMS a bassa risoluzione per aumentare la copertura peptidica nella proteomica a basso carico e a singola cellula
Vedere di più partendo da meno
La biologia moderna lavora spesso con campioni estremamente piccoli—talvolta il contenuto di una singola cellula. Per capire cosa accade in questi minuscoli mondi, gli scienziati si affidano a strumenti in grado di rilevare migliaia di proteine diverse contemporaneamente. Questo studio dimostra che, variando delicatamente il modo in cui si usa uno di questi strumenti, chiamato FAIMS, i ricercatori possono osservare molti più frammenti proteici dallo stesso ridotto quantitativo di materiale, senza acquistare nuovi strumenti o riscrivere software.
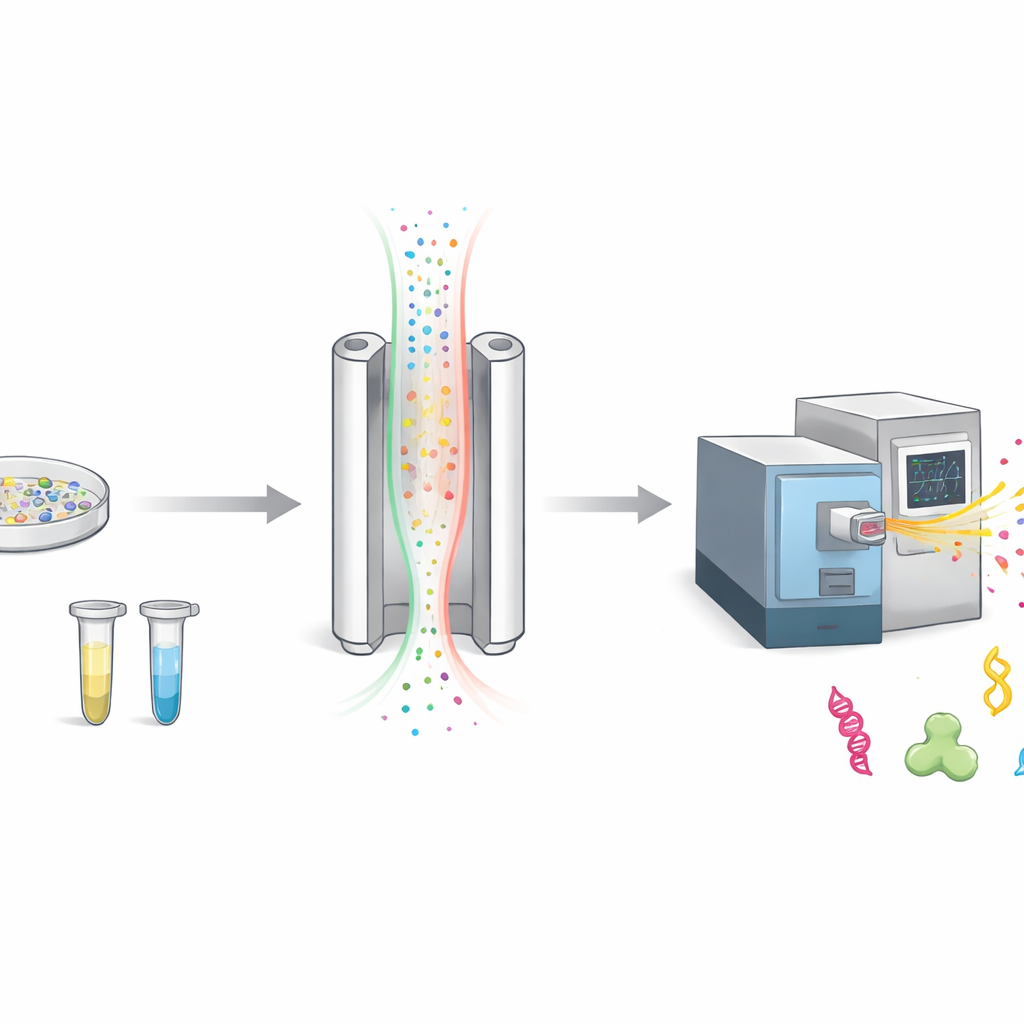
Come separiamo molecole cariche nell’aria
Quando gli scienziati studiano le proteine, di solito le tagliano in pezzi più piccoli chiamati peptidi e poi ne misurano la massa con uno spettrometro di massa. Prima della misura, FAIMS aggiunge un passaggio di separazione. Invia molecole cariche attraverso una fessura stretta tra due piastre metalliche mentre un campo elettrico viene rapidamente acceso e spento. Solo le molecole il cui moto corrisponde a un’impostazione scelta riescono a passare fino al rivelatore; le altre vengono scartate come rumore di fondo. Questo rende la misura più pulita, ma significa anche che molte molecole potenzialmente interessanti non raggiungono lo strumento.
Il compromesso tra nitidezza e luminosità
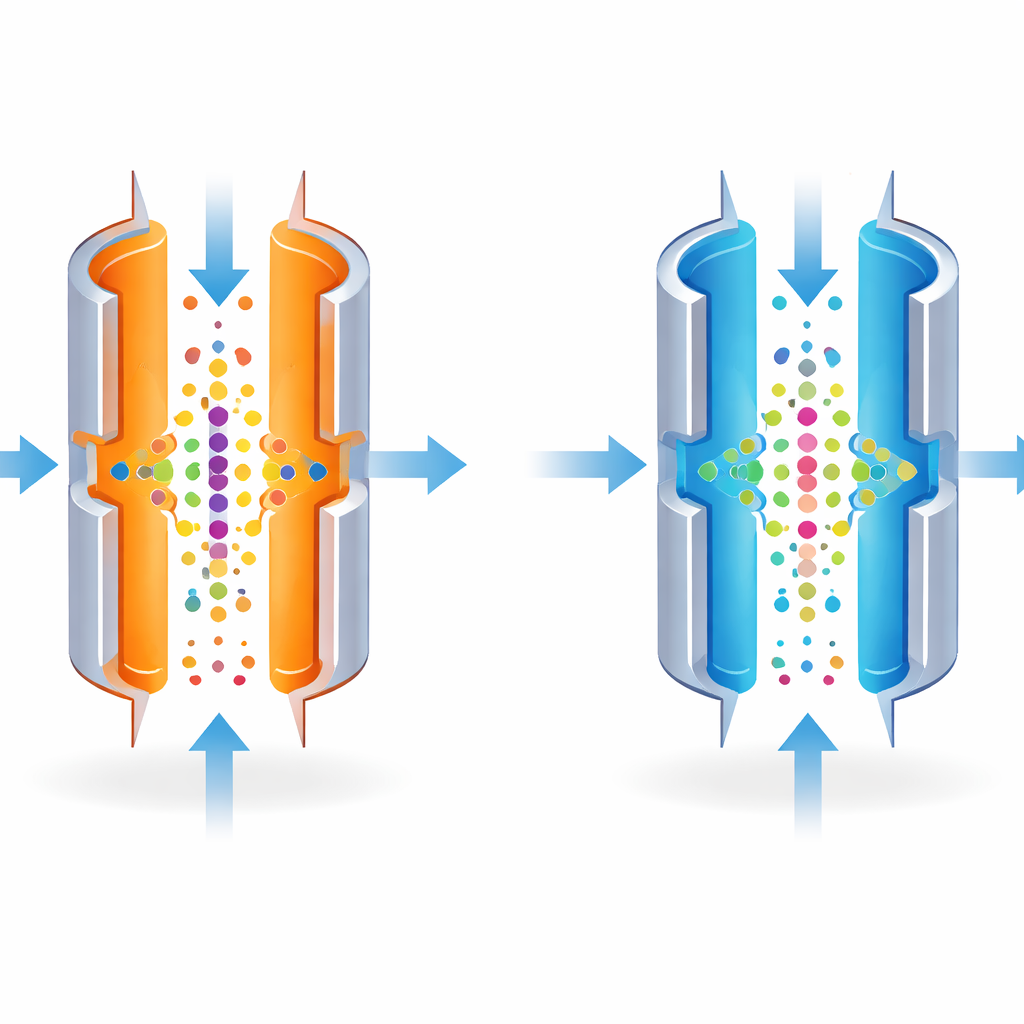
FAIMS può essere regolato per separare le molecole in modo molto preciso, come un obiettivo fotografico messo a fuoco su un singolo punto. Le impostazioni più nitide, però, lasciano passare solo una stretta fascia di molecole, attenuando il segnale complessivo. Gli autori hanno osservato che la temperatura delle piastre metalliche influenza fortemente quanto sia definita questa fascia. Raffreddando la piastra esterna rispetto a quella interna, hanno reso intenzionalmente la separazione meno severa. Ciò ha allargato l’intervallo di molecole che potevano oltrepassare a una data impostazione, permettendo a più ioni di raggiungere lo spettrometro di massa in una singola corsa.
Abbassare il calore per rivelare peptidi nascosti
Il gruppo ha prima testato l’idea con miscele standard di molecole note e con quantità molto ridotte di una linea cellulare ben studiata (HeLa). Abbassando la temperatura della piastra esterna da 100 °C a 80 °C si è ampliata la finestra di molecole che superavano il FAIMS e si è aumentato il numero totale di ioni rilevati. In termini pratici, lo strumento ha identificato il 25–34% in più di peptidi distinti, e un numero di proteine leggermente superiore, dallo stesso campione minimo. Questi guadagni sono stati più evidenti alle quantità di campione più basse, dove ogni molecola aggiuntiva rilevata conta di più.
Visioni migliori all’interno delle singole cellule
I ricercatori hanno quindi applicato il metodo a veri campioni di singole cellule provenienti da una linea di cancro polmonare chiamata H460. Anche in questo caso l’impostazione FAIMS più delicata ha aumentato sia il numero di peptidi sia il numero di proteine rilevate per cellula. La sensibilità aggiuntiva ha migliorato le “impronte” che descrivono il profilo proteico di ciascuna cellula, rendendo più evidenti le differenze tra cellule. Pozzetti di controllo senza cellule hanno prodotto segnali, ma questi riflettevano per lo più rumore di fondo e passaggi di manipolazione. L’osservazione chiave è che la semplice modifica della temperatura della piastra ha modificato quanti protein‑segnali significativi potevano essere visti all’interno di ogni singola cellula.
Una semplice regolazione con grande resa
Nel complesso, lo studio mostra che abbassare deliberatamente la risoluzione di FAIMS—raffreddando una delle sue piastre—può aumentare sostanzialmente il numero di frammenti proteici rilevati da campioni ultra‑piccoli, incluse singole cellule. Per i non specialisti, il messaggio è che a volte allentare un filtro permette di vedere di più di ciò che conta: qui, una separazione leggermente più sfocata in FAIMS conduce a un quadro complessivamente più luminoso del paesaggio proteico cellulare. Poiché questa modifica utilizza hardware esistente e impostazioni semplici, molti laboratori possono adottarla rapidamente per approfondire la loro visione della biologia alle scale più piccole.
Citazione: Hoch, D.G., Belford, M., Heil, L.R. et al. Low-resolution FAIMS for increased peptide coverage in low-load and single-cell proteomics. Sci Rep 16, 14454 (2026). https://doi.org/10.1038/s41598-026-45228-3
Parole chiave: proteomica a singola cellula, FAIMS, spettrometria di massa, analisi delle proteine, mobilità ionica