Clear Sky Science · pl
FAIMS o niskiej rozdzielczości dla zwiększenia pokrycia peptydów w proteomice przy niskim obciążeniu i analizie pojedynczych komórek
Widzieć więcej z mniejszej ilości
Współczesna biologii często pracuje z zanadto małymi próbkami — czasem z zawartością pojedynczej komórki. Aby zrozumieć, co dzieje się w tych mikroskopijnych światach, naukowcy polegają na narzędziach mogących jednocześnie wykrywać tysiące różnych białek. Badanie pokazuje, że przez delikatną zmianę trybu pracy jednego z takich narzędzi, zwanego FAIMS, badacze mogą zobaczyć znacznie więcej fragmentów białek z tej samej maleńkiej ilości materiału, bez kupowania nowych urządzeń czy przepisywania oprogramowania.
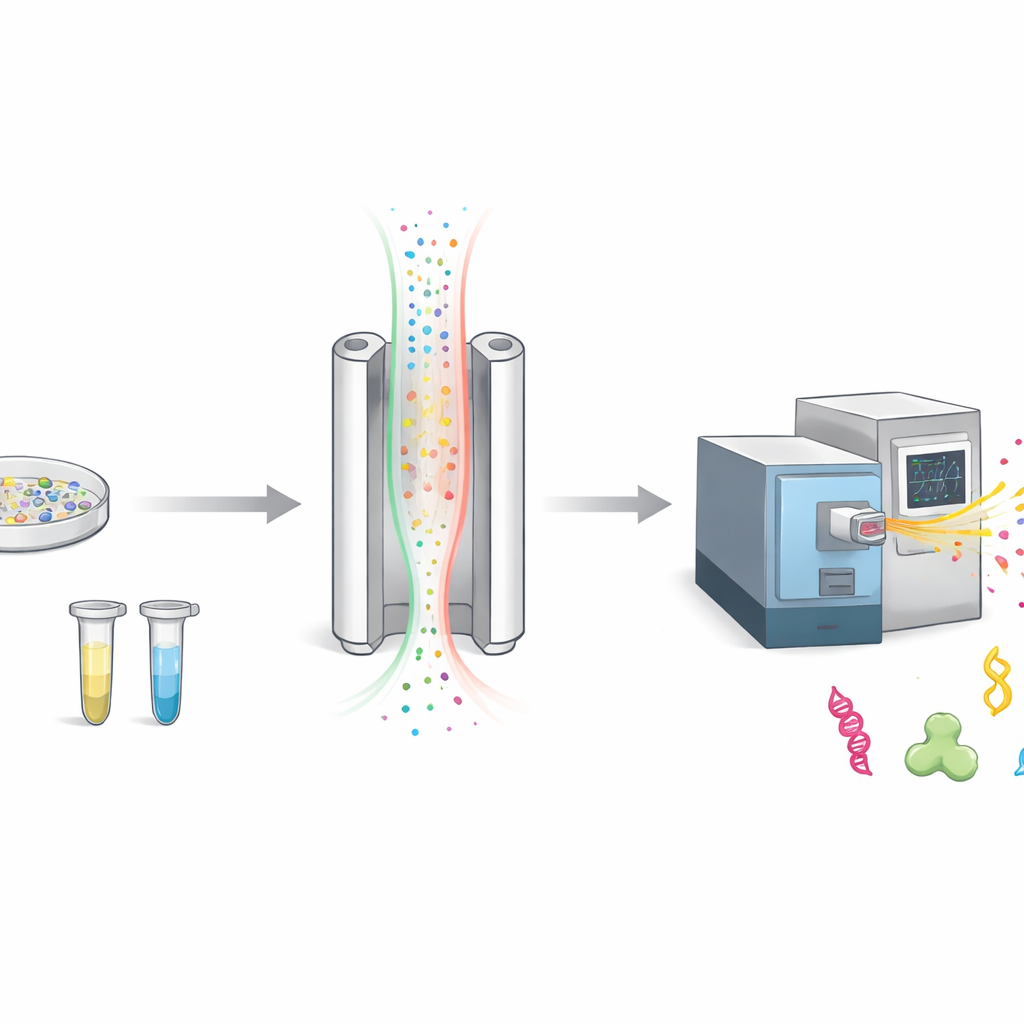
Jak sortujemy naładowane cząstki w powietrzu
Gdy naukowcy badają białka, zwykle rozbijają je na mniejsze kawałki zwane peptydami, a następnie ważą je za pomocą spektrometru mas. Przed ważeniem FAIMS dodaje dodatkowy etap sortowania. Wysyła naładowane cząstki przez wąską szczelinę pomiędzy dwiema metalowymi płytami, podczas gdy pole elektryczne szybko przełącza się między stanami. Tylko cząstki, których ruch odpowiada wybranemu ustawieniu, przechodzą do detektora; reszta jest odrzucana jako tło. To oczyszcza pomiar, ale oznacza też, że wiele potencjalnie interesujących cząstek nigdy nie dociera do instrumentu.
Kompomis między ostrością a jasnością
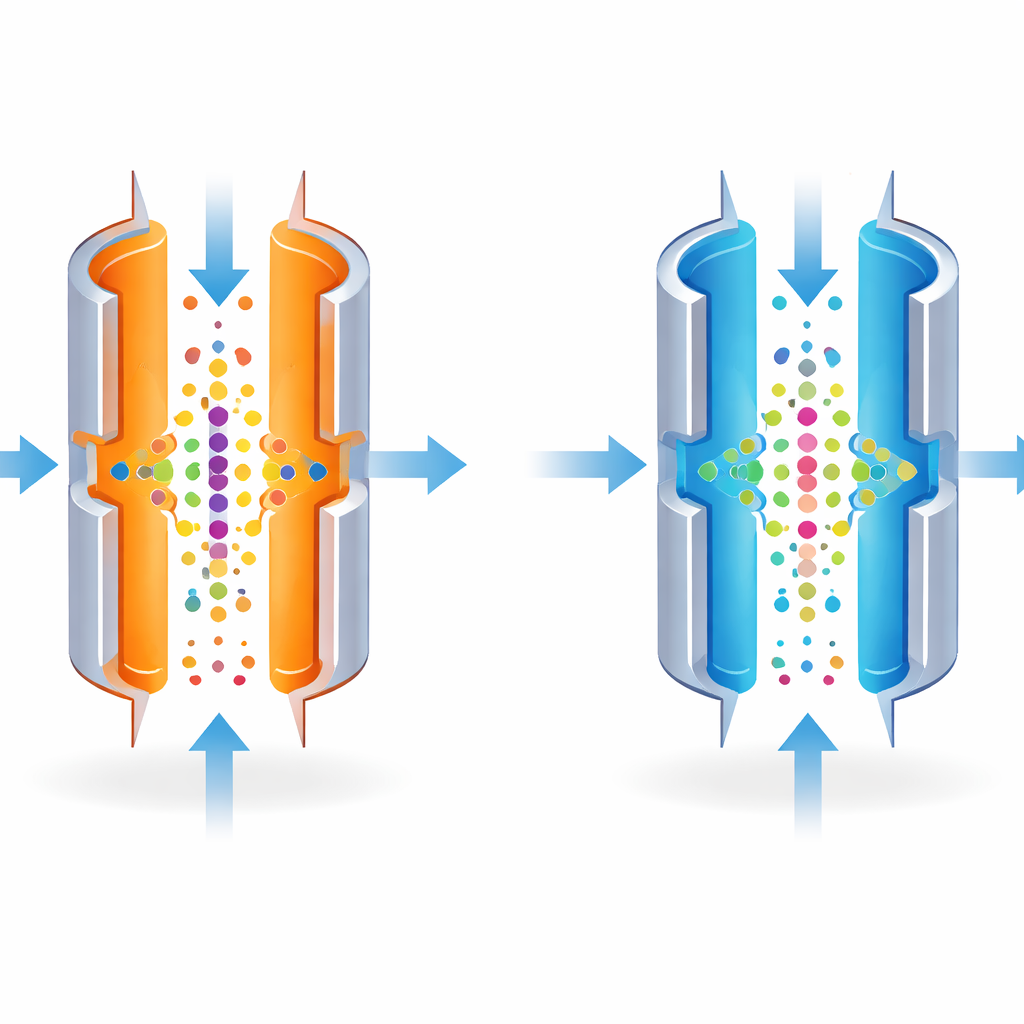
FAIMS można dostroić tak, by rozdzielał cząstki bardzo precyzyjnie, niczym obiektyw aparatu ustawiony na pojedynczy punkt. Najostrzejsze ustawienia przepuszczają jednak tylko wąski pas cząstek, przyciemniając ogólny sygnał. Autorzy zauważyli, że temperatura metalowych płyt mocno wpływa na to, jak ciasno zdefiniowany jest ten pas. Chłodząc zewnętrzną płytę w porównaniu z wewnętrzną, celowo osłabili rygor sortowania. Poszerzyło to zakres cząstek, które mogły przejść przy danym ustawieniu, pozwalając większej liczbie jonów dotrzeć do spektrometru mas w jednym przebiegu.
Obniżenie temperatury, aby odsłonić ukryte peptydy
Zespół najpierw przetestował pomysł na standardowych mieszankach znanych związków i przy bardzo małych ilościach dobrze zbadanej linii komórkowej (HeLa). Obniżenie temperatury zewnętrznej płyty z 100 °C do 80 °C rozszerzyło okno cząstek przepuszczanych przez FAIMS i zwiększyło całkowitą liczbę wykrytych jonów. W praktyce instrument zidentyfikował o 25–34% więcej odrębnych peptydów, a także nieco więcej białek, z tej samej drobnej próbki. Zyski te były największe przy najniższych ilościach materiału, gdzie każdy dodatkowo wykryty fragment ma największe znaczenie.
Lepsze spojrzenie wewnątrz pojedynczych komórek
Naukowcy zwrócili się następnie do prawdziwych próbek pojedynczych komórek z linii raka płuca H460. Stosowanie łagodniejszego ustawienia FAIMS ponownie zwiększyło zarówno liczbę peptydów, jak i białek wykrywanych w każdej komórce. Dodatkowa czułość poprawiła „odciski palców” opisujące skład białkowy każdej komórki, czyniąc różnice między komórkami bardziej wyraźnymi. Studzienki kontrolne bez komórek również generowały sygnały, ale w większości odzwierciedlały tło i etapy manipulacji. Kluczowa obserwacja była taka, że zwykła zmiana temperatury płyty przesunęła liczbę znaczących białek widocznych w każdej pojedynczej komórce.
Prosta zmiana o dużym zysku
Podsumowując, badanie pokazuje, że celowe obniżenie rozdzielczości FAIMS — przez schłodzenie jednej z jego płyt — może znacząco zwiększyć liczbę fragmentów białek wykrywanych w ultramałych próbkach, w tym pojedynczych komórkach. Dla osób spoza specjalności wniosek jest taki, że czasem poluzowanie filtra pozwala zobaczyć więcej tego, co istotne: tutaj nieco mniej ostra separacja w FAIMS daje jaśniejszy obraz białkowego krajobrazu komórki. Ponieważ zmiana ta wykorzystuje istniejący sprzęt i proste ustawienia, wiele laboratoriów może szybko ją przyjąć, by pogłębić swoje spojrzenie na biologię w najmniejszych skalach.
Cytowanie: Hoch, D.G., Belford, M., Heil, L.R. et al. Low-resolution FAIMS for increased peptide coverage in low-load and single-cell proteomics. Sci Rep 16, 14454 (2026). https://doi.org/10.1038/s41598-026-45228-3
Słowa kluczowe: proteomika pojedynczych komórek, FAIMS, spektrometria mas, analiza białek, mobilność jonów