Clear Sky Science · fr
FAIMS basse résolution pour augmenter la couverture peptidique en protéomique à faible charge et en protéomique unicellulaire
Voir plus à partir de moins
La biologie moderne travaille souvent avec des échantillons infinitésimaux — parfois le contenu d’une seule cellule. Pour comprendre ce qui se passe dans ces mondes minuscules, les scientifiques s’appuient sur des outils capables de détecter des milliers de protéines différentes simultanément. Cette étude montre qu’en modifiant légèrement le mode d’utilisation d’un de ces outils, appelé FAIMS, les chercheurs peuvent observer beaucoup plus de fragments protéiques à partir de la même quantité infime de matière, sans acheter de nouvel instrument ni réécrire de logiciels.
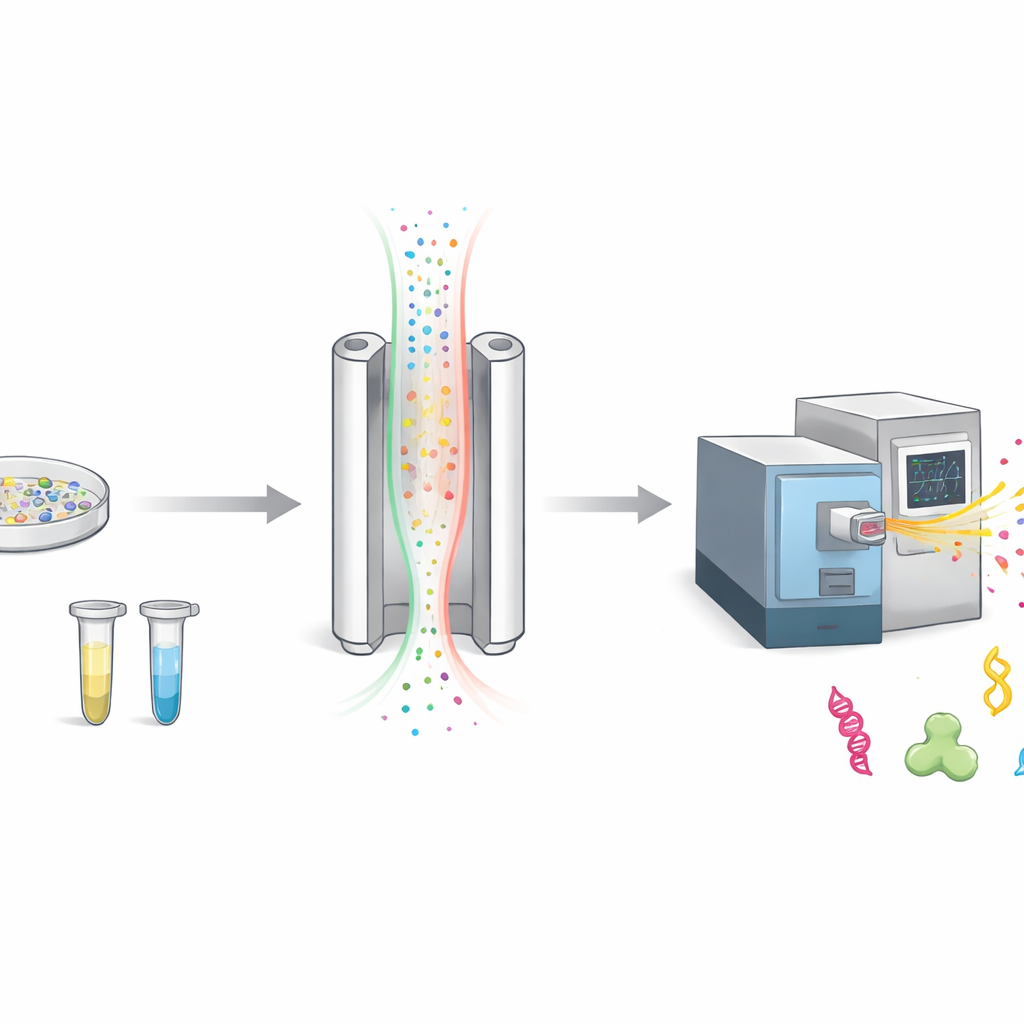
Comment nous trions les molécules chargées dans l’air
Quand les scientifiques étudient les protéines, ils les coupent généralement en morceaux plus petits appelés peptides, puis les pèsent avec une spectrométrie de masse. Avant la pesée, FAIMS ajoute une étape de tri supplémentaire. Il fait passer des molécules chargées à travers un espace étroit entre deux plaques métalliques tout en commutant rapidement un champ électrique. Seules les molécules dont le comportement correspond à un réglage choisi passent jusqu’au détecteur ; le reste est rejeté comme bruit de fond. Cela rend la mesure plus propre, mais signifie aussi que de nombreuses molécules potentiellement intéressantes n’atteignent jamais l’instrument.
Le compromis entre netteté et luminosité
FAIMS peut être ajusté pour séparer les molécules très précisément, comme un objectif de caméra focalisé sur un point unique. Les réglages les plus nets ne laissent cependant passer qu’une bande étroite de molécules, atténuant le signal global. Les auteurs ont constaté que la température des plaques métalliques influe fortement sur la largeur de cette bande. En refroidissant délibérément la plaque externe par rapport à la plaque interne, ils ont rendu le tri moins strict. Cela a élargi la plage de molécules pouvant passer à un réglage donné, permettant à davantage d’ions d’atteindre la spectrométrie de masse en une seule passe.
Baisser la température pour révéler des peptides cachés
L’équipe a d’abord testé l’idée avec des mélanges standards de molécules connues et avec de très petites quantités d’une lignée cellulaire bien étudiée (HeLa). Abaisser la température de la plaque externe de 100 °C à 80 °C a élargi la fenêtre de molécules passant à travers FAIMS et augmenté le nombre total d’ions détectés. En termes pratiques, cela signifiait que l’instrument identifiait 25–34 % de peptides distincts en plus, et un peu plus de protéines, à partir du même échantillon minime. Ces gains étaient les plus marqués aux plus faibles quantités d’échantillon, où chaque molécule détectée supplémentaire a le plus d’importance.
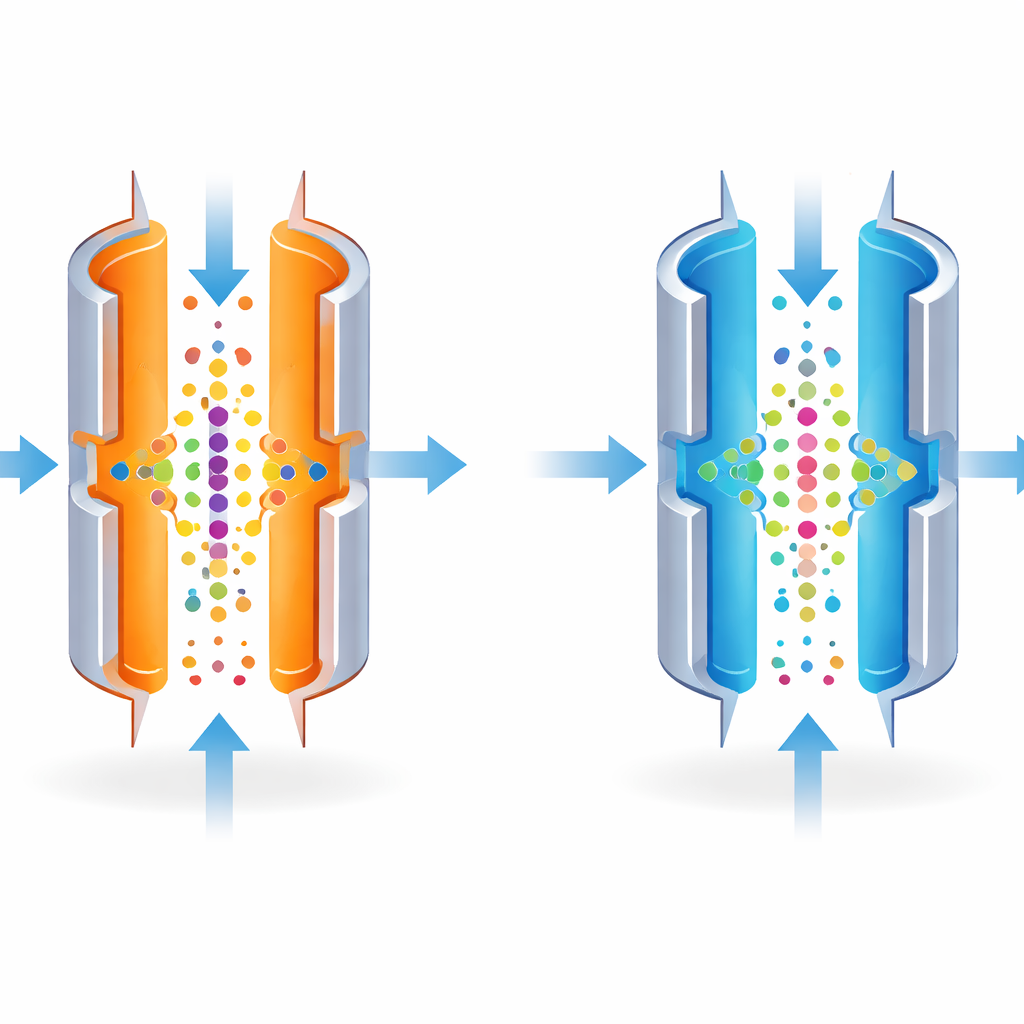
Meilleures vues à l’intérieur des cellules uniques
Les chercheurs sont ensuite passés à de véritables échantillons unicellulaires d’une lignée de cancer du poumon appelée H460. L’utilisation à nouveau d’un réglage FAIMS plus doux a augmenté à la fois le nombre de peptides et le nombre de protéines détectés dans chaque cellule. La sensibilité accrue a amélioré les « empreintes » décrivant la composition protéique de chaque cellule, rendant les différences entre cellules plus nettes. Les puits témoins ne contenant pas de cellules ont aussi produit des signaux, mais ceux-ci reflétaient principalement le bruit de fond et les étapes de manipulation. L’observation clé est que le simple changement de température d’une plaque modifiait le nombre de protéines significatives pouvant être observées dans chaque cellule individuelle.
Un ajustement simple avec un fort rendement
Dans l’ensemble, l’étude montre que réduire délibérément la résolution de FAIMS — en refroidissant l’une de ses plaques — peut augmenter sensiblement le nombre de fragments protéiques détectés à partir d’échantillons ultra‑petits, y compris des cellules uniques. Pour les non‑spécialistes, la leçon est que parfois desserrer un filtre permet de mieux voir l’essentiel : ici, une séparation légèrement plus floue dans FAIMS conduit à une image globale plus lumineuse du paysage protéique de la cellule. Comme ce changement utilise du matériel existant et des réglages simples, de nombreux laboratoires peuvent l’adopter rapidement pour approfondir leur regard sur la biologie aux plus petites échelles.
Citation: Hoch, D.G., Belford, M., Heil, L.R. et al. Low-resolution FAIMS for increased peptide coverage in low-load and single-cell proteomics. Sci Rep 16, 14454 (2026). https://doi.org/10.1038/s41598-026-45228-3
Mots-clés: protéomique unicellulaire, FAIMS, spectrométrie de masse, analyse des protéines, mobilité ionique