Clear Sky Science · ar
FAIMS منخفض الدقة لزيادة تغطية الببتيدات في بروتيوميات الأحمال المنخفضة والخلايا المفردة
رؤية أكثر من أقل
تعمل الأحياء الحديثة غالباً على عينات ضئيلة للغاية—أحياناً محتويات خلية واحدة فقط. لفهم ما يحدث داخل هذه العوالم الصغيرة، يعتمد العلماء على أدوات قادرة على اكتشاف آلاف البروتينات المختلفة في آن واحد. تُظهر هذه الدراسة أنه من خلال تغيير بسيط في طريقة تشغيل إحدى هذه الأدوات المسماة FAIMS، يمكن للباحثين رؤية المزيد من قطع البروتين من نفس الكمية الصغيرة من المادة، دون الحاجة لشراء أجهزة جديدة أو إعادة كتابة البرامج.
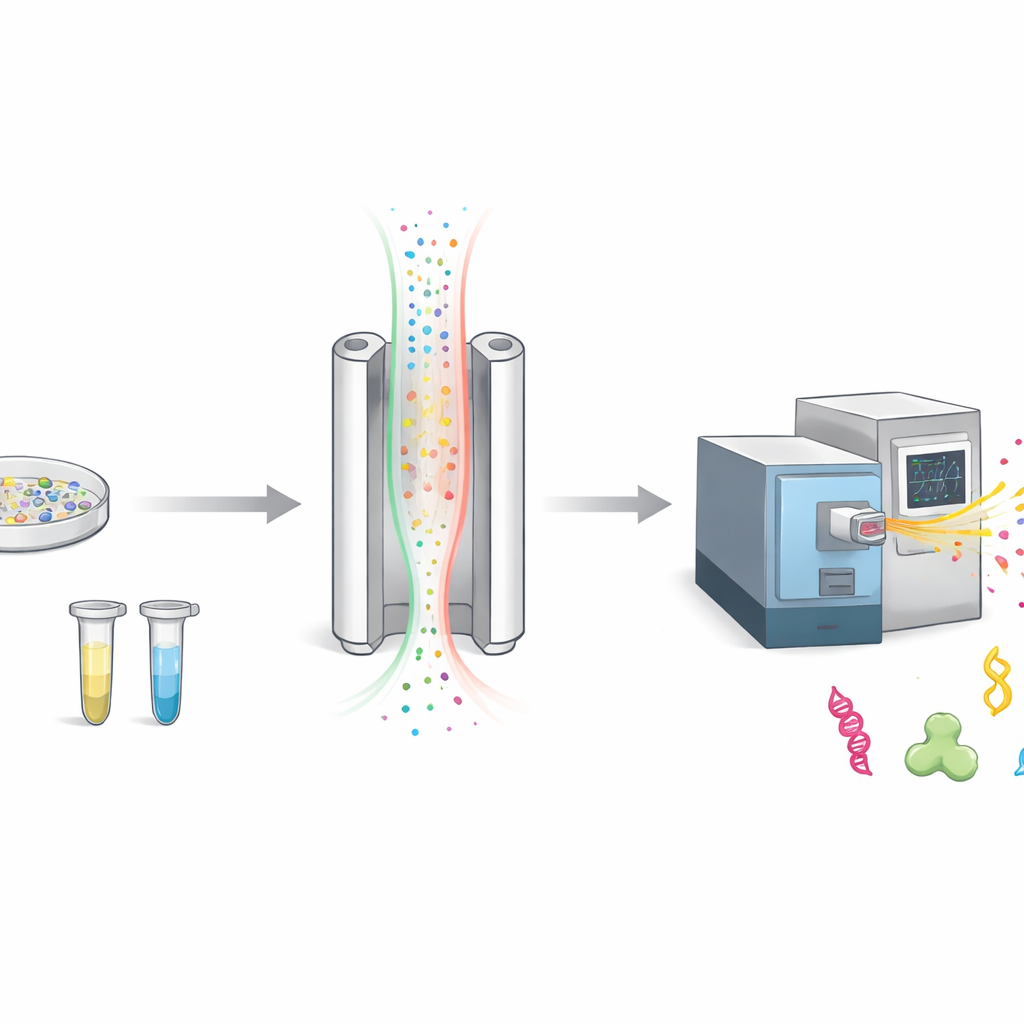
كيف نفرز الجزيئات المشحونة في الهواء
عندما يدرس العلماء البروتينات، فإنهم عادةً يجزئونها إلى قطع أصغر تسمى ببتيدات ثم يزنونها بمطياف الكتلة. قبل الوزن، تضيف FAIMS خطوة فرز إضافية. ترسل جزيئات مشحونة عبر فجوة ضيقة بين لوحين معدنيين بينما يبدّل مجال كهربائي بسرعة بين التشغيل والإيقاف. فقط الجزيئات التي تتطابق حركتها مع الإعداد المختار تنجح في المرور إلى الكاشف؛ والباقي يُستبعد كخلفية. هذا يجعل القياس أنظف، لكنه يعني أيضاً أن العديد من الجزيئات المثيرة للاهتمام قد لا تصل إلى الجهاز.
الموازنة بين الحدة والسطوع
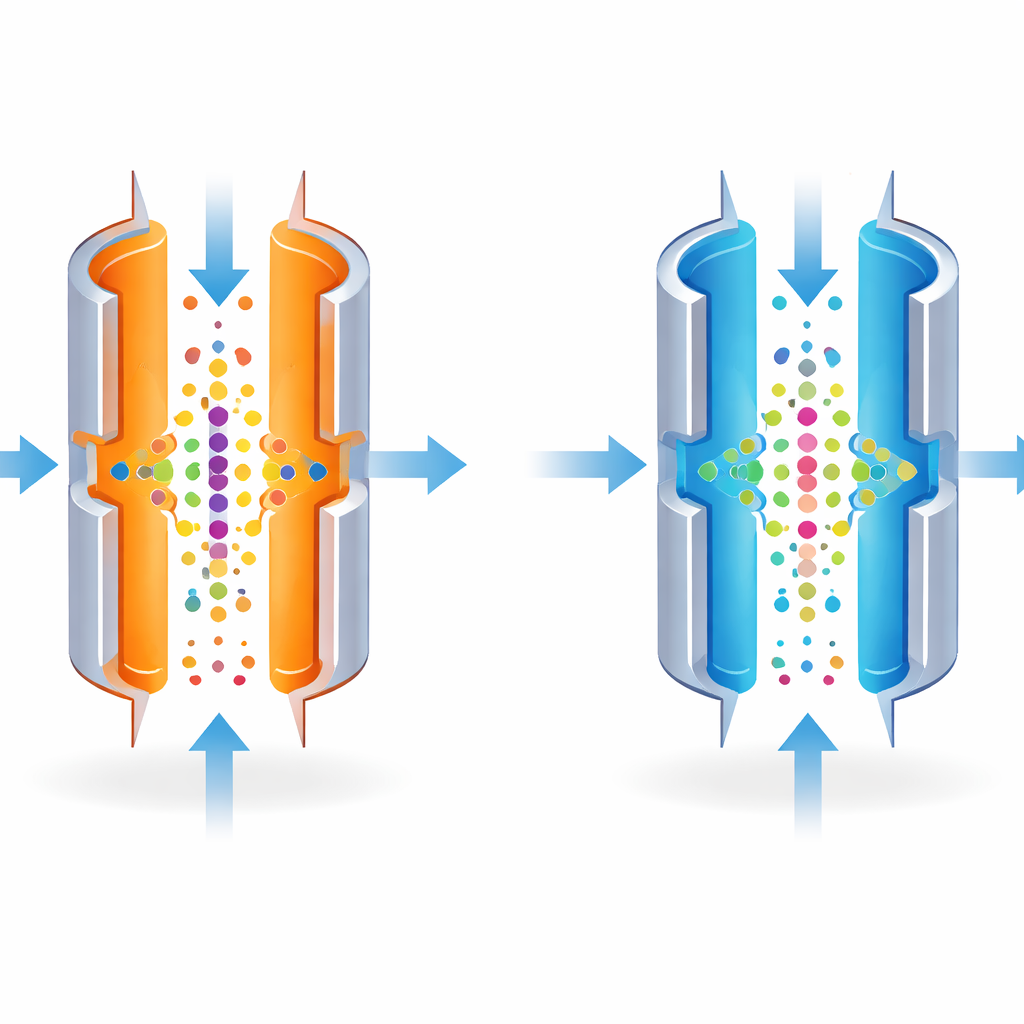
يمكن ضبط FAIMS للفصل بين الجزيئات بدقة، مثل عدسة كاميرا مركزة على نقطة واحدة. ومع ذلك، فإن الإعدادات الأشد حدة تسمح بمرور نطاق ضيق فقط من الجزيئات، مما يضعف الإشارة الإجمالية. لاحظ المؤلفون أن درجة حرارة الألواح المعدنية تؤثر بقوة على مدى ضيق هذا النطاق. من خلال تبريد اللوح الخارجي أكثر من اللوح الداخلي عمدًا إلى جعل الفرز أقل تشددًا. أدى ذلك إلى توسيع نطاق الجزيئات التي يمكنها المرور عند إعداد معين، مما أتاح وصول المزيد من الأيونات إلى مطياف الكتلة خلال تشغيل واحد.
خفض الحرارة لكشف ببتيدات مخفية
اختبر الفريق الفكرة أولاً باستخدام خلطات معيارية من جزيئات معروفة وبكميات صغيرة جدًا من خط خلوي معروف جيدًا (HeLa). إن خفض درجة حرارة اللوح الخارجي من 100 °م إلى 80 °م وسع نافذة الجزيئات التي مرت عبر FAIMS وزاد العدد الإجمالي للأيونات المكتشفة. عمليًا، تعني هذه الخطوة أن الجهاز حدّد 25–34% المزيد من الببتيدات المميزة، وعددًا متزايدًا بشكل متواضع من البروتينات، من نفس العينة الصغيرة. كانت هذه الزيادات الأكبر عند أدنى كميات العينة، حيث كل جزيء مكتشف إضافي له قيمة أكبر.
رؤى أفضل داخل الخلايا المفردة
ثم انتقل الباحثون إلى عينات خلية مفردة حقيقية من خط خلوي لسرطان الرئة يُدعى H460. أعاد استخدام إعداد FAIMS الألطف زيادة كل من عدد الببتيدات وعدد البروتينات المكتشفة في كل خلية. حسّنت الحساسية الإضافية «بصمات» التي تصف تكوين البروتين في كل خلية، مما جعل الفروقات بين الخلايا أوضح. كما أن الآبار الضابطة التي لم تحتوي على خلايا أنتجت إشارات، لكنها عكست في الغالب الخلفية وخطوات المعالجة. الملاحظة الأساسية كانت أن تغييرًا بسيطًا في درجة حرارة اللوح حوّل عدد البروتينات المفيدة التي يمكن رؤيتها داخل كل خلية مفردة.
تعديل بسيط بعائد كبير
بشكل عام، تُظهر الدراسة أن خفض دقة FAIMS عمدًا—عن طريق تبريد أحد ألواحها—يمكن أن يزيد بشكل ملحوظ عدد قطع البروتين المكتشفة من العينات الصغيرة للغاية، بما في ذلك الخلايا المفردة. للاختصاصيين غير المتخصصين، الخلاصة أن تخفيف فلتر ما أحيانًا يسمح برؤية ما يهم أكثر: هنا، فصل أهون قليلاً في FAIMS يؤدي إلى صورة إجمالية أكثر إشراقًا لمشهد البروتين داخل الخلية. وبما أن هذا التغيير يستخدم أجهزة حالية وإعدادات مباشرة، فيمكن للعديد من المختبرات اعتماده بسرعة لتعميق رؤيتها إلى الأحياء على أصغر المستويات.
الاستشهاد: Hoch, D.G., Belford, M., Heil, L.R. et al. Low-resolution FAIMS for increased peptide coverage in low-load and single-cell proteomics. Sci Rep 16, 14454 (2026). https://doi.org/10.1038/s41598-026-45228-3
الكلمات المفتاحية: بروتيوميات الخلية المفردة, FAIMS, مطيافية الكتلة, تحليل البروتين, تنقل الأيونات