Clear Sky Science · he
FAIMS ברזולוציה נמוכה להגברת כיסוי הפפטידים בפרוטאומיקה בעומס נמוך ותא יחיד
לראות יותר מתוך פחות
בביולוגיה המודרנית עובדים לעתים עם דגימות זעירות—לפעמים עם תוכנו של תא יחיד. כדי להבין מה מתרחש בעולמות הקטנים האלה, מדענים מסתמכים על כלים שיכולים לזהות אלפי חלבונים שונים בבת אחת. המחקר הזה מראה שברקיון שינוי עדין באופן ההפעלה של כלי אחד כזה, שנקרא FAIMS, החוקרים יכולים לגלות הרבה יותר חתיכות חלבון מאותו כמות זעירה של חומר, בלי לקנות מכשירים חדשים או לשכתב תוכנה.
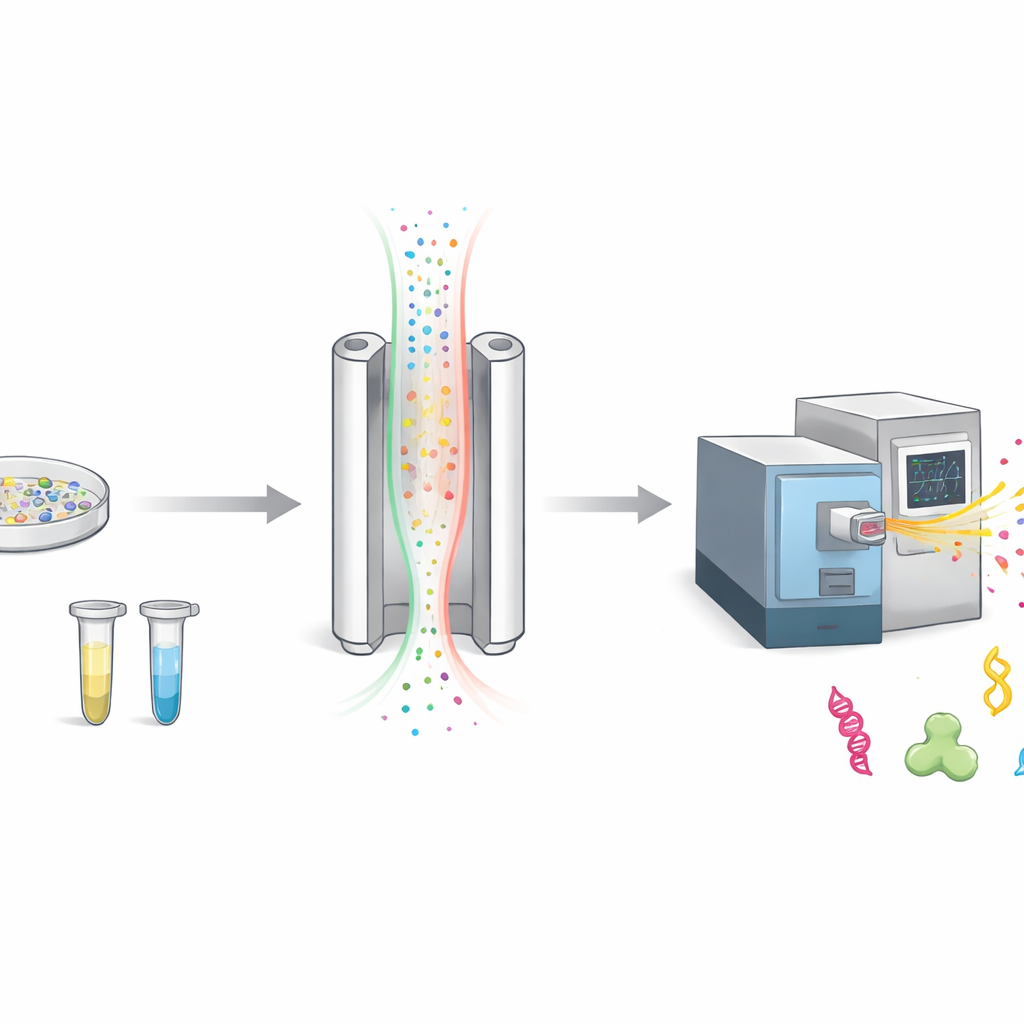
איך אנו ממיינים מולקולות טעונות באוויר
כשמדענים חוקרים חלבונים, הם לרוב חותכים אותם לחתיכות קטנות יותר הנקראות פפטידים ואז שוקלים אותם באמצעות ספקטרומטר מסה. לפני המדידה, FAIMS מוסיפה שלב נוסף של מיון. הוא שולח מולקולות טעונות דרך רווח צר בין שתי צלחות מתכת בעוד שדה חשמלי מתחלף במהירות בין מצב דולק וכבוי. רק מולקולות שהתנועה שלהן מתאימה להגדרה שנבחרה מעבירות ונכנסות לגלאי; השאר נדחות כרעש רקע. זה מנקה את המדידה, אבל גם אומר שמולקולות מעניינות רבות עשויות אף פעם לא להגיע למכשיר.
הפשרה בין חדות לעוצמה
ניתן להגדיר את FAIMS כך שיבדיל מולקולות במדויק גבוה, כמו עדשת מצלמה ממוקדת על נקודה יחידה. עם זאת, ההגדרות החדות ביותר מעבירות רק פס צר של מולקולות, וכך מעמעמות את האות הכולל. המחברים שם לב שטמפרטורת הצלחות המתכת משפיעה במידה רבה על כמה באופן מחמירה הפס מוגדר. על ידי קירור הצלחת החיצונית ביחס לפנימית, הם הפכו בכוונה את המיון לפחות קשוח. זה הרחיב את הטווח של מולקולות שיכלו לעבור באותה הגדרה, ואיפשר ליותר יונים להגיע לספקטרומטר המסה בהרצה אחת.
הפחתת החום כדי לחשוף פפטידים נסתרים
הקבוצה בחנה תחילה את הרעיון עם תערובות סטנדרטיות של מולקולות ידועות ועם כמויות קטנות מאוד של קו תאים שנחקר רבות (HeLa). הורדת טמפרטורת הצלחת החיצונית מ-100 °C ל-80 °C הרחיבה את חלון המולקולות שעברו דרך FAIMS והגדילה את מספר היונים שנתגלו בסך הכל. במונחים מעשיים, המשמעות הייתה שהמכשיר זיהה 25–34% יותר פפטידים מובחנים, וכמות ממעטת יותר של חלבונים, מאותה דגימה זעירה. השיפורים הללו היו הגדולים ביותר בעומסי הדגימה הנמוכים ביותר, שם כל מולקולה נוספת שזוהתה חשובה במיוחד.
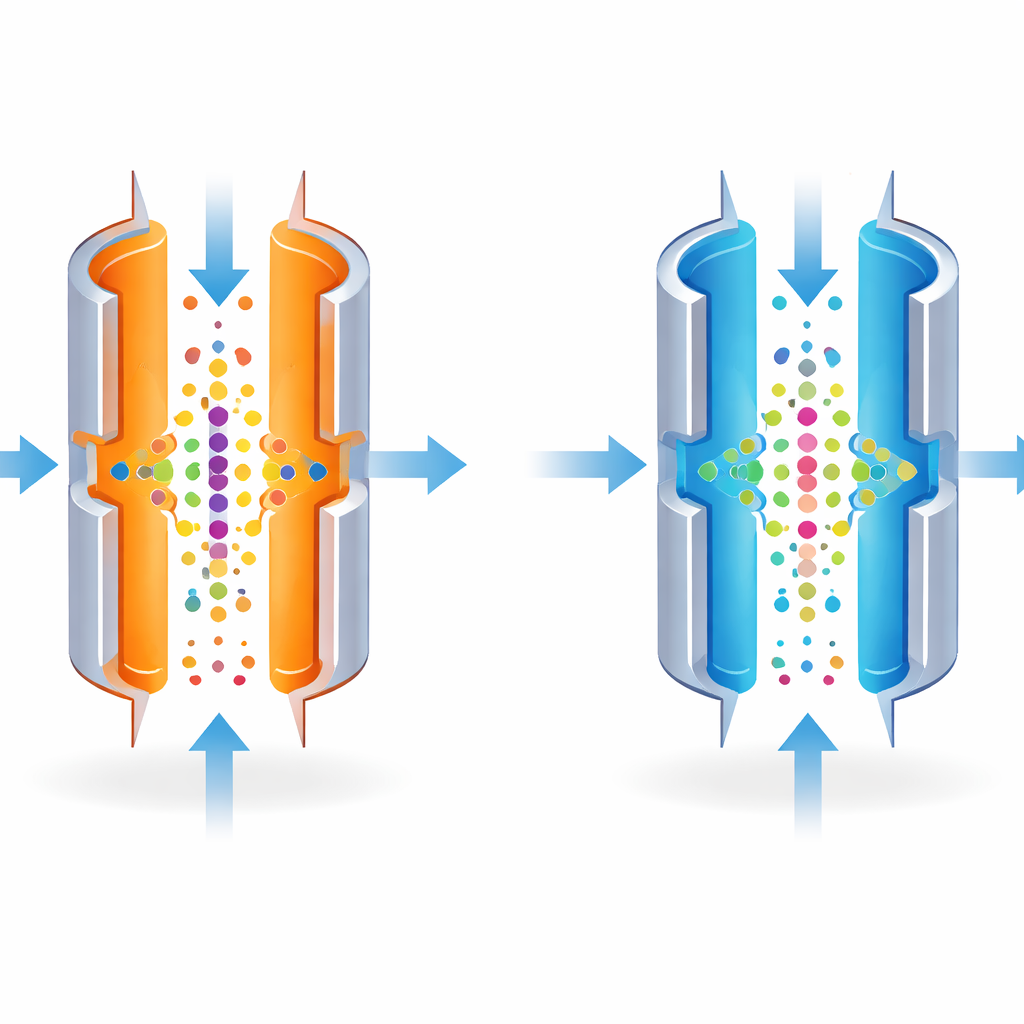
מבט טוב יותר בתוך תאים יחידים
החוקרים פנו לאחר מכן לדגימות תא יחיד אמיתיות מקו תאי סרטן ריאה בשם H460. שימוש בהגדרת FAIMS העדינה יותר שוב הגדיל הן את מספר הפפטידים והן את מספר החלבונים שהתגלו מכל תא. הרגישות הנוספת שיפרה את ה"טביעות האצבע" המתארות את הרכב החלבונים של כל תא, והפכה הבדלים בין תאים לברורים יותר. לבדיקות בקרה המכילות לא תאים נוצרו גם כן אותות, אך אלה השתקפו בעיקר רקע ושלבי טיפול. התצפית החשובה הייתה שאפילו שינוי פשוט בטמפרטורת הצלחות השפיע על מספר החלבונים משמעותיים שניתן לראות בתוך כל תא יחיד.
שינוי פשוט עם תשואה גדולה
בסך הכל, המחקר מראה שהורדת הרזולוציה של FAIMS בכוונה—על ידי קירור אחת מהצלחות—יכולה להגביר באופן מהותי כמה חתיכות חלבון מתגלות מדגימות זעירות במיוחד, כולל תאים יחידים. למי שאינו מומחה, המסקנה היא שלעיתים הרחבת מסננת משחררת מאפשרת לראות יותר ממה שחשוב: כאן, הפרדה מעט מטושטשת יותר ב-FAIMS מובילה לתמונה בהירה יותר של נוף החלבונים בתא. מאחר ששינוי זה משתמש בחומרה קיימת ובהגדרות פשוטות, מעבדות רבות יכולות לאמץ אותו במהירות ולהעמיק את ההבנה שלהן בביו־לממדים הקטנים ביותר.
ציטוט: Hoch, D.G., Belford, M., Heil, L.R. et al. Low-resolution FAIMS for increased peptide coverage in low-load and single-cell proteomics. Sci Rep 16, 14454 (2026). https://doi.org/10.1038/s41598-026-45228-3
מילות מפתח: פרוטאומיקה של תא יחיד, FAIMS, ספקטרומטריית מסה, ניתוח חלבונים, ניידות יונית