Clear Sky Science · es
FAIMS de baja resolución para aumentar la cobertura de péptidos en proteómica de carga baja y de una sola célula
Ver más con menos
La biología moderna a menudo trabaja con muestras increíblemente pequeñas, a veces el contenido de una sola célula. Para entender lo que ocurre dentro de estos mundos diminutos, los científicos dependen de herramientas capaces de detectar miles de proteínas diferentes a la vez. Este estudio muestra que, ajustando suavemente el modo de operación de una de esas herramientas, llamada FAIMS, los investigadores pueden ver muchas más piezas proteicas a partir de la misma cantidad minúscula de material, sin comprar nuevos instrumentos ni reescribir el software.
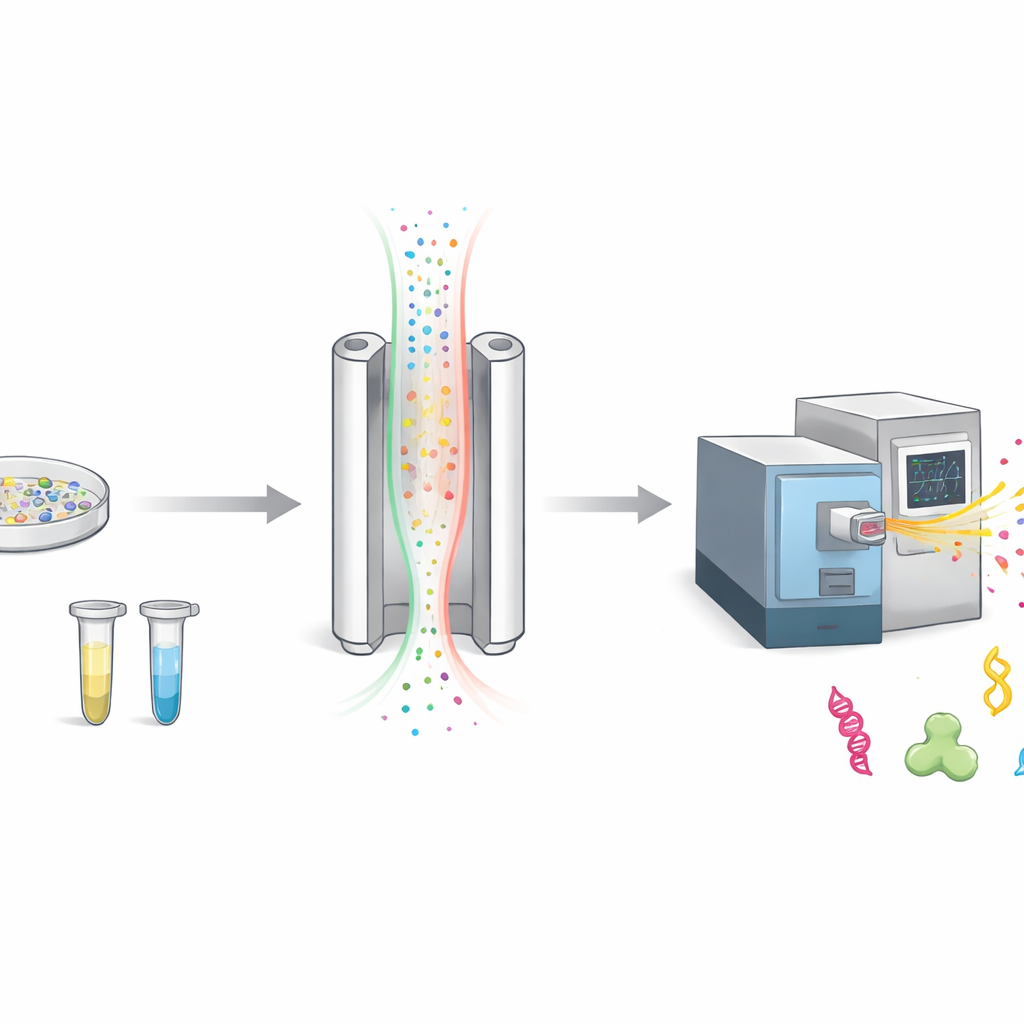
Cómo clasificamos moléculas cargadas en el aire
Cuando los científicos estudian proteínas, suelen trocearlas en fragmentos más pequeños llamados péptidos y luego pesarlos con un espectrómetro de masas. Antes de pesarlos, FAIMS añade un paso extra de clasificación. Envía moléculas cargadas a través de una ranura estrecha entre dos placas metálicas mientras cambia rápidamente un campo eléctrico. Solo las moléculas cuya movilidad coincide con un ajuste elegido pasan al detector; el resto se descarta como fondo. Esto hace la medida más limpia, pero también implica que muchas moléculas potencialmente interesantes nunca llegan al instrumento.
El intercambio entre nitidez y brillo
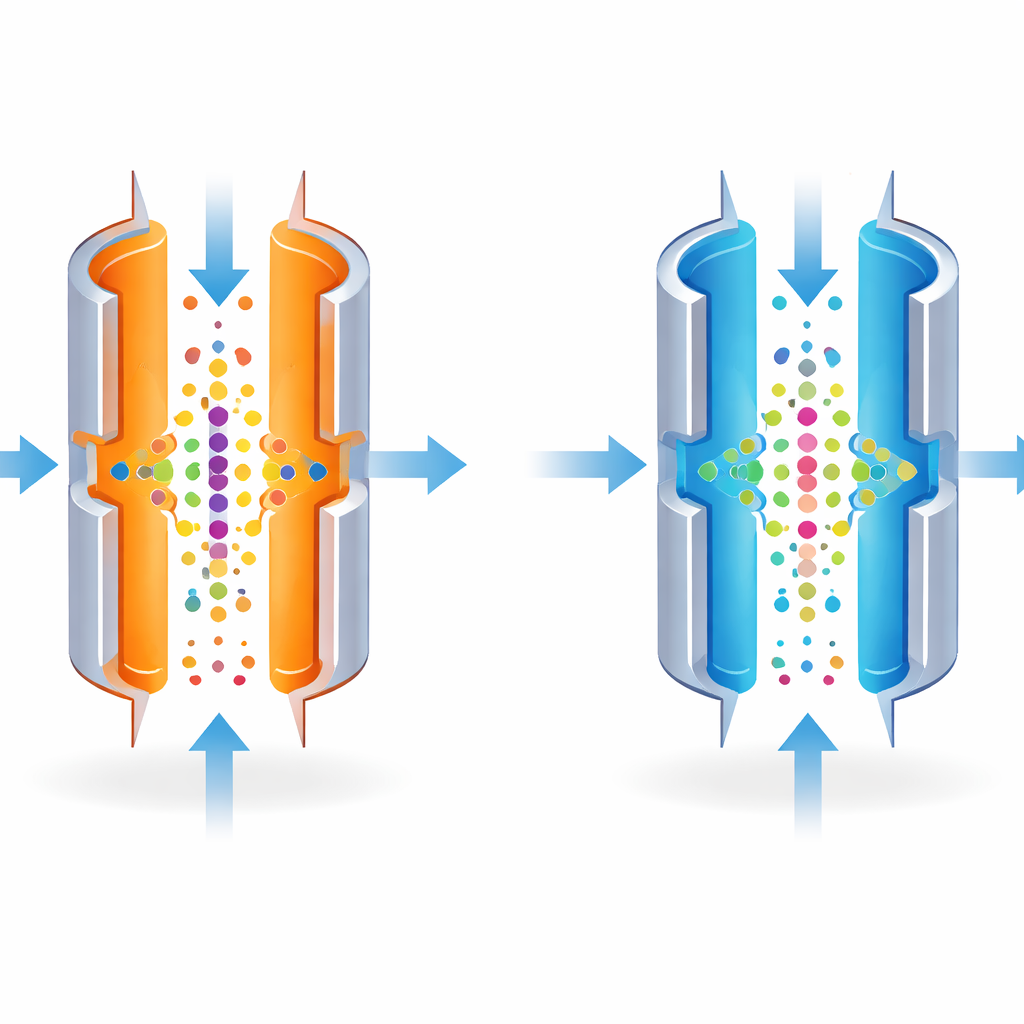
FAIMS puede ajustarse para separar las moléculas con gran precisión, como un objetivo fotográfico enfocado en un punto. Sin embargo, los ajustes más nítidos solo dejan pasar una estrecha franja de moléculas, atenuando la señal general. Los autores observaron que la temperatura de las placas metálicas afecta mucho cuán definida está esa franja. Enfriando la placa exterior respecto a la interior, hicieron intencionadamente la clasificación menos estricta. Esto amplió el rango de moléculas que podían atravesar con un mismo ajuste, permitiendo que más iones alcanzaran el espectrómetro de masas en una sola pasada.
Bajar la temperatura para revelar péptidos ocultos
El equipo probó primero la idea con mezclas estándar de moléculas conocidas y con cantidades muy pequeñas de una línea celular bien estudiada (HeLa). Bajar la temperatura de la placa exterior de 100 °C a 80 °C amplió la ventana de moléculas que pasaban por FAIMS e incrementó el número total de iones detectados. En términos prácticos, esto significó que el instrumento identificó entre un 25 y un 34 % más de péptidos distintos, y un aumento modesto en proteínas, a partir de la misma muestra diminuta. Estas ganancias fueron mayores en las cantidades de muestra más bajas, donde cada molécula adicional detectada importa más.
Mejores vistas dentro de células individuales
Los investigadores aplicaron después el ajuste más suave a muestras verdaderas de célula única de una línea de cáncer de pulmón llamada H460. Usar de nuevo la configuración más suave de FAIMS aumentó tanto el número de péptidos como el de proteínas detectadas en cada célula. La sensibilidad extra mejoró las "huellas" que describen la composición proteica de cada célula, haciendo más claras las diferencias entre células. Los pocillos de control sin células también generaron señales, pero estas reflejaron principalmente ruido de fondo y pasos de manipulación. La observación clave fue que simplemente cambiar la temperatura de la placa modificó cuántas proteínas relevantes podían verse dentro de cada célula individual.
Un ajuste sencillo con gran beneficio
En conjunto, el estudio demuestra que reducir deliberadamente la resolución de FAIMS—enfriando una de sus placas—puede aumentar sustancialmente cuántas piezas proteicas se detectan en muestras ultra pequeñas, incluidas células individuales. Para el público no especialista, la conclusión es que a veces aflojar un filtro permite ver mejor lo que importa: aquí, una separación ligeramente más difusa en FAIMS conduce a una imagen global más brillante del paisaje proteico de la célula. Dado que este cambio usa hardware existente y ajustes sencillos, muchos laboratorios pueden adoptarlo rápidamente para profundizar su visión de la biología a las escalas más pequeñas.
Cita: Hoch, D.G., Belford, M., Heil, L.R. et al. Low-resolution FAIMS for increased peptide coverage in low-load and single-cell proteomics. Sci Rep 16, 14454 (2026). https://doi.org/10.1038/s41598-026-45228-3
Palabras clave: proteómica de célula única, FAIMS, espectrometría de masas, análisis de proteínas, movilidad iónica