Clear Sky Science · ja
低サンプル量および単一細胞プロテオミクスにおけるペプチドカバレッジ向上のための低分解能FAIMS
少量からより多くを観る
現代の生物学では、しばしばごく微小な試料—ときには単一細胞の内容物—を扱います。こうした極小世界で何が起きているかを理解するために、研究者は同時に何千もの異なるタンパク質を検出できる道具に頼っています。本研究は、FAIMSと呼ばれるそのような機器の動作を穏やかに変えることで、新たな装置を購入したりソフトウェアを書き換えたりすることなく、同じわずかな試料からはるかに多くのタンパク質断片を観測できることを示しています。
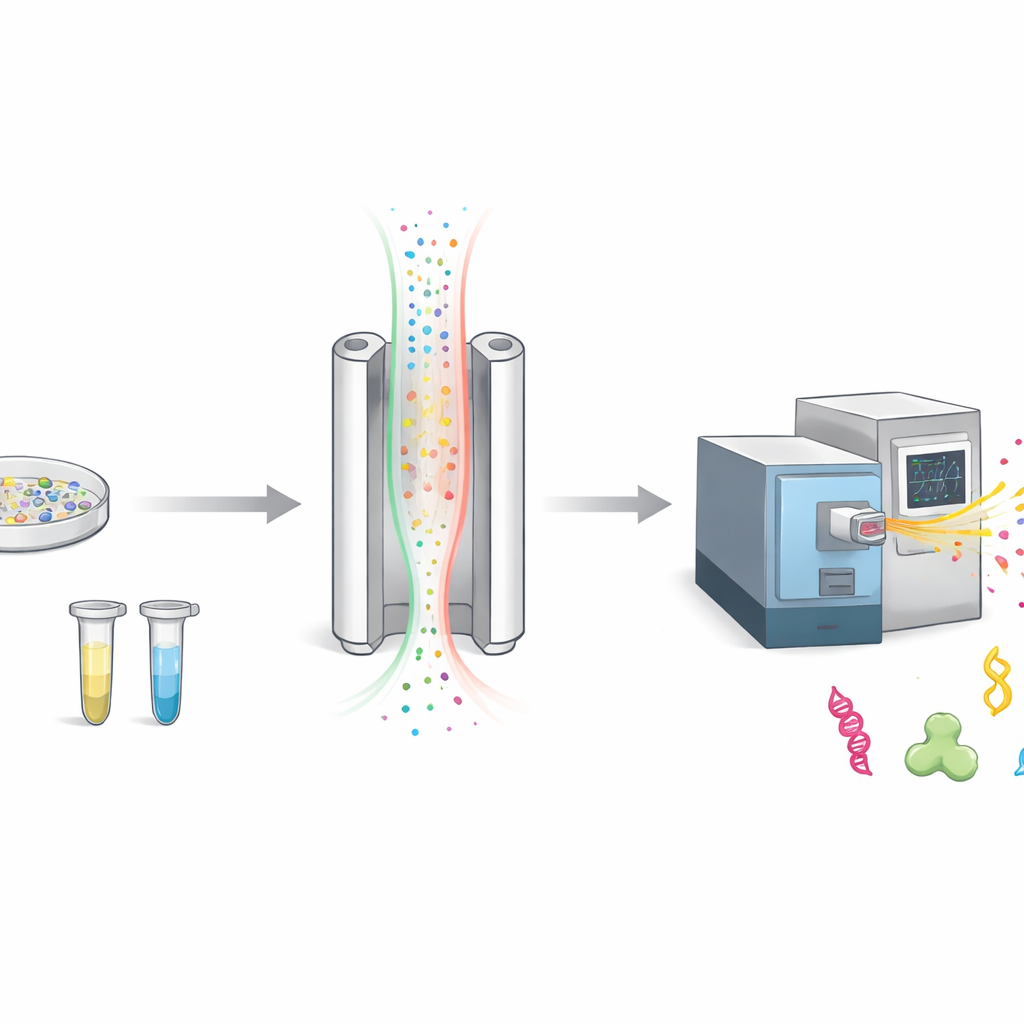
空中で荷電分子をどう仕分けるか
タンパク質を調べる際、通常はそれらをペプチドと呼ばれる小さな断片に切断し、質量分析計で質量を測ります。測定の前に、FAIMSは仕分けの追加ステップを挟みます。荷電した分子を二枚の金属板の間の狭いギャップに通しつつ、電界を高速で切り替えます。ある設定に合致する運動をする分子だけが検出器へ通過し、それ以外は背景として除かれます。これにより測定はクリーンになりますが、多くの興味深い分子が機器に届かないままになるという側面もあります。
鮮明さと明るさのトレードオフ
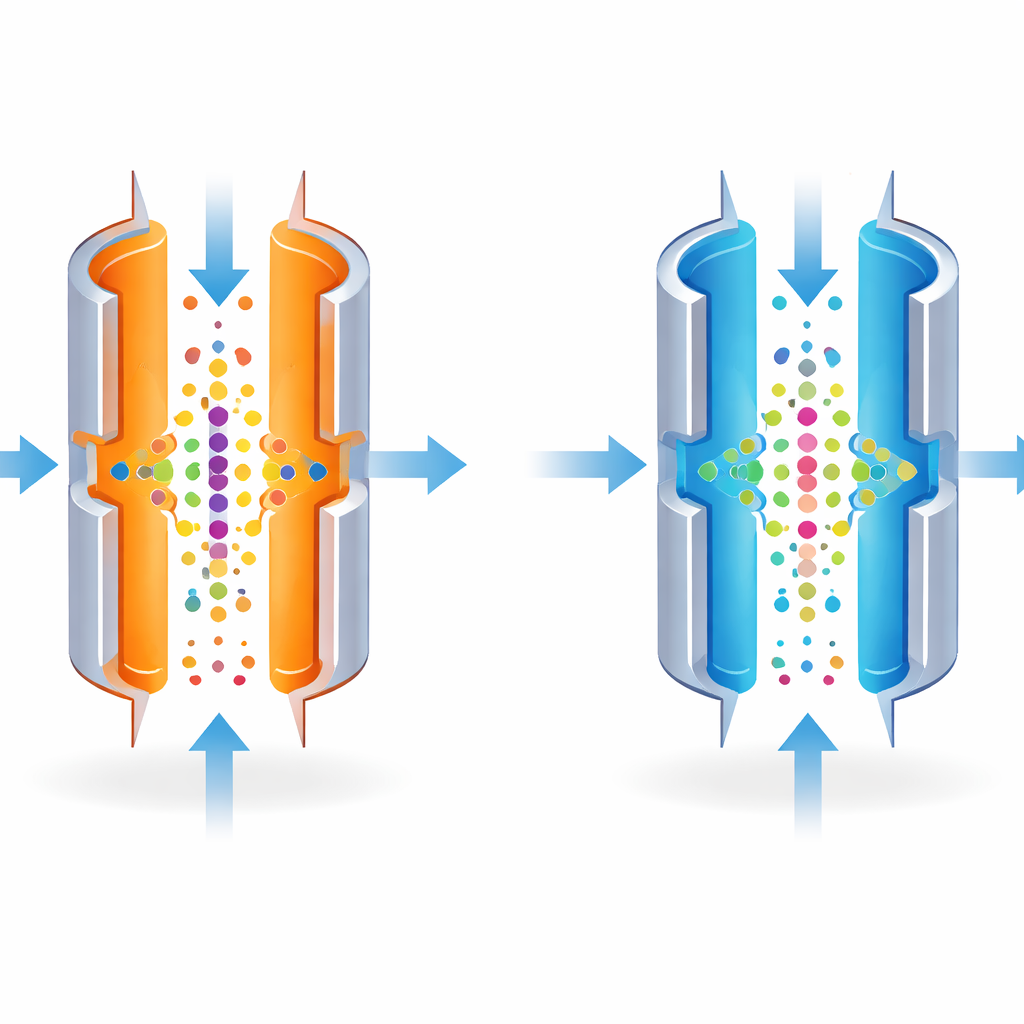
FAIMSはレンズを一点に合わせるかのように分子を非常に精密に分離するよう調整できます。しかし最もシャープな設定は狭い帯域しか通さず、全体の信号を暗くしてしまいます。著者らは、金属板の温度がこの帯域の幅に強く影響することに気づきました。外側の板を内側よりも冷やすことで、仕分けを意図的に厳しくしすぎないようにしました。これにより、ある設定で通過できる分子の範囲が広がり、単一の走査で質量分析計に到達するイオンが増えました。
隠れたペプチドを明らかにするために温度を下げる
まず研究チームは既知の分子の標準混合物と、よく研究された細胞株(HeLa)の非常に少量の試料でこの考えを検証しました。外側の板の温度を100°Cから80°Cに下げることで、FAIMSを通過する分子のウィンドウが拡大し、検出されるイオンの総数が増加しました。実務的には、同じわずかな試料から同定される異なるペプチド数が25~34%増え、タンパク質数もわずかに増加しました。これらの利得は試料量が最も少ない条件で最大になり、追加で検出される各分子の価値が最も大きくなりました。
単一細胞内部のより良い観察
次に研究者たちは、H460という肺がん細胞株からの真の単一細胞試料に取り組みました。穏やかなFAIMS設定を用いることで、各細胞から検出されるペプチド数とタンパク質数の両方が増加しました。感度の向上により、各細胞のタンパク質組成を表す“フィンガープリント”が改善され、細胞間の違いがより明確になりました。細胞を含まない対照ウェルでも信号は得られましたが、これらは主に背景や取り扱い工程に由来するものでした。重要な観察は、単に板の温度を変えるだけで、個々の細胞内で見ることのできる意味あるタンパク質の数が変わるという点でした。
単純な調整がもたらす大きな効果
総じて、この研究はFAIMSの分解能を意図的に下げる—すなわち一方の板を冷やす—ことで、超小量試料や単一細胞から検出されるタンパク質断片の数を大幅に増やせることを示しています。専門外の方への要点は、時にフィルターを緩めることで重要なものをより多く見られるということです。ここではFAIMSの分離をややぼかすことで、細胞のタンパク質風景の全体像がより明るくなります。この変更は既存のハードウェアと簡単な設定で実現できるため、多くの研究室が迅速に採用して、最小スケールの生物学をより深く観察できるようになるでしょう。
引用: Hoch, D.G., Belford, M., Heil, L.R. et al. Low-resolution FAIMS for increased peptide coverage in low-load and single-cell proteomics. Sci Rep 16, 14454 (2026). https://doi.org/10.1038/s41598-026-45228-3
キーワード: 単一細胞プロテオミクス, FAIMS, 質量分析, タンパク質解析, イオン移動度