Clear Sky Science · pt
Sequência completa do genoma de Sphingomonas sp. gentR, uma bactéria com alta resistência à gentamicina
Por que um microrganismo de laboratório importa para a medicina do dia a dia
Antibióticos como a gentamicina são pilares em hospitais e fazendas, mas as bactérias vêm aprendendo progressivamente a sobreviver a eles. Este estudo focaliza um micro-organismo incomumente resistente chamado Sphingomonas sp. gentR, capaz de tolerar doses massivas de gentamicina. Ao decodificar seu roteiro genético completo, os pesquisadores revelam onde seus artifícios de resistência estão escondidos e disponibilizam esses dados livremente para que outros possam rastrear, compreender e, talvez, desarmar microrganismos semelhantes antes que suas defesas se espalhem para bactérias causadoras de doenças.
Um micro-organismo resistente vindo de um frasco de antibiótico
A história começa em um laboratório comum, onde uma solução de trabalho de gentamicina — um antibiótico usado para tratar infecções graves — havia sido armazenada sob refrigeração. Dessa mesma solução, a equipe isolou inesperadamente uma bactéria amarelada, em forma de bastonete, pertencente ao grupo Sphingomonas. Ao testar a quantidade de gentamicina que ela podia suportar, o microrganismo cresceu mesmo em concentrações cerca de mil vezes maiores do que aquelas que inibem muitas bactérias, identificando-o como um sobrevivente extremo. Espécies de Sphingomonas já são conhecidas por viver em ambientes hostis, como areias do deserto, gelo glacial, rochas profundas e até naves espaciais, mas esse nível de resistência à gentamicina não havia sido observado no grupo antes.
Lendo o manual de instruções completo do microrganismo
Para descobrir o que tornava essa linhagem tão resistente, os cientistas extraíram seu DNA e usaram duas tecnologias de sequenciamento complementares. Uma produziu muitos fragmentos de DNA curtos e precisos, enquanto a outra gerou menos fragmentos, porém muito longos. Ao combinar esses dados, montaram um genoma completo e sem lacunas da bactéria: um cromossomo circular principal e dois fragmentos circulares menores de DNA chamados plasmídeos. Em seguida, empregaram um conjunto de ferramentas computacionais especializadas e bancos de dados de referência para prever genes, localizar elementos móveis como vírus e ilhas genômicas, e atribuir funções prováveis a quase todas as partes do genoma, desde metabolismo básico até respostas ao estresse.
Onde a resistência está escondida
Com o genoma completo em mãos, a equipe o comparou a coleções curadas de genes de resistência a antibióticos conhecidos. Encontraram um pequeno conjunto de genes claramente associados à resistência contra várias classes de drogas. Mais notavelmente, três genes de resistência confirmados — dois que podem inativar aminoglicosídeos como gentamicina e estreptomicina, e um que protege contra sulfonamidas — estão agrupados em um trecho distinto de DNA inserido em um dos plasmídeos. Essa região, conhecida como ilha genômica, é o equivalente molecular de um módulo plug-and-play: um aglomerado de genes que pode se mover entre moléculas de DNA e, potencialmente, entre bactérias. O genoma também contém muitos genes que afinam como a célula percebe o ambiente, bombeia compostos tóxicos para fora e mantém suas membranas, todos os quais podem reforçar a sobrevivência sob estresse por antibióticos.
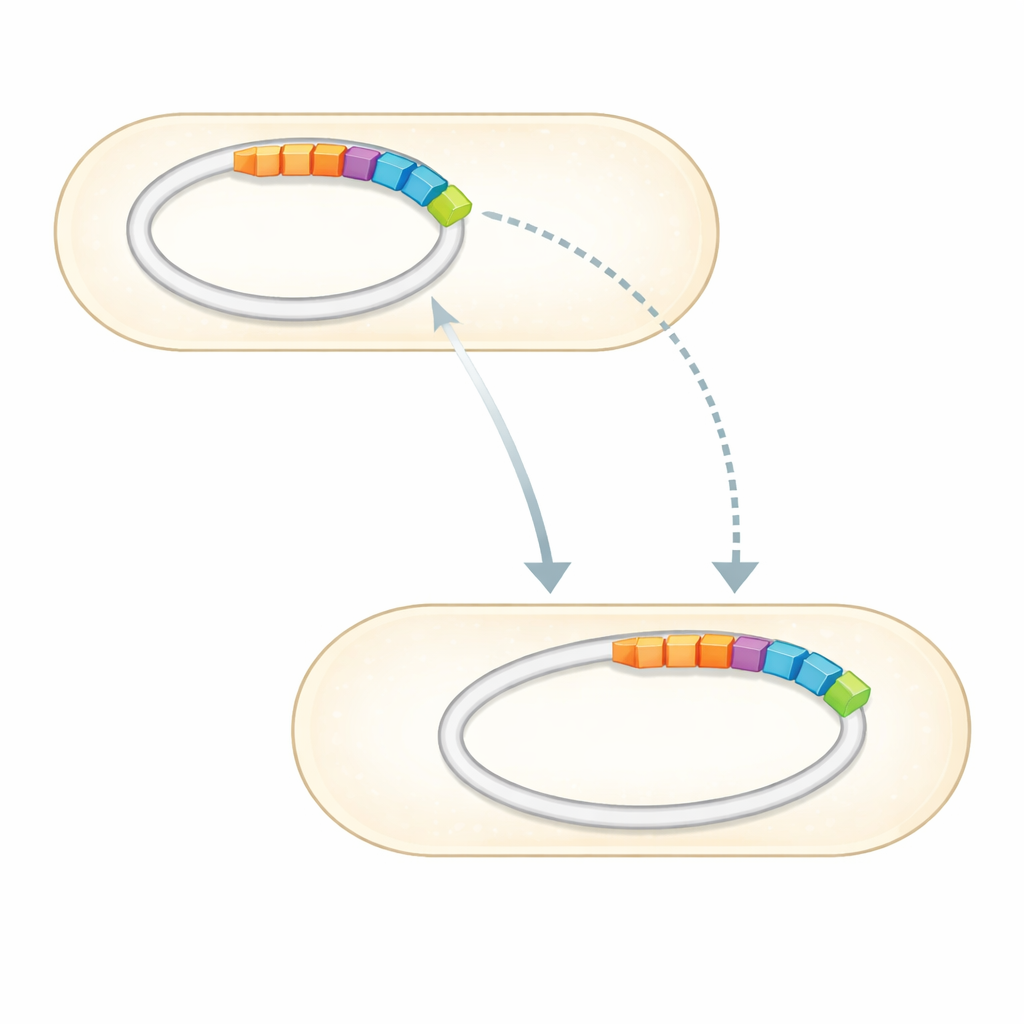
Um conjunto de ferramentas versátil para viver em ambientes adversos
Além da própria resistência, o catálogo gênico apresenta Sphingomonas sp. gentR como um generalista metabólico bem adaptado a viver em ambientes pobres ou poluídos. Muitos de seus genes suportam produção de energia, utilização de aminoácidos e a degradação ou transporte de moléculas diversas, sugerindo que pode recorrer a fontes de alimento incomuns. Outros indicam capacidade de tolerar diferentes estresses e possivelmente degradar compostos estrangeiros. Essa versatilidade ajuda a explicar por que espécies de Sphingomonas são estudadas tanto como parceiras benéficas para plantas quanto como agentes de limpeza para contaminantes industriais, e por que uma linhagem individual pode prosperar em um nicho rico em antibióticos, como uma solução de fármaco.
O que este genoma significa para a saúde e o meio ambiente
Ao mapear completamente o DNA de uma linhagem de Sphingomonas excepcionalmente resistente à gentamicina e localizar seus genes-chave de resistência em uma ilha móvel de um plasmídeo, o estudo fornece uma referência detalhada para cientistas em todo o mundo. Para a saúde pública, destaca uma via potencial pela qual traços poderosos de resistência podem saltar de bactérias ambientais inofensivas para patógenos que infectam pessoas, animais ou culturas. Para as ciências ambientais e biotecnologia, oferece um kit genético que pode ser aproveitado para limpar locais poluídos onde antibióticos ou outros químicos se acumulam. Em termos simples, o trabalho mostra tanto o quão resistentes alguns microrganismos de fundo se tornaram quanto dá aos pesquisadores as instruções necessárias para monitorar e gerir essa resistência.
Citação: Liu, Y., Jiang, L., Zhang, J. et al. Complete genome sequence of Sphingomonas sp. gentR, a high-level gentamicin-resistant bacterium. Sci Data 13, 672 (2026). https://doi.org/10.1038/s41597-026-06723-4
Palavras-chave: resistência a antibióticos, gentamicina, Sphingomonas, genoma bacteriano, genes plasmidiais