Clear Sky Science · nl
Complete genoomsequentie van Sphingomonas sp. gentR, een hooggradig gentamicine-resistente bacterie
Waarom een laboratoriummicrobe van belang is voor alledaagse geneeskunde
Antibiotica zoals gentamicine zijn werkpaarden in ziekenhuizen en op boerderijen, maar bacteriën leren gestaag hoe ze eraan kunnen ontsnappen. Deze studie zoomt in op één enkele, uitzonderlijk taaie microbe genaamd Sphingomonas sp. gentR die enorme doses gentamicine kan weerstaan. Door zijn volledige genetische blauwdruk te decoderen, onthullen de onderzoekers waar zijn resistentiemechanismen verborgen zitten en maken die gegevens vrij beschikbaar zodat anderen vergelijkbare microben kunnen volgen, begrijpen en mogelijk ontwapenen voordat die verdedigingsmechanismen zich naar ziekteverwekkende bacteriën verspreiden.
Een robuuste microbe uit een flesje antibioticum
Het verhaal begint in een gewoon laboratorium, waar een werkoplossing van gentamicine—een antibioticum dat wordt gebruikt voor de behandeling van ernstige infecties—in de kou was bewaard. Uit diezelfde oplossing is het team onverwacht een gele, staafvormige bacterie van de Sphingomonas-groep geïsoleerd. Bij tests om te bepalen hoeveel gentamicine hij kon verdragen, groeide de microbe zelfs bij concentraties die ongeveer duizend keer hoger liggen dan die welke veel bacteriën stoppen, waarmee hij als een extreme overlever wordt aangemerkt. Sphingomonas-soorten staan al bekend om hun vermogen te overleven in barre omgevingen zoals woestijnzanden, gletsjerijs, diepe ondergrondse gesteenten en zelfs ruimtevaartuigen, maar dit niveau van gentamicineresistentie was binnen de groep nog niet eerder gezien.
Het hele instructieboekje van de microbe lezen
Om te achterhalen wat deze stam zo veerkrachtig maakte, haalden de wetenschappers zijn DNA eruit en gebruikten twee aanvullende sequentietechnologieën. De ene leverde veel korte, nauwkeurige DNA-fragmenten, terwijl de andere minder maar zeer lange fragmenten produceerde. Door deze gegevens te combineren assembleerden ze een volledig, gatvrij genoom van de bacterie: één hoofdcirculair chromosoom en twee kleinere circulaire DNA-stukjes die plasmiden worden genoemd. Vervolgens zetten ze een reeks gespecialiseerde computerhulpmiddelen en referentiedatabases in om genen te voorspellen, mobiele elementen zoals virussen en genomische eilanden te lokaliseren, en waarschijnlijke functies toe te kennen aan vrijwel elk deel van het genoom, van basaal metabolisme tot stressresponsen.
Waar de resistentie zich verschuilt
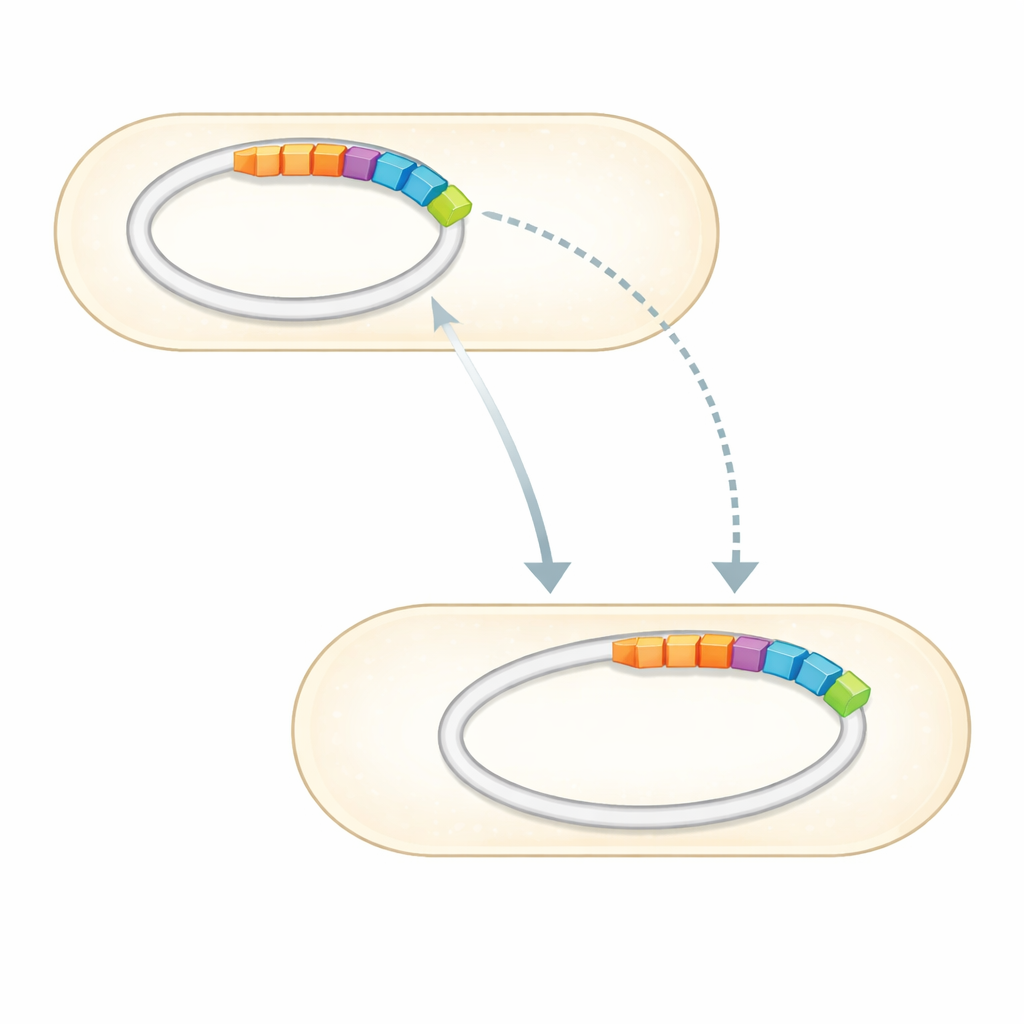
Met het volledige genoom in handen doorzocht het team het tegen gecureerde verzamelingen van bekende antibioticaresistentiegenen. Ze vonden een kleine set genen die duidelijk gekoppeld zijn aan resistentie tegen meerdere geneesmiddelklassen. Meest opvallend zitten drie bevestigde resistentiegenen—twee die aminoglycoside-antibiotica zoals gentamicine en streptomycine kunnen inactiveren, en één die beschermt tegen sulfonamiden—samen op een specifieke DNA-strook ingebed in een van de plasmiden. Dit gebied, bekend als een genomisch eiland, is het moleculaire equivalent van een plug-and-play-module: een cluster van genen die kan bewegen tussen DNA-moleculen en mogelijk tussen bacteriën. Het genoom draagt ook veel genen die fijnregelen hoe de cel zijn omgeving waarneemt, toxische verbindingen uitpompt en zijn membranen onderhoudt, wat allemaal kan bijdragen aan overleving onder antibiotische stress.
Een veelzijdige gereedschapskist voor leven in zware omstandigheden
Voorbij de resistentie zelf schetst het gencatalogus Sphingomonas sp. gentR als een metabole generalist, goed aangepast aan leven in arme of vervuilde omgevingen. Veel van zijn genen ondersteunen energieproductie, gebruik van aminozuren en de afbraak of het transport van diverse moleculen, wat suggereert dat hij op ongewone voedselbronnen kan teren. Andere genen wijzen op het vermogen verschillende stressfactoren te weerstaan en mogelijk vreemde chemicaliën af te breken. Deze veelzijdigheid helpt verklaren waarom Sphingomonas-soorten worden onderzocht als zowel plantenvriendelijke partners als opruimingsagenten voor industriële verontreiniging, en waarom een individuele stam kan floreren in een antibioticumrijke nis zoals een geneesmiddeloplossing.
Wat dit genoom betekent voor gezondheid en milieu
Door het DNA van een uitzonderlijk gentamicine-resistente Sphingomonas-stam volledig in kaart te brengen en zijn sleutelresistentiegenen aan een mobiel eiland op een plasmide te koppelen, levert de studie een gedetailleerde referentie voor wetenschappers wereldwijd. Voor de volksgezondheid benadrukt het een mogelijk pad waarlangs sterke resistentiekenmerken kunnen overspringen van onschuldige omgevingsbacteriën naar pathogenen die mensen, dieren of gewassen infecteren. Voor milieu- en biotechnologieonderzoek biedt het een genetische gereedschapskist die kan worden aangewend voor het opschonen van verontreinigde locaties waar antibiotica of andere chemicaliën zich ophopen. In eenvoudige bewoordingen laat het werk zien hoe taai sommige achtergrondmicroben zijn geworden en geeft het onderzoekers de instructies die ze nodig hebben om die taaiheid te monitoren en te beheersen.
Bronvermelding: Liu, Y., Jiang, L., Zhang, J. et al. Complete genome sequence of Sphingomonas sp. gentR, a high-level gentamicin-resistant bacterium. Sci Data 13, 672 (2026). https://doi.org/10.1038/s41597-026-06723-4
Trefwoorden: antibioticaresistentie, gentamicine, Sphingomonas, bacterieel genoom, plasmidegenen