Clear Sky Science · pl
Kompletny sekwencjonowanie genomu Sphingomonas sp. gentR, bakterii o wysokiej oporności na gentamycynę
Dlaczego drobnoustrój z laboratorium ma znaczenie dla codziennej medycyny
Antybiotyki takie jak gentamycyna są filarami opieki zdrowotnej i hodowli zwierząt, ale bakterie stopniowo uczą się, jak im się przeciwstawiać. To badanie koncentruje się na pojedynczym, niezwykle odpornym drobnoustroju o nazwie Sphingomonas sp. gentR, który potrafi przetrwać olbrzymie dawki gentamycyny. Dekodując jego pełny plan genetyczny, badacze ujawniają, gdzie ukryte są mechanizmy oporności i udostępniają te dane powszechnie, aby inni mogli śledzić, rozumieć i być może unieszkodliwiać podobne mikroby, zanim ich mechanizmy rozprzestrzenią się do bakterii chorobotwórczych.
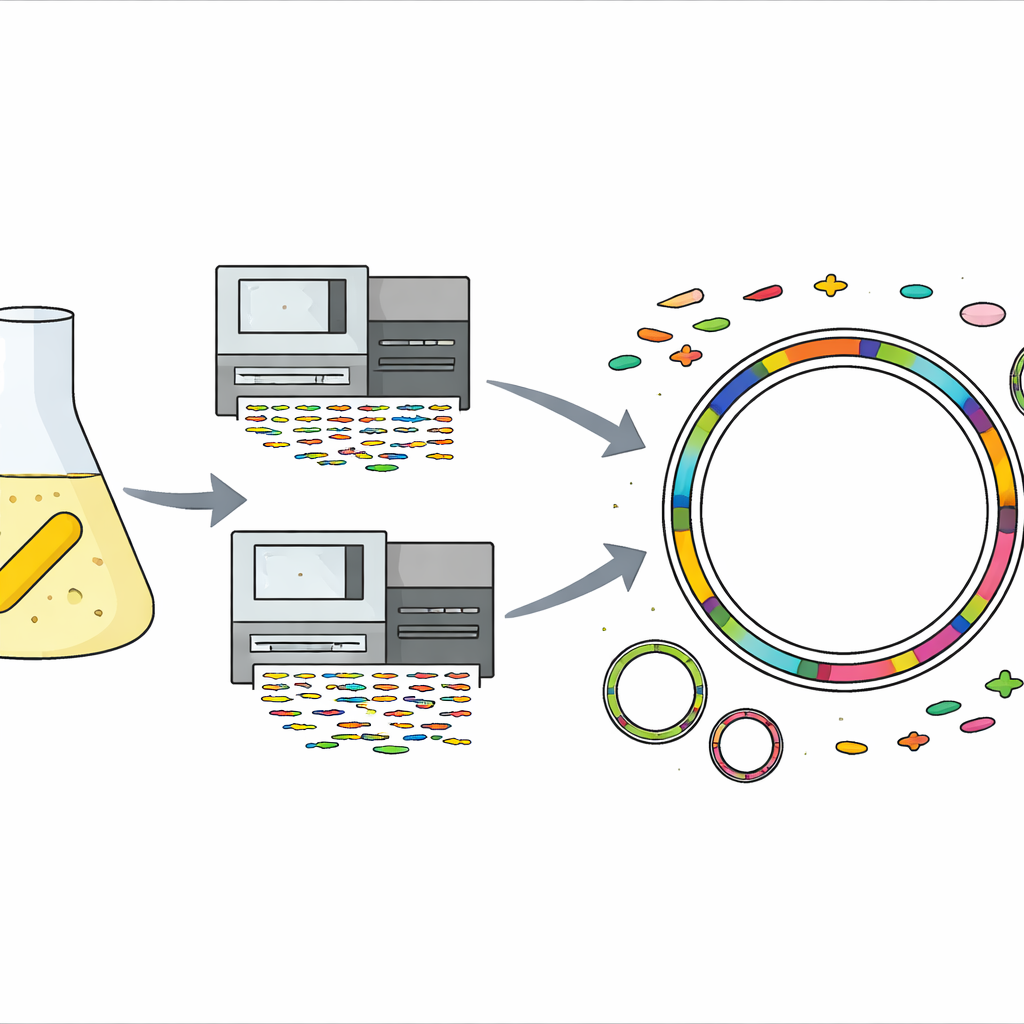
Wytrzymały drobnoustrój z butelki z antybiotykiem
Historia zaczyna się w zwykłym laboratorium, gdzie roztwór roboczy gentamycyny — antybiotyku stosowanego w leczeniu poważnych infekcji — był przechowywany w chłodzie. Z tego właśnie roztworu zespół niespodziewanie wyizolował żółtą, pałeczkowatą bakterię należącą do grupy Sphingomonas. Testy tolerancji na gentamycynę wykazały, że drobnoustrój rósł nawet przy stężeniach około tysiąc razy wyższych od tych, które zahamowują wiele bakterii, co czyni go skrajnym przetrwańcem. Gatunki Sphingomonas są już znane z życia w ekstremalnych miejscach, takich jak piaszczyste pustynie, lodowce, skały głęboko pod ziemią, a nawet na pokładach statków kosmicznych, lecz tak wysoki poziom odporności na gentamycynę nie był wcześniej obserwowany w tej grupie.
Odczytywanie całego podręcznika instrukcji mikroba
Aby dowiedzieć się, co czyni ten szczep tak odpornym, naukowcy wyizolowali jego DNA i zastosowali dwie komplementarne technologie sekwencjonowania. Jedna dostarczyła wiele krótkich, precyzyjnych fragmentów DNA, podczas gdy druga wytworzyła mniej, ale bardzo długich odcinków. Łącząc te dane, złożyli kompletny, pozbawiony luk genom bakterii: jedną główną kolistą chromosomową cząstkę i dwa mniejsze koliste fragmenty DNA zwane plazmidami. Następnie użyli zestawu wyspecjalizowanych narzędzi komputerowych i baz referencyjnych, by przewidzieć geny, zlokalizować elementy mobilne takie jak wirusy czy wyspy genomowe oraz przypisać prawdopodobne funkcje niemal każdemu fragmentowi genomu, od podstawowego metabolizmu po reakcje na stres.
Gdzie ukrywa się oporność
Mając pełny genom, zespół porównał go z uporządkowanymi zbiorami znanych genów oporności na antybiotyki. Odkryli niewielki zestaw genów wyraźnie związanych z opornością na kilka klas leków. Najbardziej uderzające były trzy potwierdzone geny oporności — dwa, które mogą inaktywować aminoglikozydowe antybiotyki, takie jak gentamycyna i streptomycyna, oraz jeden chroniący przed sulfonamidami — umieszczone razem na wyraźnym odcinku DNA osadzonym w jednym z plazmidów. Ten region, znany jako wyspa genomowa, jest molekularnym odpowiednikiem modułu plug-and-play: skupiskiem genów, które mogą przemieszczać się między cząstkami DNA i potencjalnie między bakteriami. Genom zawiera też wiele genów regulujących, jak komórka odbiera sygnały ze środowiska, wypompowuje toksyczne związki i utrzymuje błony komórkowe, co łącznie może wzmacniać przetrwanie pod presją antybiotyków.
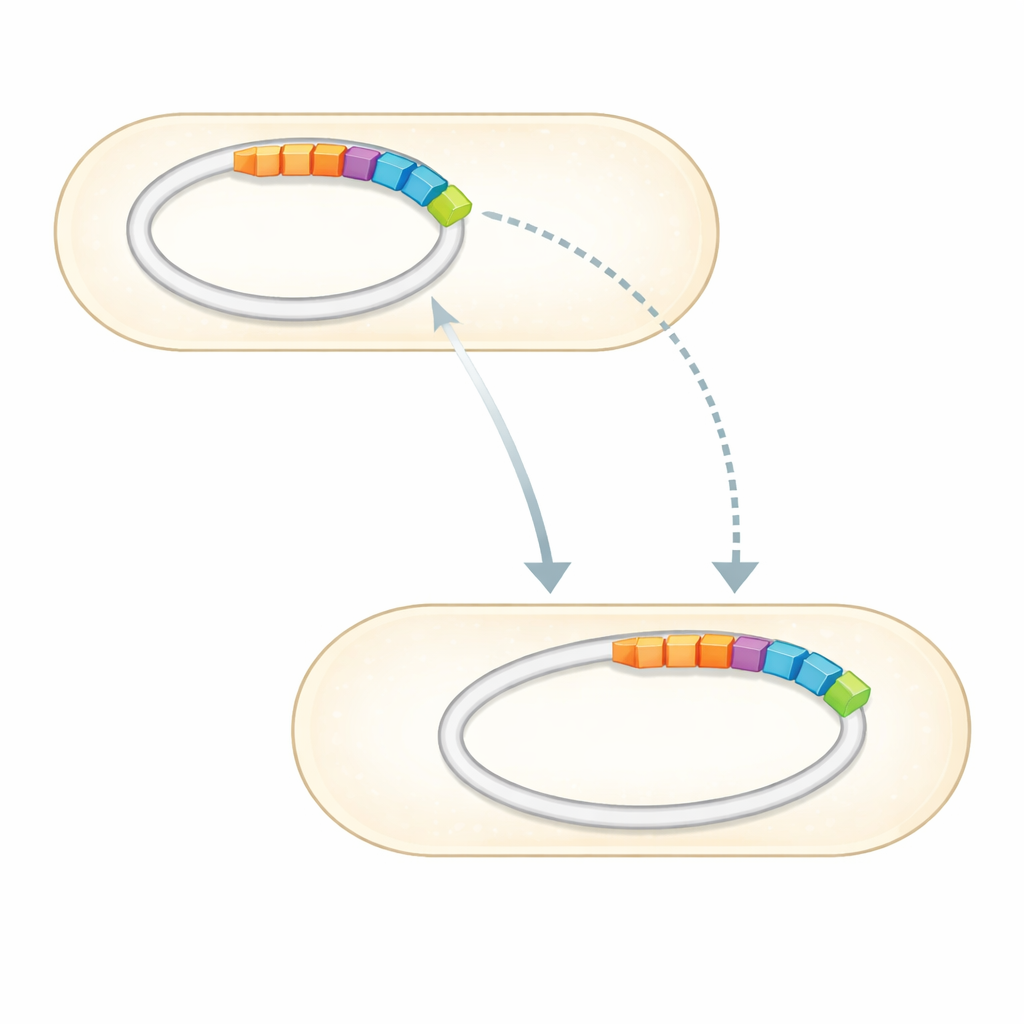
Wszechstronne narzędzia do życia w trudnych warunkach
Powyżej samej oporności, katalog genów przedstawia Sphingomonas sp. gentR jako metabolicznego generalistę dobrze przystosowanego do życia w ubogich lub zanieczyszczonych środowiskach. Wiele jego genów wspiera produkcję energii, wykorzystanie aminokwasów oraz rozkład i transport różnorodnych cząsteczek, co sugeruje zdolność do korzystania z nietypowych źródeł pokarmu. Inne wskazują na zdolność radzenia sobie z różnymi stresami i być może rozkładu obcych substancji chemicznych. Ta wszechstronność pomaga wyjaśnić, dlaczego gatunki Sphingomonas są badane jako przyjazni roślinom partnerzy oraz jako środki oczyszczające środowiska z przemysłowych zanieczyszczeń, i dlaczego pojedynczy szczep może rozkwitać w niszy bogatej w antybiotyki, takiej jak roztwór leku.
Co ten genom znaczy dla zdrowia i środowiska
Pełne zmapowanie DNA wyjątkowo opornego na gentamycynę szczepu Sphingomonas i umiejscowienie jego kluczowych genów oporności na ruchomej wyspie w plazmidzie dostarcza szczegółowego odniesienia dla naukowców na całym świecie. Dla zdrowia publicznego podkreśla potencjalną ścieżkę, poprzez którą silne cechy oporności mogą przeskoczyć z niegroźnych, środowiskowych bakterii do patogenów zakażających ludzi, zwierzęta lub rośliny. Dla nauk o środowisku i biotechnologii oferuje zestaw genetycznych narzędzi, które można wykorzystać do oczyszczania zanieczyszczonych miejsc, gdzie akumulują się antybiotyki lub inne związki chemiczne. Mówiąc prościej, praca pokazuje zarówno, jak odporne stały się niektóre bakterie tła, jak i daje badaczom instrukcje potrzebne do monitorowania i zarządzania tą odpornością.
Cytowanie: Liu, Y., Jiang, L., Zhang, J. et al. Complete genome sequence of Sphingomonas sp. gentR, a high-level gentamicin-resistant bacterium. Sci Data 13, 672 (2026). https://doi.org/10.1038/s41597-026-06723-4
Słowa kluczowe: oporność na antybiotyki, gentamycyna, Sphingomonas, genom bakterii, geny plazmidowe