Clear Sky Science · fr
Séquence complète du génome de Sphingomonas sp. gentR, une bactérie fortement résistante à la gentamicine
Pourquoi un microbe de laboratoire compte pour la médecine de tous les jours
Des antibiotiques comme la gentamicine sont des piliers dans les hôpitaux et les élevages, mais les bactéries apprennent progressivement à y survivre. Cette étude se concentre sur un microbe particulier, remarquablement résistant, appelé Sphingomonas sp. gentR, capable de supporter des doses massives de gentamicine. En décodant son plan génétique complet, les chercheurs dévoilent où se cachent ses mécanismes de résistance et rendent ces données accessibles pour que d’autres puissent suivre, comprendre et peut‑être neutraliser des microbes similaires avant que leurs défenses ne se transmettent à des bactéries pathogènes.
Un microbe coriace issu d’un flacon d’antibiotique
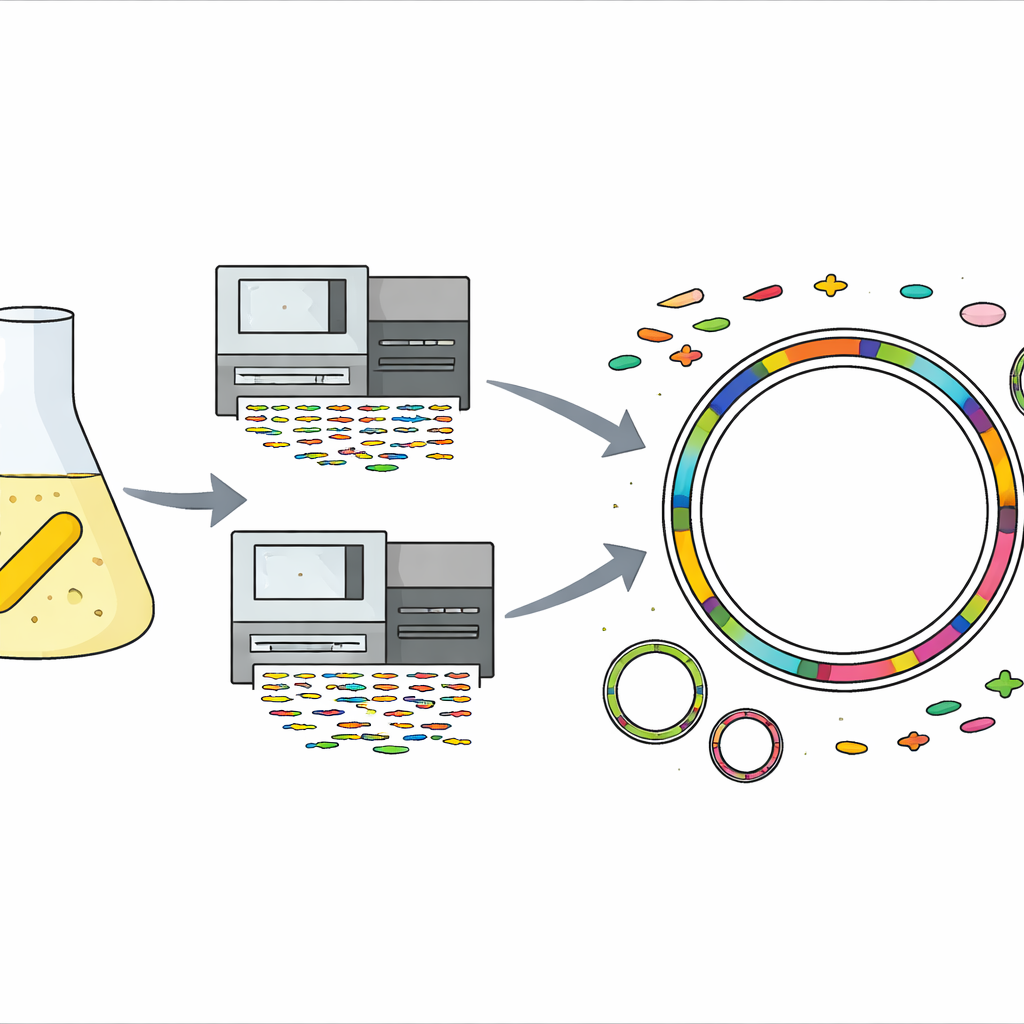
L’histoire commence dans un laboratoire ordinaire, où une solution de travail de gentamicine — un antibiotique utilisé pour traiter des infections graves — avait été conservée au froid. C’est à partir de cette même solution que l’équipe a isolé, de manière inattendue, une bactérie jaune en forme de bâtonnet appartenant au groupe Sphingomonas. Lorsqu’ils ont testé la quantité de gentamicine qu’elle pouvait tolérer, le microbe a poussé même à des concentrations environ mille fois supérieures à celles qui arrêtent de nombreuses bactéries, le classant parmi les survivants extrêmes. Les espèces de Sphingomonas sont déjà connues pour vivre dans des milieux hostiles comme les sables désertiques, les glaces glaciaires, les roches en profondeur et même les engins spatiaux, mais un tel niveau de résistance à la gentamicine n’avait pas été observé auparavant dans ce groupe.
Lire le mode d’emploi complet du microbe
Pour comprendre ce qui rendait cette souche si résistante, les scientifiques ont extrait son ADN et utilisé deux technologies de séquençage complémentaires. L’une a produit de nombreux fragments d’ADN courts et précis, tandis que l’autre a généré moins de fragments mais très longs. En combinant ces données, ils ont assemblé un génome complet et sans lacunes pour la bactérie : un chromosome circulaire principal et deux petites molécules d’ADN circulaires appelées plasmides. Ils ont ensuite utilisé une suite d’outils informatiques spécialisés et des bases de données de référence pour prédire les gènes, repérer les éléments mobiles comme les virus et les îlots génomiques, et attribuer une fonction probable à presque chaque partie du génome, de la métabolisme de base aux réponses au stress.
Où se cache la résistance
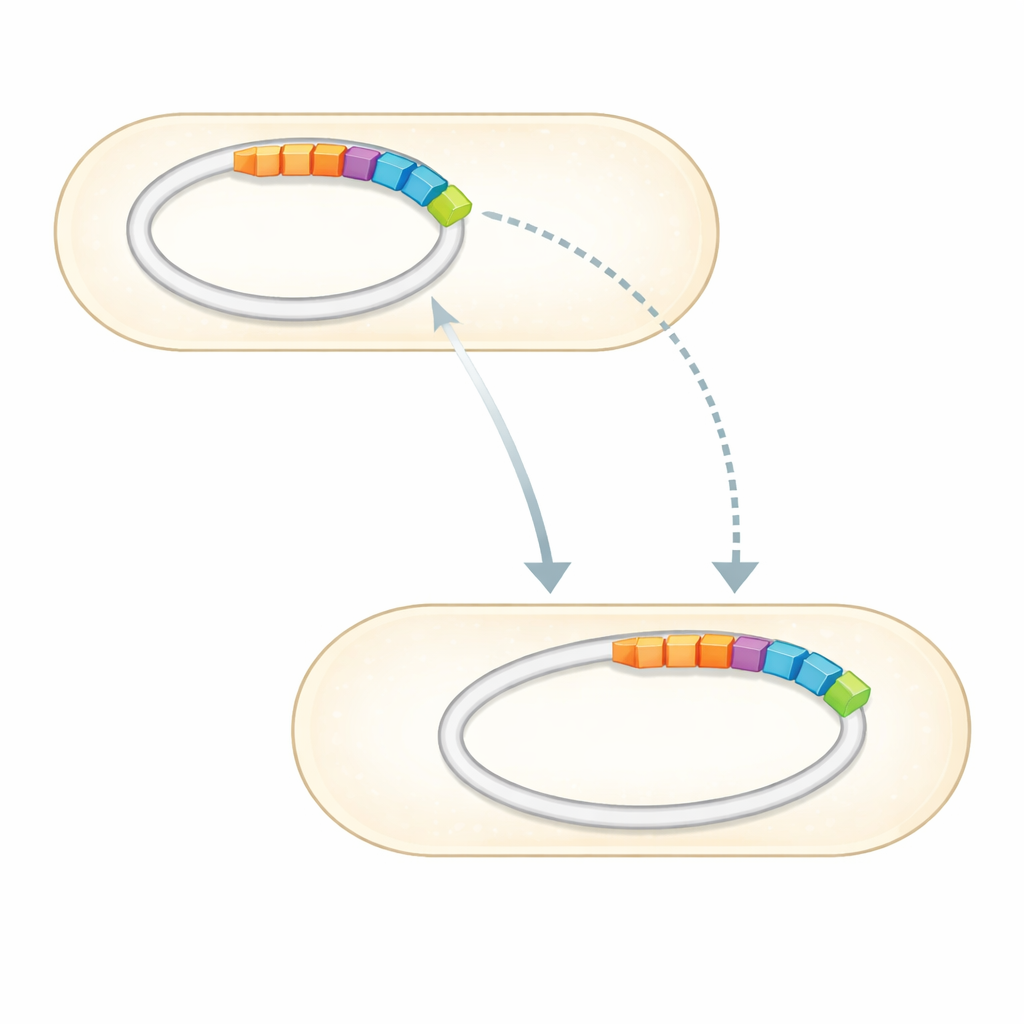
Avec le génome complet en main, l’équipe l’a comparé à des collections annotées de gènes de résistance aux antibiotiques. Ils ont identifié un petit ensemble de gènes clairement liés à la résistance contre plusieurs classes de médicaments. De façon particulièrement frappante, trois gènes de résistance confirmés — deux capables d’inactiver les aminoglycosides tels que la gentamicine et la streptomycine, et un qui protège contre les sulfamides — sont regroupés sur un segment distinct d’ADN intégré dans l’un des plasmides. Cette région, connue sous le nom d’îlot génomique, est l’équivalent moléculaire d’un module plug-and-play : un groupe de gènes pouvant se déplacer entre molécules d’ADN et, potentiellement, entre bactéries. Le génome porte aussi de nombreux gènes qui affinent la manière dont la cellule détecte son environnement, expulse des composés toxiques et maintient ses membranes, autant de fonctions susceptibles de renforcer la survie sous pression antibiotique.
Une boîte à outils polyvalente pour vivre dans des milieux difficiles
Au‑delà de la résistance elle‑même, le catalogue de gènes peint Sphingomonas sp. gentR comme un généraliste métabolique bien adapté à la vie dans des environnements pauvres ou pollués. Beaucoup de ses gènes soutiennent la production d’énergie, l’utilisation des acides aminés et la dégradation ou le transport de molécules diverses, ce qui suggère qu’il peut exploiter des sources de nourriture inhabituelles. D’autres évoquent la capacité à résister à différents stress et peut‑être à dégrader des composés étrangers. Cette polyvalence aide à expliquer pourquoi les espèces de Sphingomonas sont étudiées à la fois comme partenaires favorables aux plantes et comme agents de dépollution industrielle, et pourquoi une souche individuelle peut prospérer dans une niche riche en antibiotiques, comme une solution médicamenteuse.
Ce que ce génome signifie pour la santé et l’environnement
En cartographiant entièrement l’ADN d’une souche de Sphingomonas exceptionnellement résistante à la gentamicine et en localisant ses principaux gènes de résistance sur un îlot mobile porté par un plasmide, l’étude fournit une référence détaillée pour les chercheurs du monde entier. Pour la santé publique, elle met en lumière une voie potentielle par laquelle des traits de résistance puissants pourraient passer de bactéries environnementales inoffensives à des agents pathogènes infectant les humains, les animaux ou les cultures. Pour les sciences de l’environnement et la biotechnologie, elle offre une boîte à outils génétique qui pourrait être exploitée pour nettoyer des sites pollués où s’accumulent antibiotiques ou autres produits chimiques. En termes simples, ce travail montre à la fois à quel point certains microbes de fond sont devenus résistants et donne aux chercheurs les indications nécessaires pour surveiller et gérer cette résistance.
Citation: Liu, Y., Jiang, L., Zhang, J. et al. Complete genome sequence of Sphingomonas sp. gentR, a high-level gentamicin-resistant bacterium. Sci Data 13, 672 (2026). https://doi.org/10.1038/s41597-026-06723-4
Mots-clés: résistance aux antibiotiques, gentamicine, Sphingomonas, génome bactérien, gènes plasmidiques