Clear Sky Science · it
Sequenza completa del genoma di Sphingomonas sp. gentR, un batterio ad alta resistenza alla gentamicina
Perché un microbo di laboratorio conta nella medicina di tutti i giorni
Antibiotici come la gentamicina sono strumenti fondamentali in ospedali e allevamenti, ma i batteri stanno progressivamente imparando a sopravvivere a questi farmaci. Questo studio si concentra su un singolo microbo particolarmente resistente, denominato Sphingomonas sp. gentR, in grado di sopportare dosi massicce di gentamicina. Decodificando l’intero suo progetto genetico, i ricercatori mostrano dove sono nascosti i meccanismi di resistenza e rendono quei dati liberamente disponibili affinché altri possano tracciare, comprendere e forse neutralizzare microrganismi simili prima che le loro difese si trasferiscano a batteri patogeni.
Un microbo resistente trovato in una fiala di antibiotico
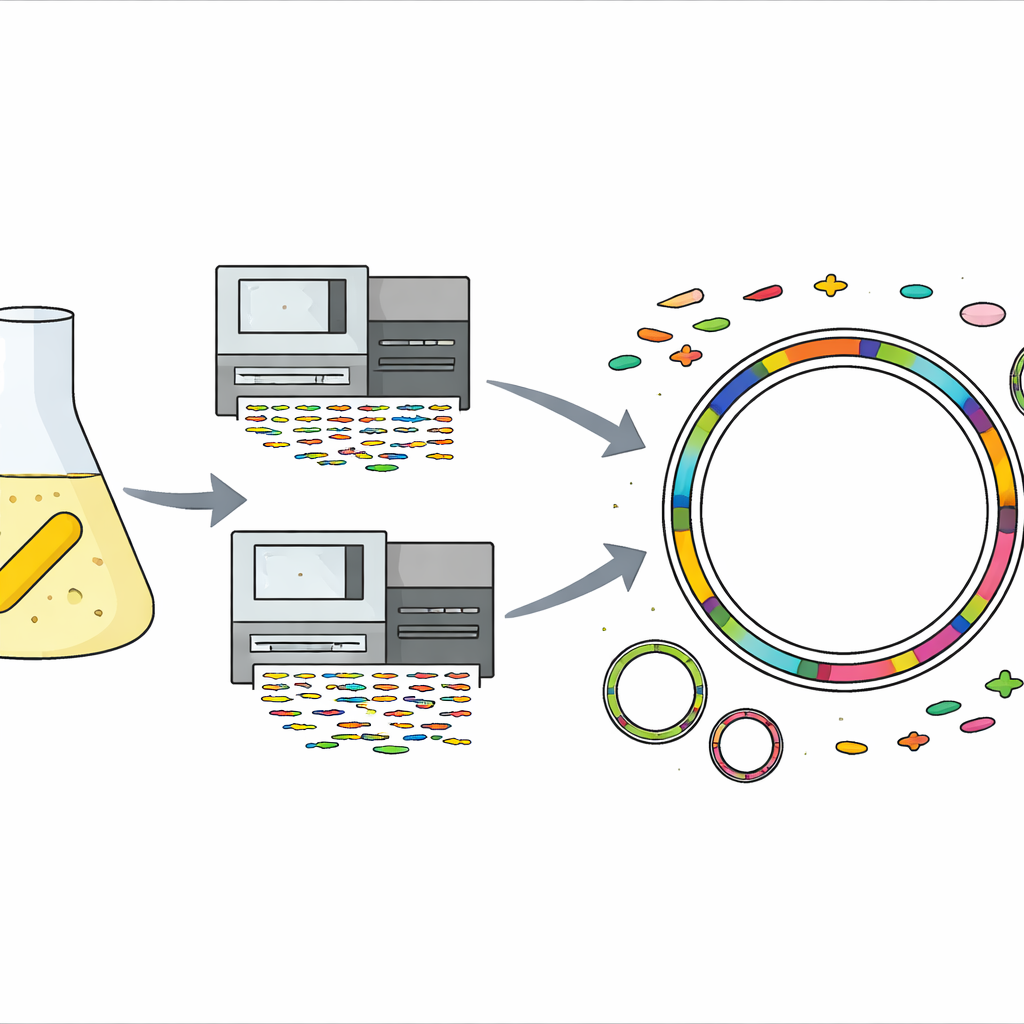
La storia inizia in un laboratorio ordinario, dove una soluzione di lavoro di gentamicina — un antibiotico usato per trattare infezioni gravi — era stata conservata al freddo. Dalla stessa soluzione il team ha inaspettatamente isolato un batterio giallo a forma di bastoncello appartenente al gruppo Sphingomonas. Quando hanno testato la quantità di gentamicina che poteva tollerare, il microbo è cresciuto anche a concentrazioni circa mille volte superiori a quelle che fermano molti altri batteri, segnalandolo come un sopravvissuto estremo. Le specie di Sphingomonas sono già note per vivere in ambienti ostili come sabbie desertiche, ghiaccio glaciale, rocce profonde e persino veicoli spaziali, ma questo livello di resistenza alla gentamicina non era mai stato osservato nel gruppo prima d’ora.
Leggere l’intero manuale di istruzioni del microbo
Per capire cosa rendesse ceppo così resistente, gli scienziati hanno estratto il suo DNA e utilizzato due tecnologie di sequenziamento complementari. Una ha prodotto molti frammenti di DNA brevi e accurati, mentre l’altra ha generato meno frammenti ma molto lunghi. Combinando questi dati, hanno assemblato un genoma completo e senza gap del batterio: un cromosoma circolare principale e due piccoli elementi di DNA circolari chiamati plasmidi. Hanno quindi impiegato una serie di strumenti informatici specializzati e banche dati di riferimento per prevedere i geni, localizzare elementi mobili come virus e isole genomiche, e assegnare probabili funzioni a quasi ogni porzione del genoma, dal metabolismo di base alle risposte allo stress.
Dove si nasconde la resistenza
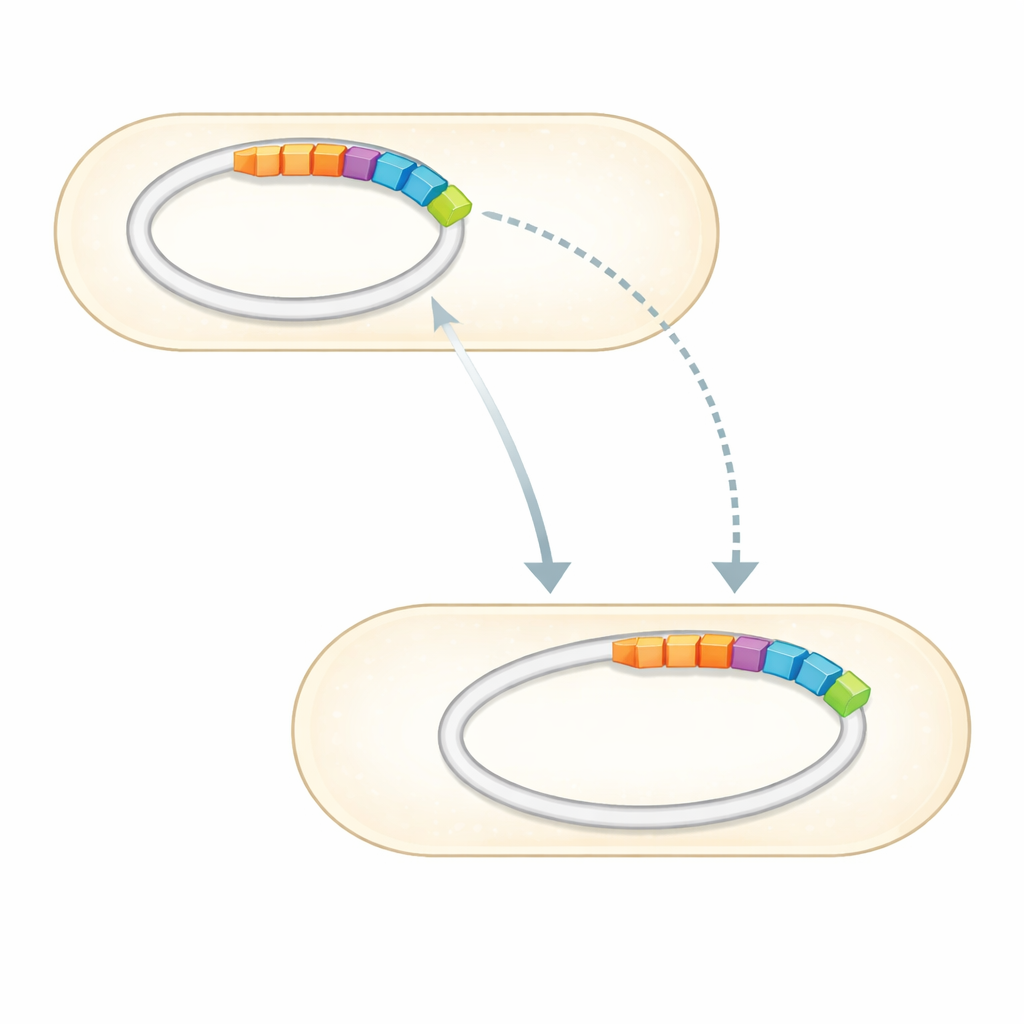
Con il genoma completo a disposizione, il team lo ha confrontato con raccolte curate di geni noti per la resistenza agli antibiotici. Hanno trovato un piccolo insieme di geni chiaramente associati alla resistenza contro diverse classi di farmaci. Più sorprendente, tre geni di resistenza confermati — due che possono inattivare antibiotici aminoglicosidici come gentamicina e streptomicina, e uno che protegge contro i sulfamidici — sono collocati insieme su un tratto di DNA distinto inserito in uno dei plasmidi. Questa regione, nota come isola genomica, è l’equivalente molecolare di un modulo plug-and-play: un cluster di geni che può muoversi tra molecole di DNA e, potenzialmente, tra batteri. Il genoma porta anche molti geni che regolano come la cellula percepisce l’ambiente, espelle composti tossici e mantiene le membrane, tutti fattori che possono rafforzare la sopravvivenza sotto stress antibiotico.
Un kit versatile per vivere in ambienti difficili
Oltre alla resistenza, il catalogo genico dipinge Sphingomonas sp. gentR come un generalista metabolico ben attrezzato per vivere in ambienti poveri o inquinati. Molti dei suoi geni supportano la produzione di energia, l’utilizzo di aminoacidi e la degradazione o il trasporto di molecole diverse, suggerendo che può sfruttare fonti di nutrimento insolite. Altri suggeriscono la capacità di resistere a diversi stress e forse di degradare sostanze chimiche estranee. Questa versatilità spiega perché le specie di Sphingomonas sono esplorate sia come partner benefici per le piante sia come agenti di bonifica per contaminanti industriali, e perché un ceppo individuale potrebbe prosperare in una nicchia ricca di antibiotici come una soluzione farmaceutica.
Cosa significa questo genoma per la salute e l’ambiente
Mappando completamente il DNA di uno ceppo di Sphingomonas eccezionalmente resistente alla gentamicina e collocando i suoi principali geni di resistenza su un’isola mobile presente in un plasmide, lo studio fornisce un riferimento dettagliato per i ricercatori di tutto il mondo. Per la salute pubblica, evidenzia una possibile via attraverso la quale potenti tratti di resistenza potrebbero saltare da batteri ambientali innocui a patogeni che infettano persone, animali o colture. Per le scienze ambientali e la biotecnologia, offre un kit genetico che potrebbe essere sfruttato per ripulire siti contaminati dove si accumulano antibiotici o altre sostanze chimiche. In termini semplici, il lavoro mostra quanto robusti siano diventati alcuni microbi di fondo e fornisce ai ricercatori le istruzioni necessarie per monitorare e gestire questa robustezza.
Citazione: Liu, Y., Jiang, L., Zhang, J. et al. Complete genome sequence of Sphingomonas sp. gentR, a high-level gentamicin-resistant bacterium. Sci Data 13, 672 (2026). https://doi.org/10.1038/s41597-026-06723-4
Parole chiave: resistenza agli antibiotici, gentamicina, Sphingomonas, genoma batterico, geni plasmidici