Clear Sky Science · de
Vollständige Genomsequenz von Sphingomonas sp. gentR, einem hochgradig gentamicinresistenten Bakterium
Warum ein Laborkeim für die alltägliche Medizin wichtig ist
Antibiotika wie Gentamicin sind in Krankenhäusern und in der Landwirtschaft wichtige Wirkstoffe, doch Bakterien lernen nach und nach, wie sie ihnen entkommen. Diese Studie fokussiert auf ein einzelnes, ungewöhnlich robustes Mikroorganismus namens Sphingomonas sp. gentR, das massive Gentamicindosen verkraften kann. Durch die Entschlüsselung seines vollständigen genetischen Bauplans zeigen die Forschenden, wo seine Mechanismen der Wirkstoffresistenz verborgen sind, und stellen diese Daten frei zugänglich zur Verfügung, damit andere ähnliche Keime verfolgen, verstehen und vielleicht neutralisieren können, bevor sich deren Abwehrmechanismen in krankheitserregenden Bakterien ausbreiten.
Ein widerstandsfähiger Keim aus einer Antibiotikaflasche
Die Geschichte beginnt in einem ganz gewöhnlichen Labor, wo eine gebrauchsfertige Lösung von Gentamicin — einem Antibiotikum zur Behandlung schwerer Infektionen — kalt gelagert worden war. Aus genau dieser Lösung isolierte das Team unerwartet ein gelbes, stäbchenförmiges Bakterium aus der Gruppe der Sphingomonas. Als sie testeten, wie viel Gentamicin es aushalten konnte, wuchs der Keim noch bei Konzentrationen, die etwa tausendmal höher liegen als jene, die viele Bakterien stoppen — ein Hinweis auf seine extreme Widerstandsfähigkeit. Sphingomonas-Arten sind bereits dafür bekannt, in rauen Umgebungen zu leben, etwa in Wüstensand, Gletschereis, tiefen Gesteinsschichten und sogar in Raumfahrtmodulen, doch ein derartiges Ausmaß an Gentamicinresistenz war in dieser Gruppe bisher nicht beschrieben.
Das gesamte Bedienungshandbuch des Keims lesen
Um herauszufinden, was diesen Stamm so widerstandsfähig macht, extrahierten die Wissenschaftler seine DNA und nutzten zwei sich ergänzende Sequenzierungstechnologien. Die eine lieferte viele kurze, sehr genaue DNA-Abschnitte, die andere weniger, dafür sehr lange Fragmente. Durch die Kombination dieser Daten assemblierten sie ein vollständiges, lückenfreies Genom des Bakteriums: ein großes zirkuläres Chromosom und zwei kleinere zirkuläre DNA-Elemente, sogenannte Plasmide. Anschließend setzten sie eine Reihe spezialisierter Computerwerkzeuge und Referenzdatenbanken ein, um Gene vorherzusagen, mobile Elemente wie Viren und genomische Inseln zu lokalisieren und nahezu jedem Abschnitt des Genoms wahrscheinliche Funktionen zuzuweisen — von Grundstoffwechsel bis zu Stressantworten.
Wo sich die Resistenz versteckt
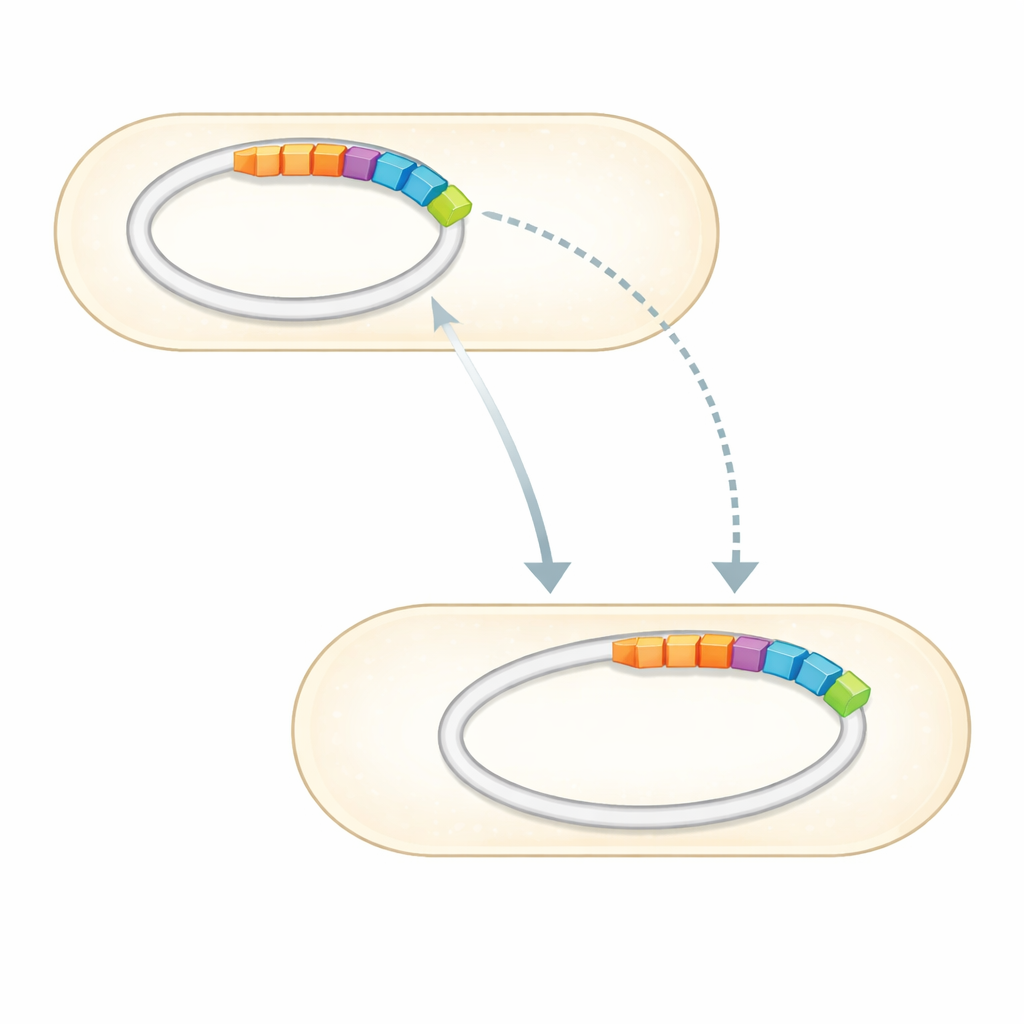
Mit dem vollständigen Genom suchte das Team in kuratierten Sammlungen bekannter Antibiotikaresistenzgene nach Übereinstimmungen. Sie fanden eine kleine Gruppe von Genen, die eindeutig mit Resistenz gegenüber mehreren Wirkstoffklassen verknüpft sind. Am markantesten sind drei bestätigte Resistenzgene — zwei, die Aminoglykosid-Antibiotika wie Gentamicin und Streptomycin inaktivieren können, und eines, das gegen Sulfonamide schützt —, die zusammen auf einem klar abgegrenzten DNA-Abschnitt eines der Plasmide liegen. Diese Region, als genomische Insel bezeichnet, ist das molekulare Gegenstück zu einem Plug-and-Play-Modul: ein Gencluster, das zwischen DNA-Molekülen und potenziell zwischen Bakterien wandern kann. Das Genom enthält außerdem viele Gene, die steuern, wie die Zelle ihre Umgebung wahrnimmt, toxische Verbindungen auspumpt und ihre Membranen aufrechterhält — Eigenschaften, die das Überleben unter Antibiotikastreß stärken können.
Ein vielseitiges Werkzeugset fürs Leben an harten Orten
Über die Resistenz hinaus zeichnet der Genkatalog Sphingomonas sp. gentR als metabolischen Generalisten aus, der gut an Leben in nährstoffarmen oder verschmutzten Umgebungen angepasst ist. Viele seiner Gene unterstützen Energiegewinnung, Aminosäurenutzung und den Abbau beziehungsweise Transport vielfältiger Moleküle, was darauf hindeutet, dass der Stamm ungewöhnliche Nahrungsquellen anzapfen kann. Andere Gene lassen auf die Fähigkeit schließen, verschiedenen Stressfaktoren zu widerstehen und möglicherweise Fremdchemikalien abzubauen. Diese Vielseitigkeit erklärt, warum Sphingomonas-Arten sowohl als pflanzenfreundliche Partner als auch als Aufräumakteure für industrielle Schadstoffe untersucht werden — und warum ein einzelner Stamm in einer antibiotikareichen Nische wie einer Wirkstofflösung gedeihen kann.
Was dieses Genom für Gesundheit und Umwelt bedeutet
Indem die Forschenden die DNA eines außergewöhnlich gentamicinresistenten Sphingomonas-Stamms vollständig kartierten und die Schlüsselfunktionen der Resistenz auf eine mobile Insel auf einem Plasmid abbildeten, liefert die Studie eine detaillierte Referenz für Wissenschaftler weltweit. Für die öffentliche Gesundheit weist sie auf einen möglichen Weg hin, auf dem potente Resistenzmerkmale von harmlosen Umweltbakterien auf Krankheitserreger springen könnten, die Menschen, Tiere oder Nutzpflanzen infizieren. Für Umweltwissenschaft und Biotechnologie bietet sie ein genetisches Werkzeugset, das sich zum Abbau verschmutzter Standorte nutzen ließe, an denen sich Antibiotika oder andere Chemikalien anreichern. Kurz gesagt zeigt die Arbeit, wie widerstandsfähig manche Hintergrundmikroben geworden sind, und gibt Forschenden die notwendigen Informationen, um diese Widerstandsfähigkeit zu überwachen und zu steuern.
Zitation: Liu, Y., Jiang, L., Zhang, J. et al. Complete genome sequence of Sphingomonas sp. gentR, a high-level gentamicin-resistant bacterium. Sci Data 13, 672 (2026). https://doi.org/10.1038/s41597-026-06723-4
Schlüsselwörter: Antibiotikaresistenz, Gentamicin, Sphingomonas, Bakteriengenom, Plasmidgene