Clear Sky Science · es
Secuencia completa del genoma de Sphingomonas sp. gentR, una bacteria con alta resistencia a la gentamicina
Por qué un microbio de laboratorio importa para la medicina cotidiana
Antibióticos como la gentamicina son herramientas fundamentales en hospitales y granjas, pero las bacterias aprenden de forma constante a sobrevivir frente a ellos. Este estudio se centra en un único microbio inusualmente resistente llamado Sphingomonas sp. gentR, capaz de soportar dosis masivas de gentamicina. Al decodificar su plano genético completo, los investigadores revelan dónde se esconden sus trucos de resistencia y ponen esos datos a disposición pública para que otros puedan rastrear, comprender y quizá desactivar microbios similares antes de que sus defensas se propaguen a bacterias patógenas.
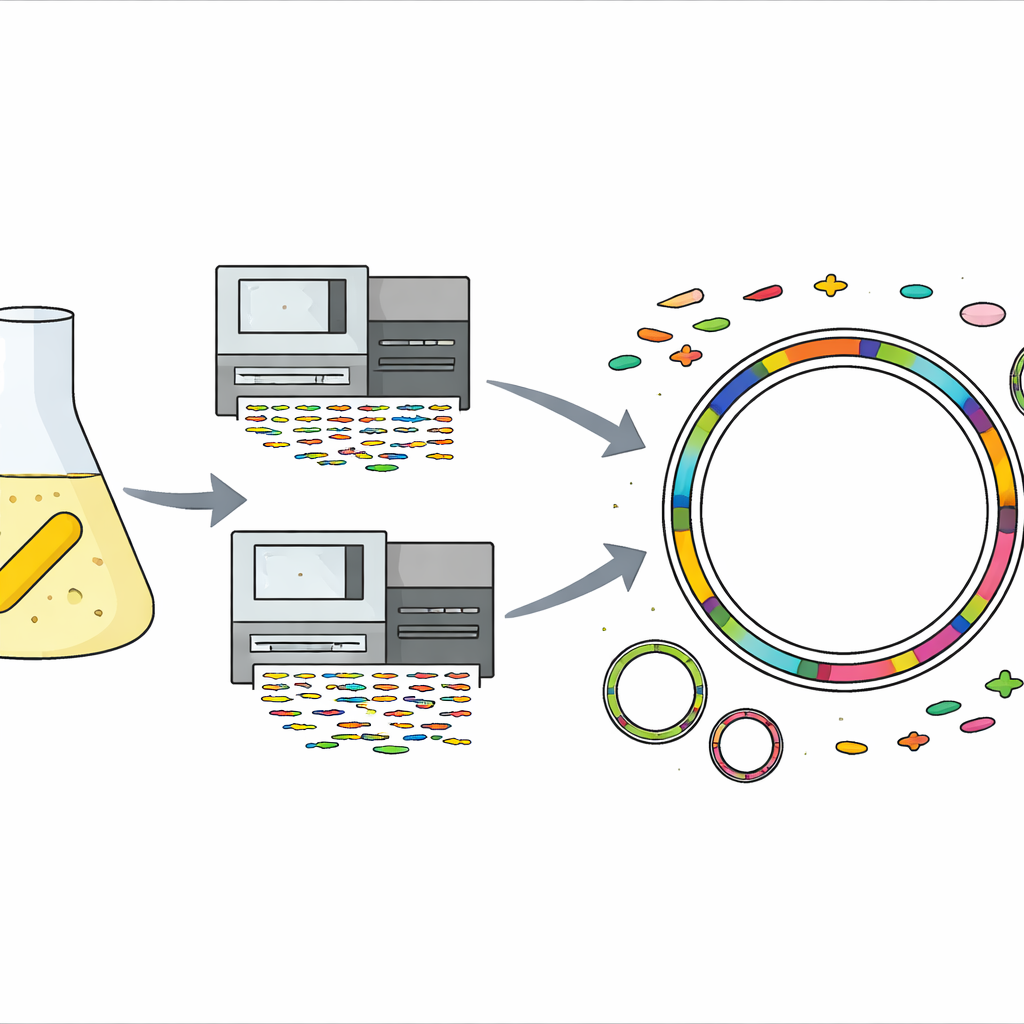
Un microbio resistente procedente de un frasco de antibiótico
La historia comienza en un laboratorio común, donde se había guardado en frío una solución de trabajo de gentamicina —un antibiótico usado para tratar infecciones graves. De esa misma solución, el equipo aisló inesperadamente una bacteria amarilla y con forma de bacilo perteneciente al grupo Sphingomonas. Al probar cuánto gentamicin podía tolerar, el microbio creció incluso a concentraciones alrededor de mil veces superiores a las que detienen a muchas bacterias, lo que lo marca como un superviviente extremo. Las especies de Sphingomonas ya son conocidas por vivir en lugares duros como arenas desérticas, hielos glaciares, rocas profundas y hasta naves espaciales, pero este nivel de resistencia a la gentamicina no se había observado antes en el grupo.
Leer todo el manual de instrucciones del microbio
Para averiguar qué hacía a esta cepa tan resistente, los científicos extrajeron su ADN y usaron dos tecnologías de secuenciación complementarias. Una produjo muchos fragmentos cortos y precisos de ADN, mientras que la otra generó menos fragmentos pero muy largos. Al combinar esos datos, ensamblaron un genoma completo y sin huecos para la bacteria: un cromosoma circular principal y dos piezas circulares de ADN más pequeñas llamadas plásmidos. Luego emplearon un conjunto de herramientas informáticas especializadas y bases de datos de referencia para predecir genes, localizar elementos móviles como virus e islas genómicas, y asignar probables funciones a casi todas las partes del genoma, desde el metabolismo básico hasta las respuestas al estrés.
Dónde se oculta la resistencia
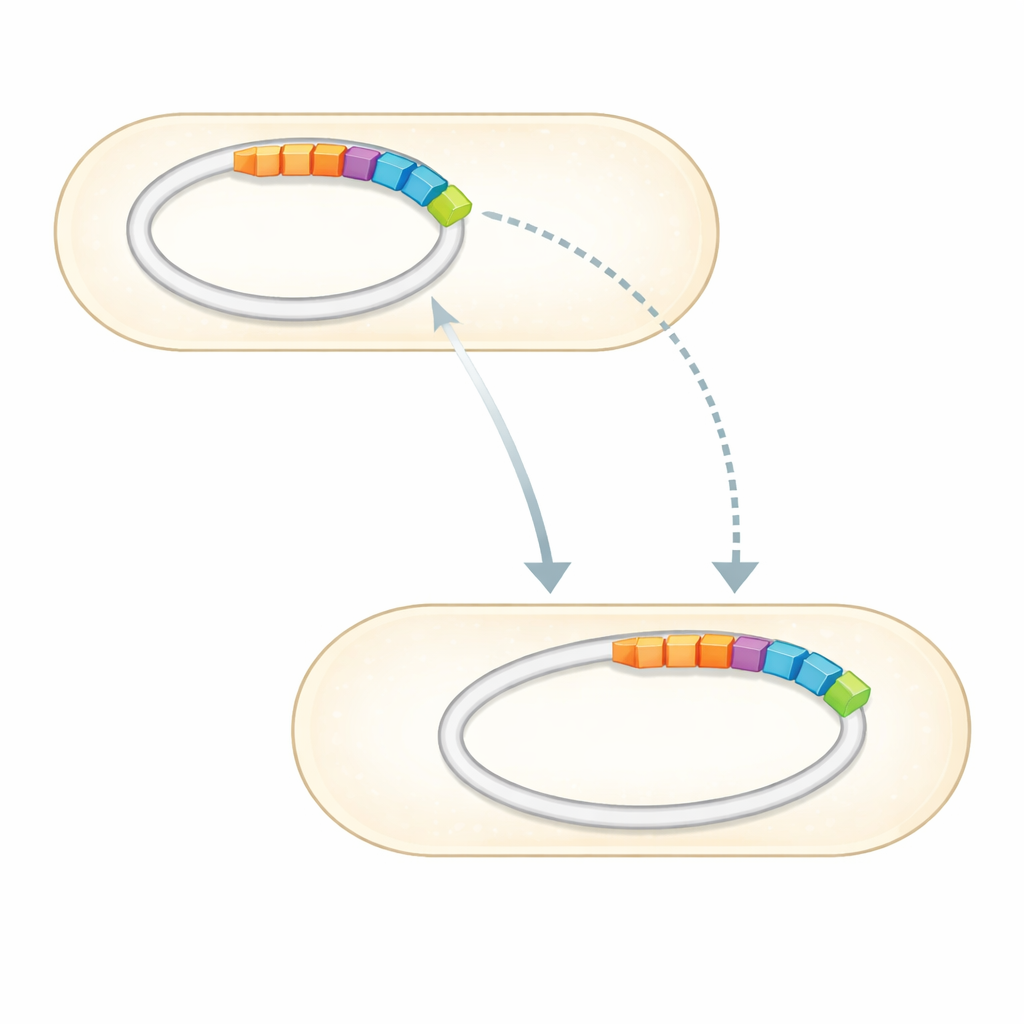
Con el genoma completo en mano, el equipo lo comparó con colecciones curadas de genes de resistencia a antibióticos conocidos. Hallaron un pequeño conjunto de genes claramente asociados con resistencia frente a varias clases de fármacos. Lo más llamativo fue que tres genes de resistencia confirmados —dos que pueden inactivar aminoglucósidos como la gentamicina y la estreptomicina, y uno que protege frente a sulfonamidas— se encuentran juntos en un tramo de ADN distinto incrustado en uno de los plásmidos. Esta región, conocida como isla genómica, es el equivalente molecular de un módulo enchufable: un cúmulo de genes que puede moverse entre moléculas de ADN y, potencialmente, entre bacterias. El genoma también alberga muchos genes que ajustan cómo la célula percibe su entorno, bombea compuestos tóxicos y mantiene sus membranas, todo lo cual puede reforzar la supervivencia bajo estrés por antibióticos.
Un conjunto de herramientas versátil para la vida en entornos duros
Más allá de la propia resistencia, el catálogo genético presenta a Sphingomonas sp. gentR como un generalista metabólico bien adaptado a la vida en ambientes pobres o contaminados. Muchos de sus genes apoyan la producción de energía, el uso de aminoácidos y la degradación o transporte de moléculas diversas, lo que sugiere que puede aprovechar fuentes de alimento inusuales. Otros genes sugieren capacidad para resistir distintos estreses y quizá degradar compuestos extranjeros. Esta versatilidad ayuda a explicar por qué las especies de Sphingomonas se exploran tanto como aliados favorables a las plantas como agentes de limpieza para contaminantes industriales, y por qué una cepa individual podría prosperar en un nicho rico en antibióticos como una solución farmacéutica.
Qué significa este genoma para la salud y el medio ambiente
Al cartografiar completamente el ADN de una cepa de Sphingomonas excepcionalmente resistente a la gentamicina y ubicar sus genes clave de resistencia en una isla móvil sobre un plásmido, el estudio proporciona una referencia detallada para científicos de todo el mundo. Para la salud pública, subraya una vía potencial por la cual rasgos potentes de resistencia podrían saltar de bacterias ambientales inocuas a patógenos que infectan a personas, animales o cultivos. Para la ciencia ambiental y la biotecnología, ofrece un conjunto genético que podría aprovecharse para limpiar sitios contaminados donde se acumulan antibióticos u otros compuestos. En términos sencillos, el trabajo muestra tanto lo resistentes que se han vuelto algunos microbios de fondo como proporciona a los investigadores las instrucciones que necesitan para vigilar y gestionar esa resistencia.
Cita: Liu, Y., Jiang, L., Zhang, J. et al. Complete genome sequence of Sphingomonas sp. gentR, a high-level gentamicin-resistant bacterium. Sci Data 13, 672 (2026). https://doi.org/10.1038/s41597-026-06723-4
Palabras clave: resistencia a antibióticos, gentamicina, Sphingomonas, genoma bacteriano, genes plasmídicos