Clear Sky Science · pl
Warianty dwualleliczne w niekodującym genie RNA RNU4-2 powodują recesywny zespół neurorozwojowy z charakterystycznymi zmianami istoty białej
Dlaczego ta rzadka genetyczna historia ma znaczenie
Większość z nas postrzega geny jako plany budowy białek, ale niektóre geny działają dyskretnie w tle, pomagając komórkom poprawiać przekazy innych genów. Artykuł opisuje nowe dziecięce zaburzenie mózgu spowodowane nie przez uszkodzone białko, lecz przez drobne zmiany w niekodującym genie RNA o nazwie RNU4-2. Śledząc rodziny na całym świecie, badacze pokazują, jak dziedziczne zmiany w tym genie zaburzają okablowanie mózgu, dają rozpoznawalny wzór w rezonansie magnetycznym i różnią się od lepiej znanego, spokrewnionego schorzenia. Praca ilustruje, jak subtelne usterki w maszynerii edycji RNA komórki mogą przekształcić rozwój mózgu — i jak nowe narzędzia genomowe wreszcie ujawniają te ukryte choroby.
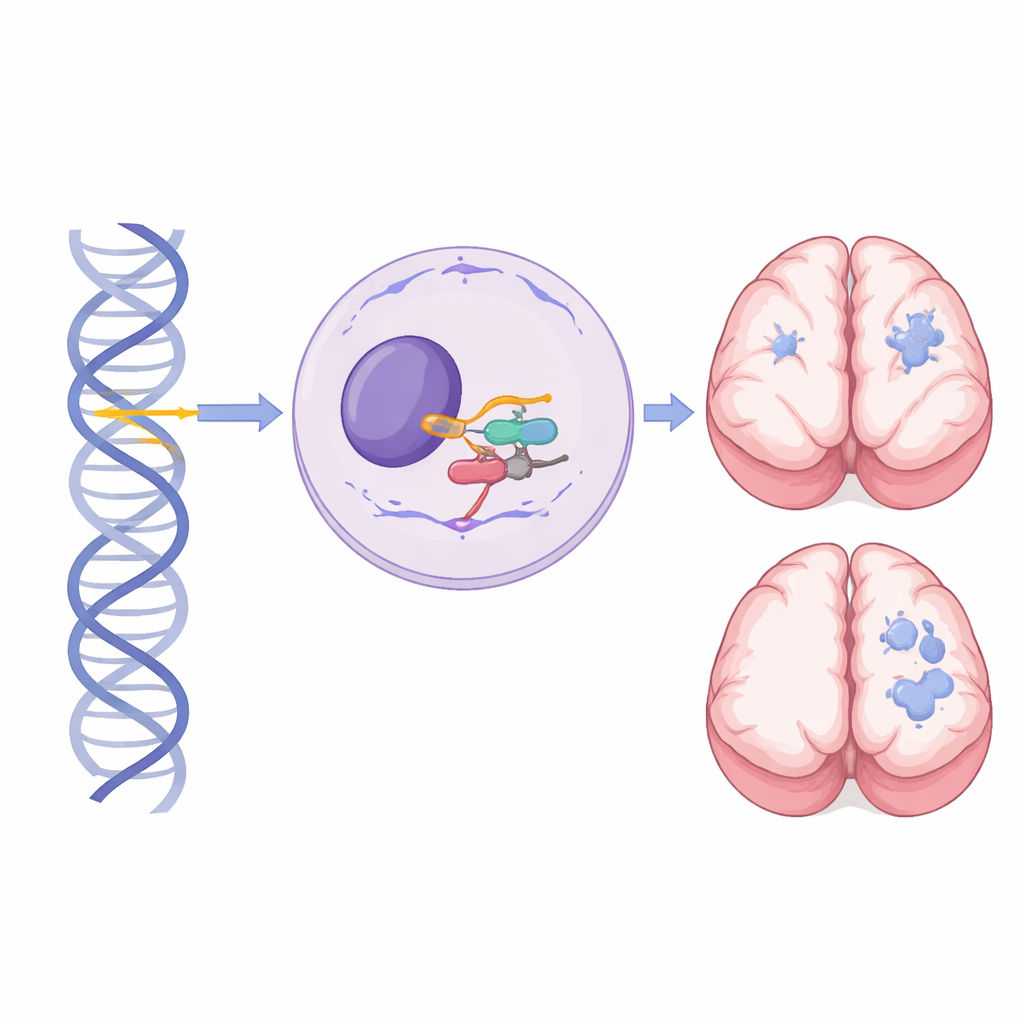
Mały gen o dużej roli w rozwoju mózgu
W każdej komórce znajduje się duża maszyna zwana spliceosomem, która wycina i składa komunikaty RNA, żeby geny mogły być przekształcone w działające cząsteczki. RNU4-2 koduje małe jądrowe RNA U4, kluczowy składnik głównego spliceosomu, który zajmuje się niemal wszystkimi intronami w naszych genach. Wcześniej wykazano, że pojedyncze de novo mutacje w krótkim, centralnym fragmencie RNU4-2 powodują powszechne dominujące zaburzenie neurorozwojowe znane jako zespół ReNU: dziecko choruje nawet wtedy, gdy zmieniona jest tylko jedna kopia genu. W przeciwieństwie do tego, badanie koncentruje się na osobach, które odziedziczyły uszkadzające warianty w obu kopiach RNU4-2 — po jednej od każdego z rodziców — ujawniając odrębny, recesywny zespół.
Odnalezienie rodzin i wspólny obraz kliniczny
Zespół przeszukał duże projekty sekwencjonowania rzadkich chorób i biobanki, aby znaleźć osoby z dwoma wariantami RNU4-2 i problemami neurorozwojowymi. Ostatecznie zidentyfikowano 38 osób z 28 rodzin i zgromadzono szczegółowe dane kliniczne dla 31 z nich. Prawie wszyscy mieli globalne opóźnienie rozwoju lub niepełnosprawność intelektualną, często w zakresie umiarkowanym do ciężkiego, z wyraźnym opóźnieniem mowy; około połowy nie posiadało znaczącego języka mówionego. Wiele dzieci zaczęło chodzić późno, a ponad jedna czwarta nigdy nie chodziła samodzielnie do piątego roku życia. Obniżone napięcie mięśniowe w okresie niemowlęcym, napady padaczkowe, zaburzenia ruchu i koordynacji oraz trudności behawioralne, takie jak agresja czy cechy obsesyjne, były częste. Zmiany skórne, problemy okulistyczne, niski wzrost i anomalie genitalne u chłopców pojawiały się u istotnej mniejszości, tworząc obraz wieloukładowy, a nie chorobę ograniczoną wyłącznie do mózgu.
Badania mózgu ujawniają uderzający wzorzec istoty białej
Rezonans magnetyczny dostarczył jednego z najjaśniejszych wskazówek, że ten recesywny stan różni się od dominującego zespołu ReNU. Wśród 27 osób z badaniami lub opisami obrazów 24 miało nieprawidłowości, a pediatryczny neuroradiolog przeanalizował szczegółowo 13 skanów. Każdy z ocenianych skanów wykazywał zajęcie istoty białej, najcharakterystyczniej poszerzenie wypełnionych płynem przestrzeni otaczających małe naczynia krwionośne (przestrzenie okołonaczyniowe) w głębokiej i okołokomorowej istocie białej. W najcięższych przypadkach przestrzenie te zlewały się w gęsto upakowane skupiska przypominające mikrokosmki, często towarzyszyło temu przerzedzenie spoidła wielkiego i pomniejszenie móżdżku. Ten dramatyczny wzorzec nie był wcześniej opisywany w zespole ReNU i rzadko występował u osób z wariantami RNU4-2 w populacji ogólnej, co czyni go silnym znakiem radiologicznym, który może skłonić do ukierunkowanego badania genetycznego.
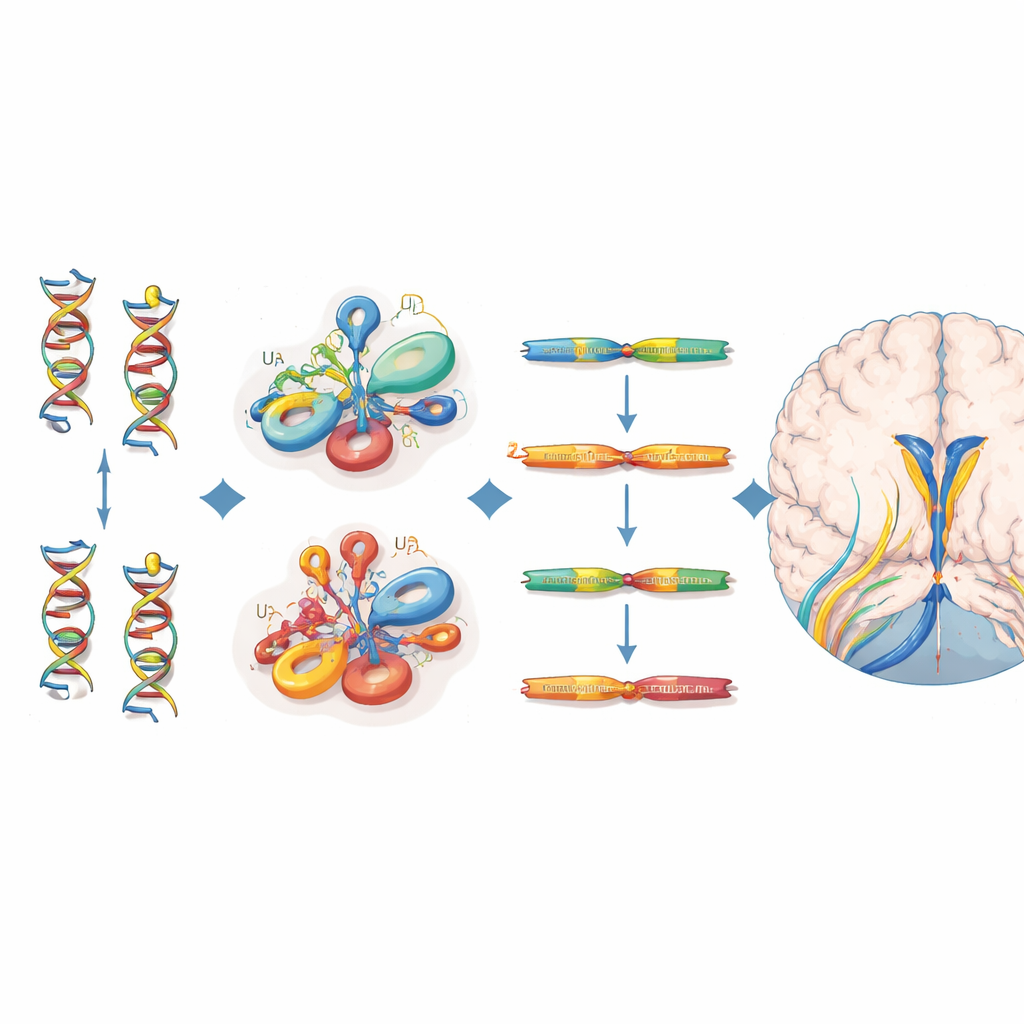
Wskazanie mutacji i ich wpływ molekularny
Wszystkie 38 dotkniętych osób miało warianty dwualleliczne, które skupiały się w określonych obszarach strukturalnych RNA U4 — w szczególności w regionie Stem II wiążącym RNA U6, w ostrym zagięciu zwanym k-turn rekrutującym białka oraz w odcinku niezbędnym do wiązania stabilizujących białek Sm. Wiele z tych pozycji odpowiada równoważnym miejscom w spokrewnionym RNA RNU4ATAC, gdzie mutacje są już znane jako przyczyna innych recesywnych zaburzeń. Aby oszacować szkodliwość poszczególnych wariantów, autorzy sięgnęli po eksperyment saturacyjnego edytowania genomu, który mierzył, jak setki możliwych zmian w RNU4-2 wpływają na przeżywalność komórek. Warianty u pacjentów z chorobą neurorozwojową miały skłonność do niższych wyników funkcji niż te obserwowane u zdrowych ochotników z UK Biobank, co wspiera ich rolę w chorobie, choć nie każdy klinicznie istotny wariant spełniał surowe kryterium w tym komórkowym teście.
Inny mechanizm choroby niż w dominującym zespole spokrewnionym
Analiza danych z sekwencjonowania RNA wykazała, że dzieci z recesywnym schorzeniem RNU4-2 mają wyraźnie obniżone poziomy RNA RNU4-2, wraz z silnym wzrostem pokrewnego RNA RNU4-1. Stosunek RNU4-2 do RNU4-1 był znacznie niższy niż w próbkach tysięcy innych pacjentów i mógł wiarygodnie odróżniać osoby dotknięte, co sugeruje mechanizm utraty funkcji częściowo kompensowany — ale nie w pełni naprawiony — przez kompensacyjny wzrost RNU4-1. Dla kontrastu, osoby z dominującym zespołem ReNU miały faktycznie podwyższone poziomy RNU4-2 i charakterystyczne przesunięcie w wykorzystaniu niektórych miejsc splicingowych, wskazujące na jakościowo inną zaburzenie molekularne. Co istotne, mimo centralnej roli U4 w głównym spliceosomie, zespół nie wykrył szerokiego wzoru zatrzymania intronów obserwowanego w powiązanych zaburzeniach minorowego spliceosomu, co sugeruje subtelniejszy lub tkankowo specyficzny defekt w przetwarzaniu RNA.
Co to oznacza dla rodzin i przyszłych diagnoz
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że badanie definiuje nowe dziedziczne schorzenie mózgu spowodowane posiadaniem dwóch wadliwych kopii małego, niekodującego genu RNA. Dzieci z tym stanem zazwyczaj wykazują znaczne opóźnienie rozwoju, częste napady padaczkowe i charakterystyczny wzorzec zmian istoty białej w MRI, ale klinicznie różnią się od pacjentów z częściej występującym, dominująco działającym zespołem ReNU. Odkrycie rozszerza znany spektrum chorób związanych ze składnikami RNA spliceosomu, podkreśla znaczenie włączania małych genów RNA do paneli badań genetycznych i wskazuje proste biomarkery — takie jak stosunek ekspresji RNU4-2 do RNU4-1 i obecność skrajnego poszerzenia przestrzeni okołonaczyniowych — które mogą pomóc zakończyć długą drogę diagnostyczną dotkniętych rodzin.
Cytowanie: Rius, R., Blakes, A.J.M., Chen, Y. et al. Biallelic variants in the noncoding RNA gene RNU4-2 cause a recessive neurodevelopmental syndrome with distinct white matter changes. Nat Genet 58, 761–773 (2026). https://doi.org/10.1038/s41588-026-02554-6
Słowa kluczowe: zaburzenie neurorozwojowe, spliceosom, niekodujące RNA, zmiany istoty białej, RNU4-2