Clear Sky Science · ar
متغيرات ثنائية الزيجوت في جين الحمض النووي الريبي غير المشفّر RNU4-2 تسبب متلازمة نمائية عصبية متنحية مع تغيّرات مميزة في المادة البيضاء
لماذا تهم هذه القصة الجينية النادرة
يميل معظمنا للتفكير في الجينات كخطط لبناء البروتينات، لكن بعض الجينات تعمل بهدوء خلف الكواليس وتساعد الخلايا على تحرير رسائل جينية أخرى. تكشف هذه الورقة عن اضطراب دماغي طفولي جديد لا ينجم عن بروتين معطوب، بل عن تغيّرات صغيرة في جين حمض نووي ريبوزي غير مشفّر يدعى RNU4-2. ومن خلال متابعة عائلات حول العالم، يُظهر الباحثون كيف أن تغيّرات موروثة في هذا الجين تعطل توصيلات الدماغ وتنتج نمط تصوير بالرنين المغناطيسي يمكن التعرف عليه، وتختلف عن حالة قريبة معروفة أكثر. يوضح العمل كيف أن عيوبًا دقيقة في آلية تحرير الحمض النووي الريبي داخل الخلية يمكن أن تشكّل تطور الدماغ—وكيف بدأت الأدوات الجينومية الجديدة تكشف عن هذه الأمراض الخفية أخيرًا.
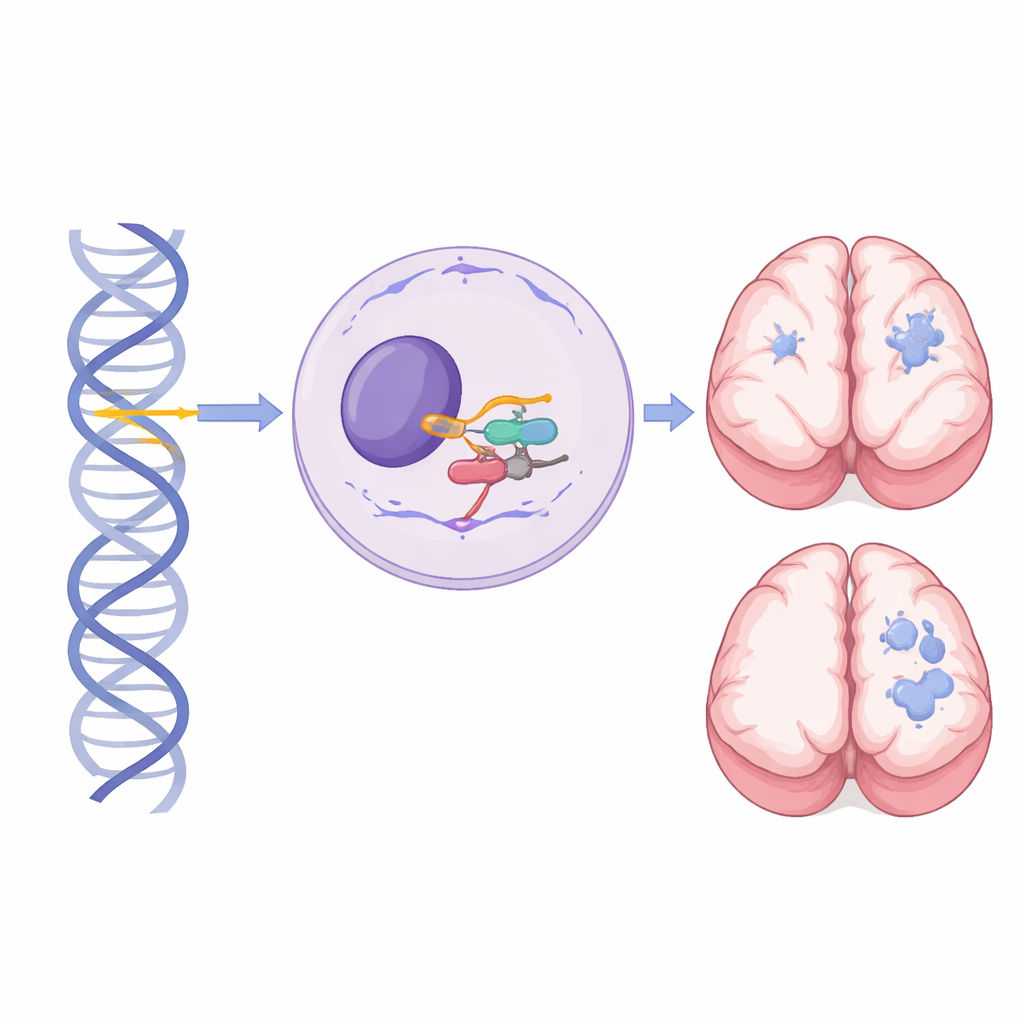
جين صغير له دور كبير في تطور الدماغ
داخل كل خلية، توجد آلة كبيرة تُسمى السبلايسوزوم تقطع وتُلصق رسائل الحمض النووي الريبي بحيث تُترجم الجينات إلى جزيئات عاملة. يشفر RNU4-2 الحمض النووي الريبي الصغير U4، وهو مكوّن حاسم من السبلايسوزوم الرئيسي الذي يتعامل مع معظم الإنترونات في جيناتنا. سابقًا، لوحظ أن طفرات جديدة مفردة في قطعة قصيرة ومركزية من RNU4-2 تسبب حالة نمائية عصبية سائدة شائعة تُعرف بمتلازمة ReNU: إذ يتأثر الطفل حتى لو تغيّر أحد النسختين فقط من الجين. بالمقابل، تركز هذه الدراسة على أشخاص ورثوا متغيرات ضارة في كلتا نسختي RNU4-2—واحدة من كل والد—مما يكشف عن متلازمة متنحية مميزة.
العثور على العائلات وصورة سريرية مشتركة
بحث الفريق في مشاريع تسلسل كبيرة لأمراض نادرة وفي بنوك عينات عن أفراد يحملون متغيرين في RNU4-2 ومشاكل نمائية عصبية. حددوا في النهاية 38 شخصًا من 28 عائلة، وجمعوا بيانات سريرية مفصلة عن 31 منهم. أصيب معظمهم بتأخر نمائي شامل أو إعاقات عقلية، غالبًا ضمن نطاق متوسط إلى شديد، مع تأخر كلامي واضح؛ إذ لم يمتلك حوالي نصفهم لغة منطوقة مجدية. تأخر العديد من الأطفال في المشي، وأكثر من ربعهم لم يمشوا مستقلين بحلول سن الخامسة. كان ضعف توتر العضلات في الرضاعة، والنوبات، ومشاكل الحركة والتنسيق، والتحديات السلوكية مثل العدوان أو السمات القهرية شائعة. ظهرت تغيّرات جلدية ومشاكل عينية وقصر القامة وتشوهات تناسلية لدى الذكور في نسبة كبيرة، مكوّنة صورة متعددة الأجهزة بدلاً من مرض مقصور على الدماغ فقط.
مسوحات الدماغ تكشف بصمة مميزة في المادة البيضاء
قدمت تصويرات الرنين المغناطيسي أحد أوضح الأدلة على أن هذه الحالة المتنحية مختلفة عن متلازمة ReNU السائدة. من بين 27 فردًا لديهم صور أو تقارير، وُجدت شذوذات لدى 24 منهم، وراجع اختصاصي تصوير عصبي أطفال 13 صورة بعمق. أظهرت كل صورة مُراجعة اشتراك المادة البيضاء، وكان أبرزها توسع المساحات المملوءة بالسائل المحيطة بالأوعية الدموية الصغيرة (المساحات المحيطة بالأوعية) في المادة البيضاء العميقة وحول البطينات. في أشد الحالات، تجمعت هذه المساحات لتكوّن عناقيد مضغوطة شبيهة بالميكروسيست، غالبًا مع ترقق الجسم الثفني وانكماش المخيخ. هذا النمط الدرامي لم يُسجّل في متلازمة ReNU ونادرًا ما ظهر لدى أشخاص لديهم متغيرات RNU4-2 من عموم السكان، ما يجعله علامة شعاعية قوية قد تثير إجراء اختبارات جينية مستهدفة.
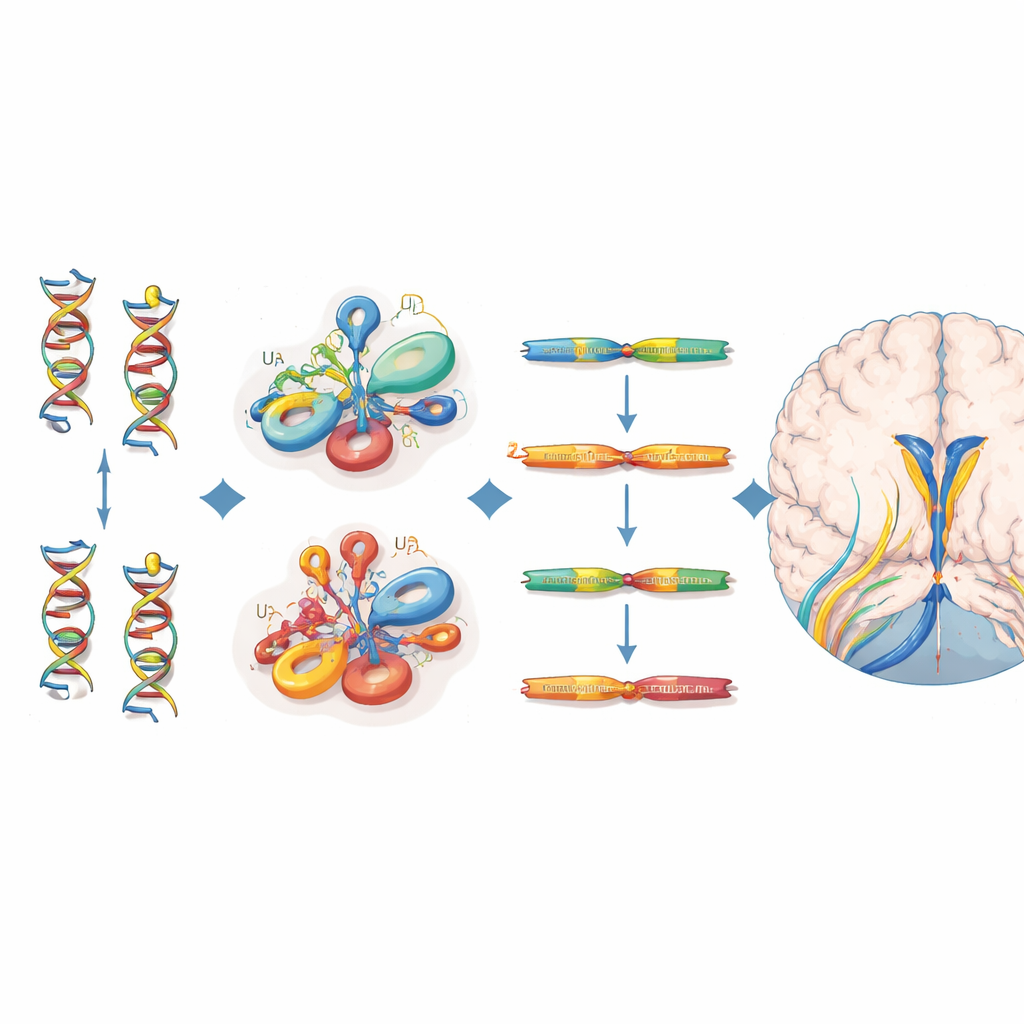
تحديد الطفرات وتأثيرها الجزيئي
حمل جميع الأفراد المصابون الـ38 متغيرات ثنائية الزيجوت تتركز في مناطق بنيوية محددة من حمض U4 الريبي—خاصة منطقة الجذع II التي ترتبط بـU6 RNA، والانثناء الحاد المسمى k-turn الذي يجذب البروتينات، ومقطع مطلوب لارتباط بروتينات Sm المثبِّتة. تتطابق العديد من هذه المواقع مع مواقع معادلة في حمض ريبِي ذي صلة، RNU4ATAC، حيث تُعرف طفرات مسبّبة لاضطرابات متنحيّة أخرى. لتقدير مدى ضرر كل متغير، استعان المؤلفون بتجربة تشـريح جيني تشبّعية قيّمت كيف تؤثر مئات التغيرات الممكنة في RNU4-2 على بقاء الخلايا. مالَت المتغيرات الموجودة عند المرضى ذوي الأمراض النمائية العصبية لأن تكون لها درجات وظيفة أدنى من تلك المرصودة في متطوعين أصحاء من بنك الأنسجة البريطاني، مما يدعم دورها في المرض، رغم أن ليس كل متغير مهم سريريًا تجاوز عتبة صارمة في هذا الاختبار الخلوي.
آلية مرضية مختلفة عن المتلازمة الشقيقة السائدة
من خلال تحليل بيانات تسلسل الحمض النووي الريبي، أظهر الباحثون أن الأطفال المصابين بالحالة المتنحية لـRNU4-2 لديهم مستويات منخفضة بشكل واضح من حمض RNU4-2 الريبي، إلى جانب ارتفاع حاد في حمض مرتبط قريبًا هو RNU4-1. كانت نسبة RNU4-2 إلى RNU4-1 أقل بكثير مما هي عليه في آلاف عينات المرضى الأخرى ويمكن أن تميّز المتأثرين بموثوقية، ما يوحي بآلية فقدان وظيفة يعوضها جزئيًا—لكن ليس بالكامل—تعويض RNU4-1 بزيادة التعبير. بالمقابل، كان لدى أشخاص متلازمة ReNU السائدة مستويات مرتفعة من RNU4-2 وتحول نموذجي في كيفية استخدام مواقع السبلايس، مما يشير إلى اضطراب جزيئي نوعي مختلف. ومن اللافت أنه رغم الدور المركزي لـU4 في السبلايسوزوم الرئيسي، لم يكشف الفريق عن نمط واسع لاحتباس الإنترونات كما يُرى في اضطرابات السبلايسوزوم الصغير ذات الصلة، مما يوحي بعيب أدق أو محدد نسيجًا في معالجة الحمض النووي الريبي.
ماذا يعني هذا للعائلات والتشخيصات المستقبلية
بالنسبة لغير المتخصصين، الرسالة الأساسية أن هذه الدراسة تحدد اضطرابًا دماغيًا وراثيًا جديدًا ناتجًا عن وجود نسختين خاطئتين من جين صغير غير مشفّر للحمض النووي الريبي. عادةً ما يظهر الأطفال المصابون بتأخر نمائي كبير ونوبات متكررة ونمط مميز من تغيرات المادة البيضاء في التصوير بالرنين المغناطيسي، لكنهم سريريًا يختلفون عن مرضى متلازمة ReNU الأكثر شيوعًا ذات السلوك السائد. توسع الاكتشاف الطيف المعروف للأمراض المرتبطة بمكوّنات الحمض النووي الريبي في السبلايسوزوم، ويؤكد أهمية تضمين جينات الحمض النووي الريبي الصغيرة في لوحات الاختبارات الجينية، ويشير إلى علامات حيوية بسيطة—مثل نسبة التعبير بين RNU4-2 وRNU4-1 ووجود توسع شديد للمساحات المحيطة بالأوعية—يمكن أن تساعد في إنهاء رحلة التشخيص للعائلات المتأثرة.
الاستشهاد: Rius, R., Blakes, A.J.M., Chen, Y. et al. Biallelic variants in the noncoding RNA gene RNU4-2 cause a recessive neurodevelopmental syndrome with distinct white matter changes. Nat Genet 58, 761–773 (2026). https://doi.org/10.1038/s41588-026-02554-6
الكلمات المفتاحية: اضطراب نمائي عصبي, السبلايسوزوم, الحمض النووي الريبي غير المشفّر, تغيّرات في المادة البيضاء, RNU4-2