Clear Sky Science · de
Biallelische Varianten im nichtkodierenden RNA-Gen RNU4-2 verursachen ein rezessives neuroentwicklungsbedingtes Syndrom mit charakteristischen Veränderungen der weißen Substanz
Warum diese seltene genetische Geschichte wichtig ist
Die meisten von uns denken bei Genen an Baupläne für Proteine, doch einige Gene wirken im Hintergrund und helfen den Zellen, die Botschaften anderer Gene zu bearbeiten. Diese Arbeit beschreibt eine neue kindliche Hirnstörung, die nicht durch ein defektes Protein, sondern durch kleine Veränderungen in einem nichtkodierenden RNA-Gen namens RNU4-2 verursacht wird. Anhand von Familien aus aller Welt zeigen die Forschenden, wie vererbte Veränderungen in diesem Gen die Gehirnverdrahtung stören, ein wiedererkennbares MRT-Muster hervorrufen und sich von einer bekannteren, verwandten Erkrankung unterscheiden. Die Studie veranschaulicht, wie subtile Defekte in der RNA‑Bearbeitungsmaschinerie der Zelle die Hirnentwicklung umgestalten können — und wie neue genomische Werkzeuge diese verborgenen Krankheiten endlich sichtbar machen.
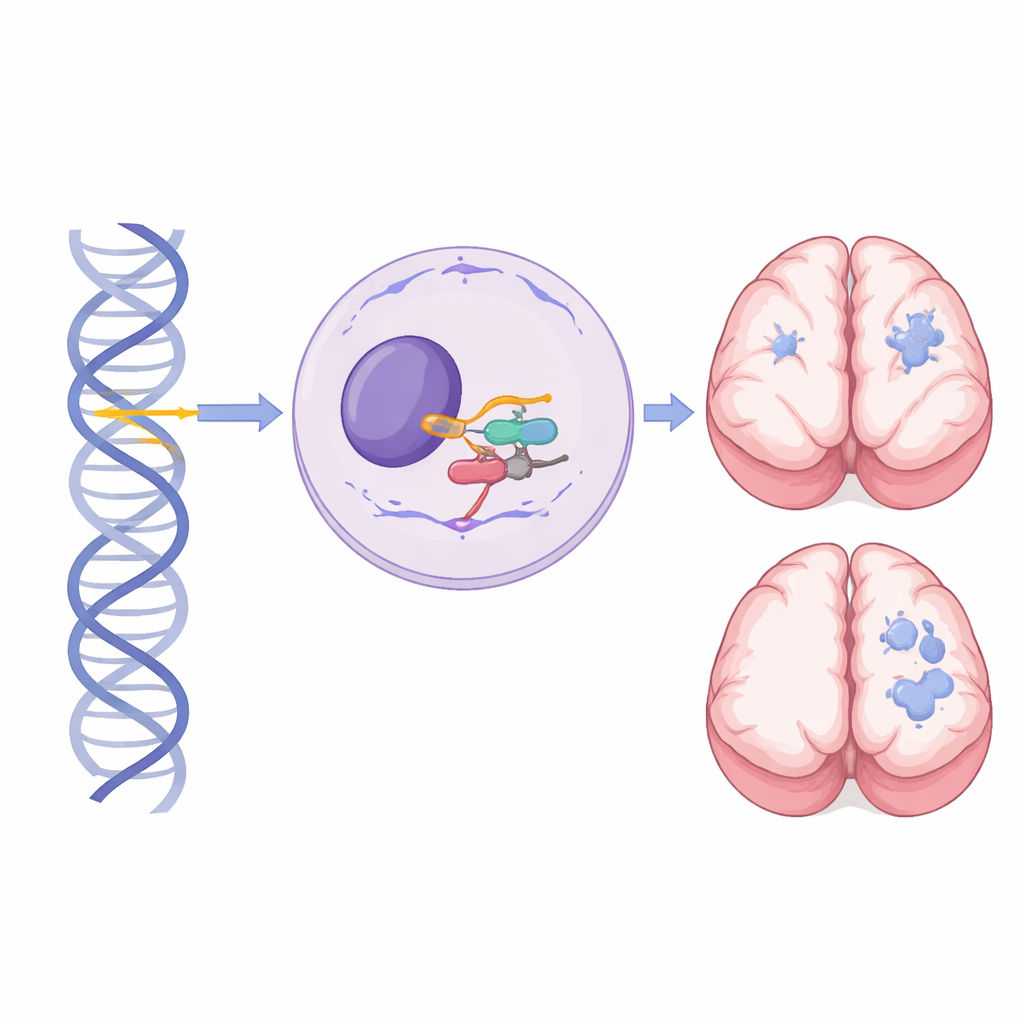
Ein kleines Gen mit großer Rolle in der Hirnentwicklung
In jeder Zelle schneidet und fügt eine große Maschine, das Spliceosom, RNA‑Botschaften so zusammen, dass Gene in funktionelle Moleküle umgesetzt werden können. RNU4-2 kodiert für die U4‑small nuclear RNA, eine kritische Komponente des majoren Spliceosoms, das nahezu alle Introns in unseren Genen bearbeitet. Bisher wurde gezeigt, dass einzelne neu aufgetretene Mutationen in einem kurzen, zentralen Abschnitt von RNU4-2 eine häufige dominante neuroentwicklungsbedingte Erkrankung verursachen, bekannt als ReNU‑Syndrom: Ein Kind ist betroffen, selbst wenn nur eine Kopie des Gens verändert ist. Diese Studie hingegen konzentriert sich auf Personen, die schädigende Varianten in beiden Kopien von RNU4-2 geerbt haben — je eine von jedem Elternteil — und zeigt ein eigenständiges, rezessives Syndrom.
Familien finden und ein gemeinsames klinisches Bild
Das Team durchsuchte große Sequenzierungsprojekte für seltene Krankheiten und Biobanken, um Personen mit zwei RNU4-2‑Varianten und neuroentwicklungsbedenken zu finden. Letztlich identifizierten sie 38 Personen aus 28 Familien und sammelten für 31 davon detaillierte klinische Daten. Fast alle zeigten globale Entwicklungsverzögerung oder intellektuelle Beeinträchtigung, häufig im mäßigen bis schweren Bereich, mit ausgeprägter Sprachverzögerung; etwa die Hälfte verfügte über keine aussagekräftige gesprochene Sprache. Viele Kinder gingen spät sprechen, und mehr als ein Viertel konnte bis zum Alter von fünf Jahren nie unabhängig laufen. Niedriger Muskeltonus in der Säuglingszeit, Anfälle, Bewegungs‑ und Koordinationsstörungen sowie Verhaltensauffälligkeiten wie Aggression oder zwanghafte Züge waren häufig. Hautveränderungen, Augenprobleme, Kleinwuchs und Genitalanomalien bei Jungen traten bei einer beträchtlichen Minderheit auf und ergaben damit eher ein multisystemisches Bild als eine ausschließlich auf das Gehirn beschränkte Erkrankung.
Hirnscans zeigen ein auffälliges Muster in der weißen Substanz
Die Magnetresonanztomografie lieferte einen der klarsten Hinweise darauf, dass diese rezessive Erkrankung vom dominanten ReNU‑Syndrom zu unterscheiden ist. Von 27 Personen mit Scans oder Berichten wiesen 24 Auffälligkeiten auf, und ein pädiatrischer Neuroradiologe begutachtete 13 Scans eingehend. Jeder geprüfte Scan zeigte Beteiligung der weißen Substanz, am charakteristischsten eine Erweiterung der flüssigkeitsgefüllten Räume, die kleine Blutgefäße umgeben (perivaskuläre Räume) in der tiefen und periventrikulären weißen Substanz. In den schwersten Fällen verschmolzen diese Räume zu dicht gepackten, mikrozystenähnlichen Clustern, häufig begleitet von Ausdünnung des Corpus callosum und Schrumpfung des Kleinhirns. Dieses dramatische Muster war beim ReNU‑Syndrom nicht beschrieben worden und wurde bei Personen mit RNU4-2‑Varianten aus der Allgemeinbevölkerung selten gesehen, wodurch es zu einem starken radiologischen Merkmal wird, das gezielte genetische Tests auslösen kann.
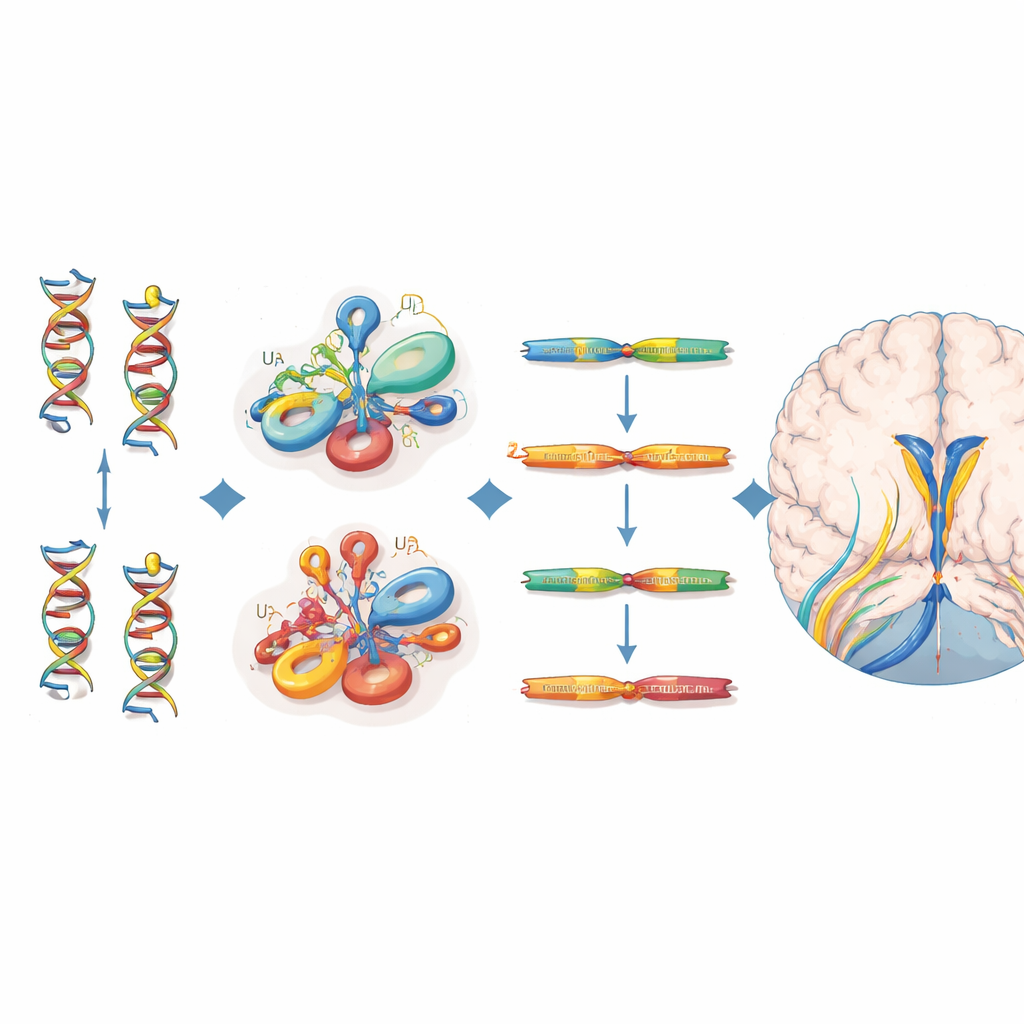
Die Mutationen lokalisieren und ihre molekulare Wirkung
Alle 38 betroffenen Personen trugen biallelische Varianten, die in bestimmten strukturellen Regionen der U4‑RNA gehäuft auftraten — insbesondere in der Stem‑II‑Region, die an die U6‑RNA bindet, in einer scharfen Biegung namens k‑turn, die Proteine anzieht, und in einem Abschnitt, der für die Bindung stabilisierender Sm‑Proteine erforderlich ist. Viele dieser Positionen entsprechen äquivalenten Stellen in einer verwandten RNA, RNU4ATAC, in der bereits Mutationen bekannt sind, die andere rezessive Erkrankungen verursachen. Um einzuschätzen, wie schädlich jede Variante ist, griffen die Autorinnen und Autoren auf ein Saturation‑Genome‑Editing‑Experiment zurück, das gemessen hatte, wie Hunderte möglicher RNU4-2‑Veränderungen das Überleben von Zellen beeinflussen. Varianten bei Patientinnen und Patienten mit neuroentwicklungsbedingter Erkrankung zeigten tendenziell niedrigere Funktionswerte als jene aus gesunden Proben des UK Biobank, was ihre Rolle bei der Krankheit stützt, obwohl nicht jede klinisch relevante Variante in diesem zellbasierten Test einen strikten Grenzwert überschritt.
Anderer Krankheitsmechanismus als beim dominanten Schwester‑Syndrom
Durch Analyse von RNA‑Sequenzierungsdaten zeigten die Forschenden, dass Kinder mit der rezessiven RNU4-2‑Erkrankung deutlich reduzierte Mengen an RNU4-2‑RNA aufwiesen, einhergehend mit einem starken Anstieg einer eng verwandten RNA, RNU4-1. Das Verhältnis von RNU4-2 zu RNU4-1 war deutlich niedriger als in Tausenden anderen Patientenproben und konnte betroffene Personen zuverlässig unterscheiden, was auf einen Loss‑of‑Function‑Mechanismus hindeutet, der teilweise — aber nicht vollständig — durch eine Hochregulation von RNU4-1 kompensiert wird. Im Gegensatz dazu hatten Personen mit dem dominanten ReNU‑Syndrom tatsächlich erhöhte RNU4-2‑Spiegel und eine charakteristische Verschiebung in der Nutzung bestimmter Spleißstellen, was auf eine qualitativ andere molekulare Störung hinweist. Bemerkenswert ist, dass das Team, trotz der zentralen Rolle von U4 im majoren Spliceosom, nicht das ausgeprägte Intron‑Retention‑Muster detektierte, das bei verwandten Störungen des minoren Spliceosoms beobachtet wird, was auf einen subtileren oder gewebespezifischen Defekt in der RNA‑Verarbeitung schließen lässt.
Was das für Familien und künftige Diagnosen bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft, dass diese Studie eine neue erbliche Hirnerkrankung definiert, die durch zwei fehlerhafte Kopien eines kleinen, nichtkodierenden RNA‑Gens verursacht wird. Kinder mit dieser Erkrankung zeigen typischerweise deutliche Entwicklungsverzögerung, häufig Anfälle und ein charakteristisches Muster von Veränderungen der weißen Substanz im MRT, unterscheiden sich jedoch klinisch von Patientinnen und Patienten mit dem häufiger auftretenden, dominant wirkenden ReNU‑Syndrom. Die Entdeckung erweitert das bekannte Spektrum von Erkrankungen, die mit den RNA‑Komponenten des Spliceosoms verknüpft sind, unterstreicht die Bedeutung, kleine RNA‑Gene in genetischen Testpanels mit aufzunehmen, und weist auf einfache Biomarker hin — wie das RNU4-2‑zu‑RNU4-1‑Expressionsverhältnis und das Vorhandensein einer ausgeprägten Erweiterung der perivaskulären Räume — die Familien helfen können, die diagnostische Odyssee zu beenden.
Zitation: Rius, R., Blakes, A.J.M., Chen, Y. et al. Biallelic variants in the noncoding RNA gene RNU4-2 cause a recessive neurodevelopmental syndrome with distinct white matter changes. Nat Genet 58, 761–773 (2026). https://doi.org/10.1038/s41588-026-02554-6
Schlüsselwörter: neuroentwicklungsstörung, Spliceosom, nichtkodierende RNA, Veränderungen der weißen Substanz, RNU4-2