Clear Sky Science · ja
非コードRNA遺伝子RNU4-2の両アレル変異は、特徴的な白質変化を伴う常染色体劣性の神経発達症候群を引き起こす
なぜこの稀な遺伝学的報告が重要なのか
多くの人は遺伝子をタンパク質の設計図と考えますが、一部の遺伝子は静かに裏方で働き、細胞が他の遺伝子のメッセージを編集するのを助けます。本論文は、壊れたタンパク質ではなく、RNU4-2と呼ばれる非コードRNA遺伝子の小さな変化によって引き起こされる新しい小児脳疾患を明らかにしています。世界中の家系を追跡することで、研究者たちはこの遺伝子の遺伝的変化が脳の配線を乱し、識別可能なMRIパターンを生み、よりよく知られた関連疾患とは異なることを示しました。この研究は、細胞のRNA編集機構における微妙な不具合が脳発達を如何に変えるか、そして新しいゲノム解析ツールがこれらの隠れた疾患をついに明らかにし始めていることを示しています。
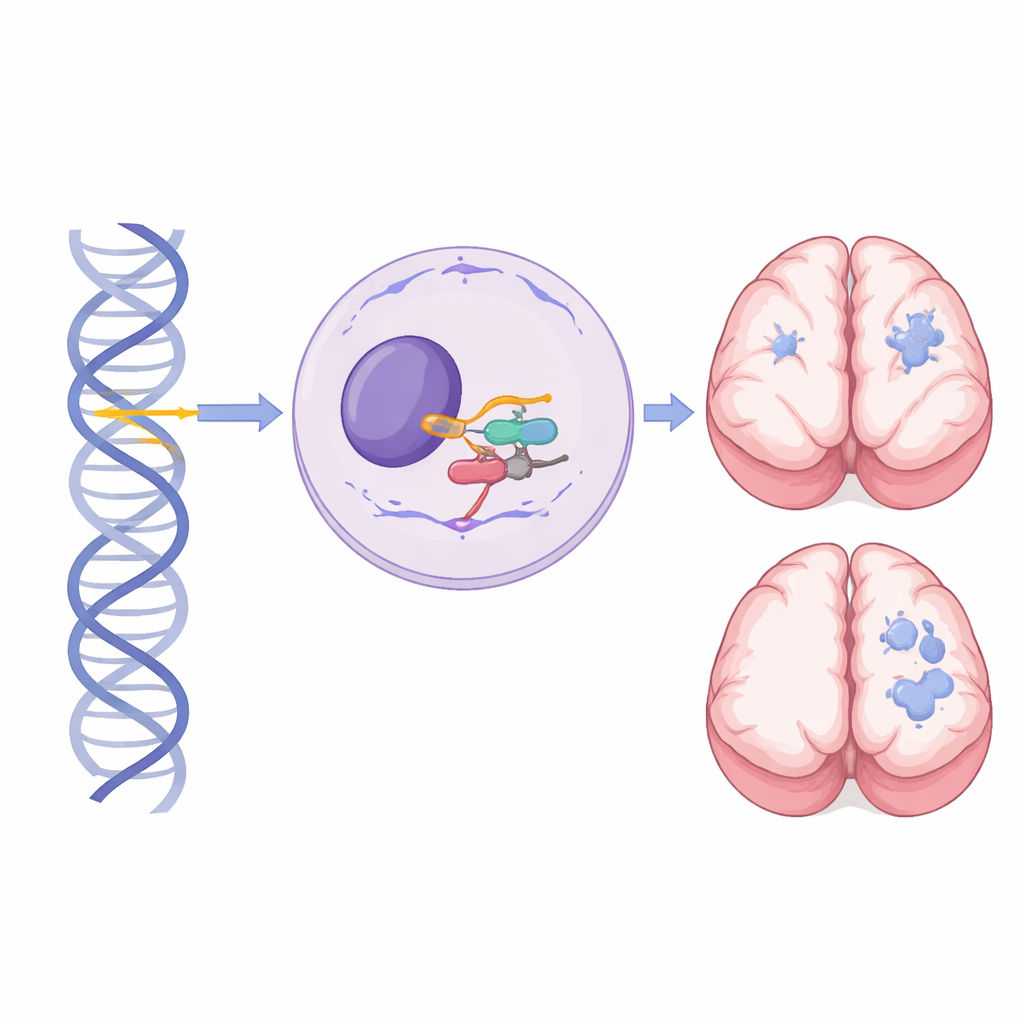
脳発達で大きな役割を果たす小さな遺伝子
すべての細胞内にはスプライソソームと呼ばれる大きな機械があり、RNAメッセージを切り貼りして遺伝子を機能分子に変換できるようにしています。RNU4-2は主要スプライソソームの重要な構成要素であるU4小核RNAをコードします。主要スプライソソームは遺伝子内のほとんどのイントロンを扱います。これまでに、RNU4-2の短く中心的な領域の新規変異が優性の神経発達症状、いわゆるReNU症候群を引き起こすことが示されていました:つまり、遺伝子の片方だけが変化していても発症します。対照的に、本研究は両親から一つずつ受け継いだRNU4-2の損傷性変異(二アレル変異)を持つ人々に焦点を当て、別個の劣性症候群を明らかにしています。
家系の探索と共有される臨床像の把握
研究チームは、大規模な希少疾患シーケンスプロジェクトやバイオバンクを検索して、RNU4-2に二つの変異を持ち神経発達の問題を有する個人を探しました。最終的に28家系から38名を同定し、そのうち31名について詳細な臨床データを収集しました。ほぼ全員が全般的な発達遅滞または知的障害を有し、しばしば中等度から重度で、顕著な発語遅延がみられました;約半数は有意な発語を示しませんでした。多くの子どもが歩行開始が遅く、5歳までに独立歩行に至らない者が4分の1を超えました。乳児期の低筋緊張、てんかん、運動・協調障害、攻撃性や強迫的傾向などの行動上の課題も共通していました。皮膚変化、眼の問題、低身長、男性の生殖器異常はかなりの割合で見られ、純粋に脳に限局した疾患ではなく多系統性の表現型を形成していました。
脳画像が示す顕著な白質の特徴
磁気共鳴画像(MRI)は、この劣性疾患が優性のReNU症候群と異なることを示す最も明瞭な手がかりの一つを提供しました。スキャンまたは所見がある27名のうち24名に異常があり、小児神経放射線科医が13例の画像を詳細に再検討しました。再検討された全例で白質の関与が確認され、最も特徴的なのは深部および脳室周囲白質における小血管を取り巻く液体で満たされた空間(脳血管周囲腔)の拡張でした。重症例では、これらの空間が微小嚢胞のような密に詰まったクラスターに融合し、しばしば脳梁の薄化や小脳の萎縮を伴っていました。この劇的なパターンはReNU症候群では報告されておらず、一般集団におけるRNU4-2変異保有者でも稀であったため、標的遺伝子検査を促す強力な放射線学的指標となります。
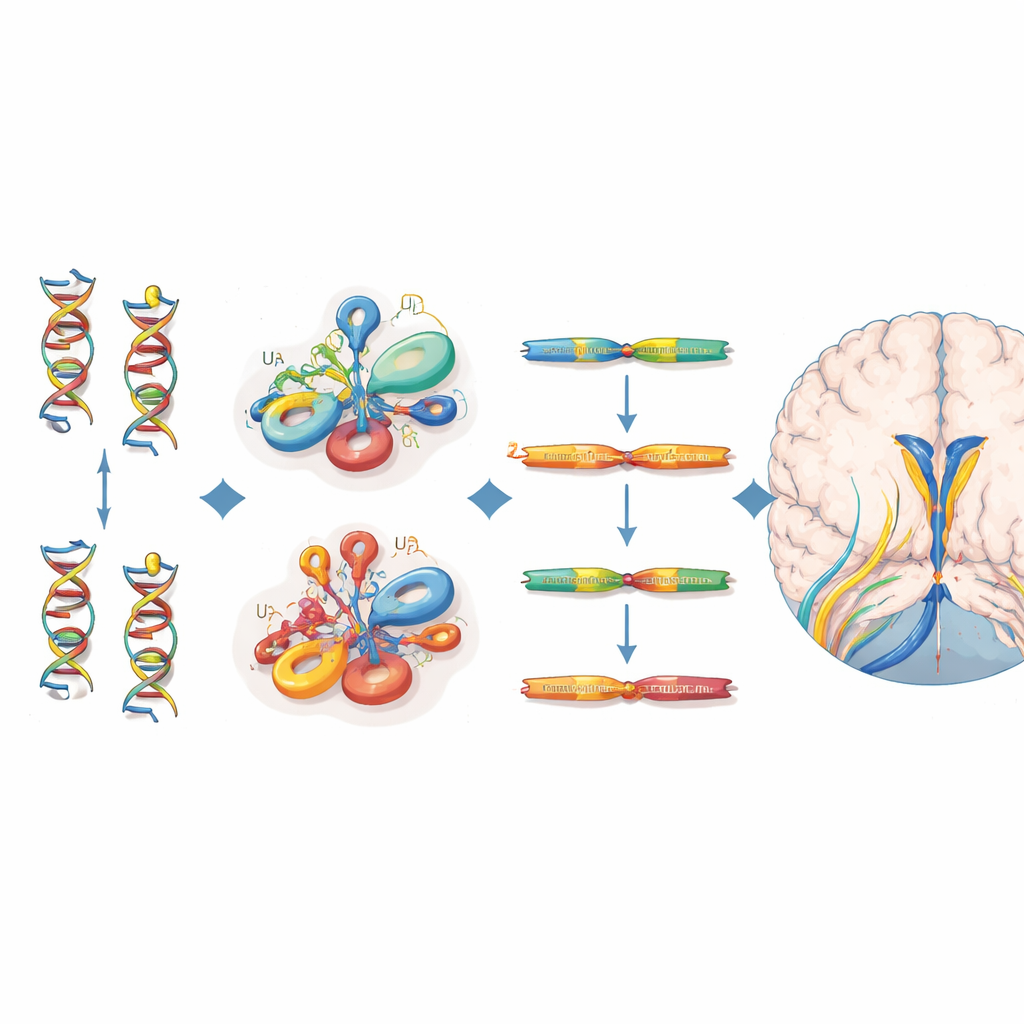
変異の特定と分子への影響の解明
影響を受けた38名はいずれもU4 RNAの特定の構造領域にクラスターする両アレル変異を持っており、特にU6 RNAと結合するStem II領域、タンパク質を呼び寄せる鋭い曲がりであるk-turn、Smタンパク質の安定化に必要な配列に集中していました。これらの多くの位置は、既に他の劣性疾患を引き起こすことが知られている関連RNAであるRNU4ATACの同等部位と一致します。各変異の有害性を評価するために、著者らは数百の可能なRNU4-2変化が細胞生存に与える影響を測定したサチュレーションゲノム編集実験のデータを利用しました。神経発達疾患の患者に見られた変異は、英国バイオバンクの健常例で観察された変異よりも機能スコアが低い傾向があり、臨床における役割を支持しましたが、すべての臨床的に重要な変異がこの細胞ベースのアッセイで厳格なカットオフを満たすわけではありませんでした。
優性の姉妹疾患とは異なる病因
RNAシーケンシングデータを解析することで、研究者たちは劣性RNU4-2症例の子どもたちがRNU4-2 RNAレベルの著しい低下と、密接に関連するRNU4-1 RNAの顕著な増加を示すことを示しました。RNU4-2とRNU4-1の比率は、他の何千もの患者サンプルと比べて著しく低く、影響を受けた個人を確実に識別できることから、部分的にRNU4-1の上方制御で相殺されるが完全には回復しない機能喪失機序を示唆します。対照的に、優性のReNU症候群の患者は実際にRNU4-2レベルの増加と特定のスプライス部位の使用における特徴的な変化を示し、質的に異なる分子障害を示していました。注目すべきは、主要スプライソソームにおけるU4の中心的役割にもかかわらず、研究チームはマイナースプライソソームの関連疾患で見られるような広範なイントロン保持パターンを検出せず、RNA処理におけるより微妙または組織特異的な欠陥を示唆したことです。
家族や将来の診断にとっての意義
専門外の方への要点は、この研究が小さな非コードRNA遺伝子の二つの欠陥コピーを持つことによって生じる新たな遺伝性脳疾患を定義したことです。この状態の子どもたちは通常、著しい発達遅滞、頻繁なてんかん発作、MRI上の特徴的な白質変化を示しますが、より一般的で優性に作用するReNU症候群の患者とは臨床的に区別されます。本発見はスプライソソームのRNA構成要素に結び付く疾患スペクトルを拡大し、小さなRNA遺伝子を遺伝子検査パネルに含める重要性を強調するとともに、RNU4-2対RNU4-1の発現比や極端な脳血管周囲腔拡張の存在といった単純なバイオマーカーが、影響を受けた家族の診断難航を終わらせる手助けになることを示しています。
引用: Rius, R., Blakes, A.J.M., Chen, Y. et al. Biallelic variants in the noncoding RNA gene RNU4-2 cause a recessive neurodevelopmental syndrome with distinct white matter changes. Nat Genet 58, 761–773 (2026). https://doi.org/10.1038/s41588-026-02554-6
キーワード: 神経発達障害, スプライソソーム, 非コードRNA, 白質変化, RNU4-2