Clear Sky Science · es
Variantes bialélicas en el gen de ARN no codificante RNU4-2 causan un síndrome neurodesarrollativo recessivo con cambios distintivos en la sustancia blanca
Por qué importa esta rara historia genética
La mayoría de nosotros pensamos en los genes como planos para fabricar proteínas, pero algunos genes funcionan en segundo plano, ayudando a las células a editar los mensajes de otros genes. Este artículo descubre un nuevo trastorno cerebral infantil causado no por una proteína defectuosa, sino por pequeños cambios en un gen de ARN no codificante llamado RNU4-2. Siguiendo familias de todo el mundo, los investigadores muestran cómo variantes heredadas en este gen alteran el cableado cerebral, producen un patrón reconocible en la resonancia magnética y difieren de una enfermedad relacionada y mejor conocida. El trabajo ilustra cómo fallos sutiles en la maquinaria de edición del ARN celular pueden remodelar el desarrollo cerebral, y cómo las nuevas herramientas genómicas están por fin revelando estas enfermedades ocultas.
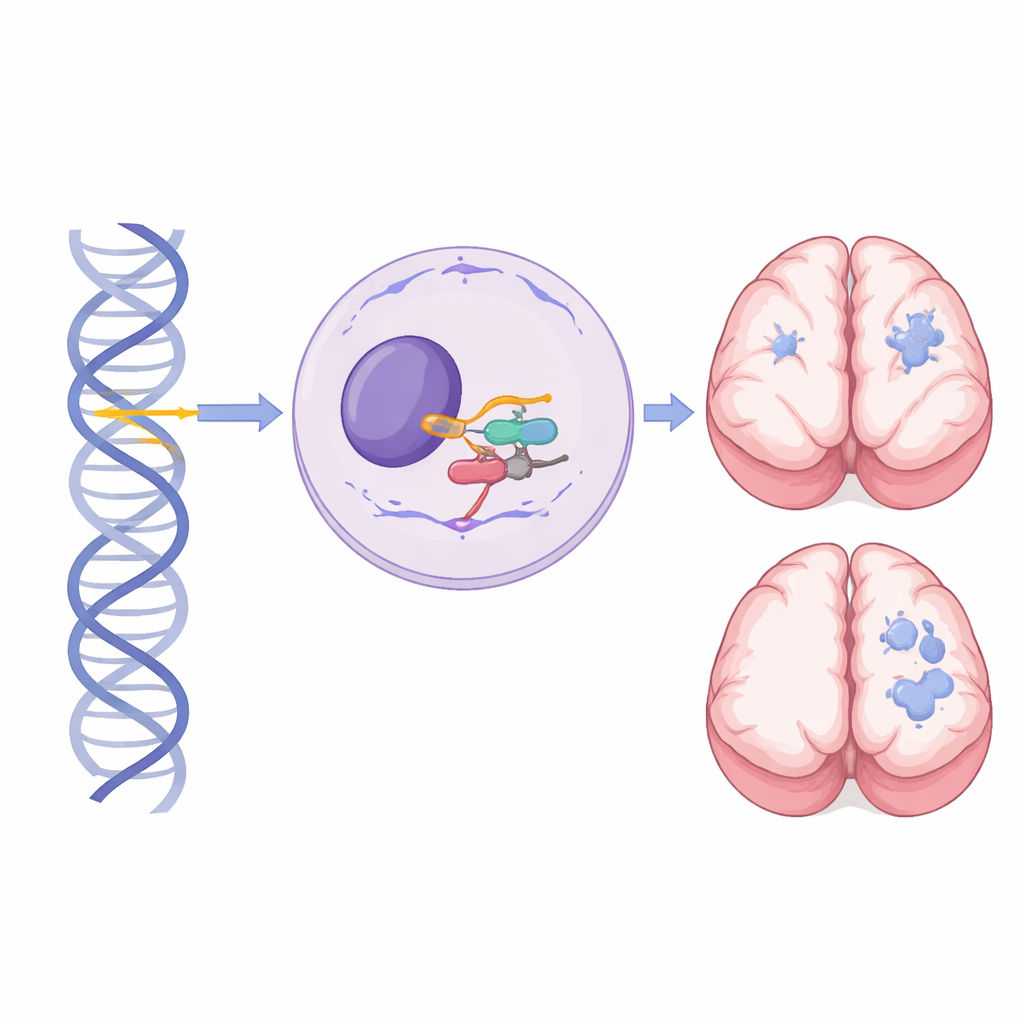
Un gen pequeño con un gran papel en el desarrollo cerebral
Dentro de cada célula, una gran máquina llamada espliceosoma corta y pega mensajes de ARN para que los genes puedan convertirse en moléculas funcionales. RNU4-2 codifica el ARN nuclear pequeño U4, un componente crítico del espliceosoma mayor, que procesa casi todos los intrones de nuestros genes. Anteriormente se demostró que mutaciones de novo en un tramo corto y central de RNU4-2 causan una condición neurodesarrollativa dominante común conocida como síndrome ReNU: un niño se afecta incluso si sólo una copia del gen está alterada. En contraste, este estudio se centra en personas que heredaron variantes dañinas en ambas copias de RNU4-2—una de cada progenitor—revelando un síndrome recesivo y distinto.
Encontrar familias y un cuadro clínico compartido
El equipo buscó en grandes proyectos de secuenciación de enfermedades raras y biobancos para encontrar individuos con dos variantes de RNU4-2 y problemas del neurodesarrollo. Finalmente identificaron a 38 personas de 28 familias y recopilaron datos clínicos detallados de 31 de ellas. Casi todos presentaron retraso global del desarrollo o discapacidad intelectual, a menudo en el rango moderado a grave, con un marcado retraso del habla; alrededor de la mitad no desarrolló lenguaje hablado significativo. Muchos niños caminaron tarde, y más de una cuarta parte nunca caminaron de forma independiente a los cinco años. Era frecuente la hipotonía en la infancia, convulsiones, problemas de movimiento y coordinación, y dificultades conductuales como agresión o rasgos obsesivos. Cambios cutáneos, problemas oculares, talla baja y anomalías genitales en varones aparecieron en una minoría sustancial, conformando un cuadro multisistémico más que una enfermedad limitada al cerebro.
Las exploraciones cerebrales revelan una firma llamativa en la sustancia blanca
La resonancia magnética proporcionó una de las pistas más claras de que esta condición recesiva es distinta del síndrome ReNU dominante. Entre 27 individuos con exploraciones o informes, 24 presentaron anomalías, y un neurorradiólogo pediátrico revisó 13 exploraciones en profundidad. Cada exploración revisada mostró afectación de la sustancia blanca, característicamente una expansión de los espacios llenos de líquido que rodean a los pequeños vasos sanguíneos (espacios perivasculares) en la sustancia blanca profunda y periventricular. En los casos más graves, estos espacios se fusionaban en racimos microquísticos compactos, a menudo acompañados de adelgazamiento del cuerpo calloso y atrofia cerebelosa. Este patrón dramático no se había descrito en el síndrome ReNU y rara vez se observó en personas con variantes de RNU4-2 en la población general, lo que lo convierte en una firma radiológica potente que puede orientar hacia pruebas genéticas dirigidas.
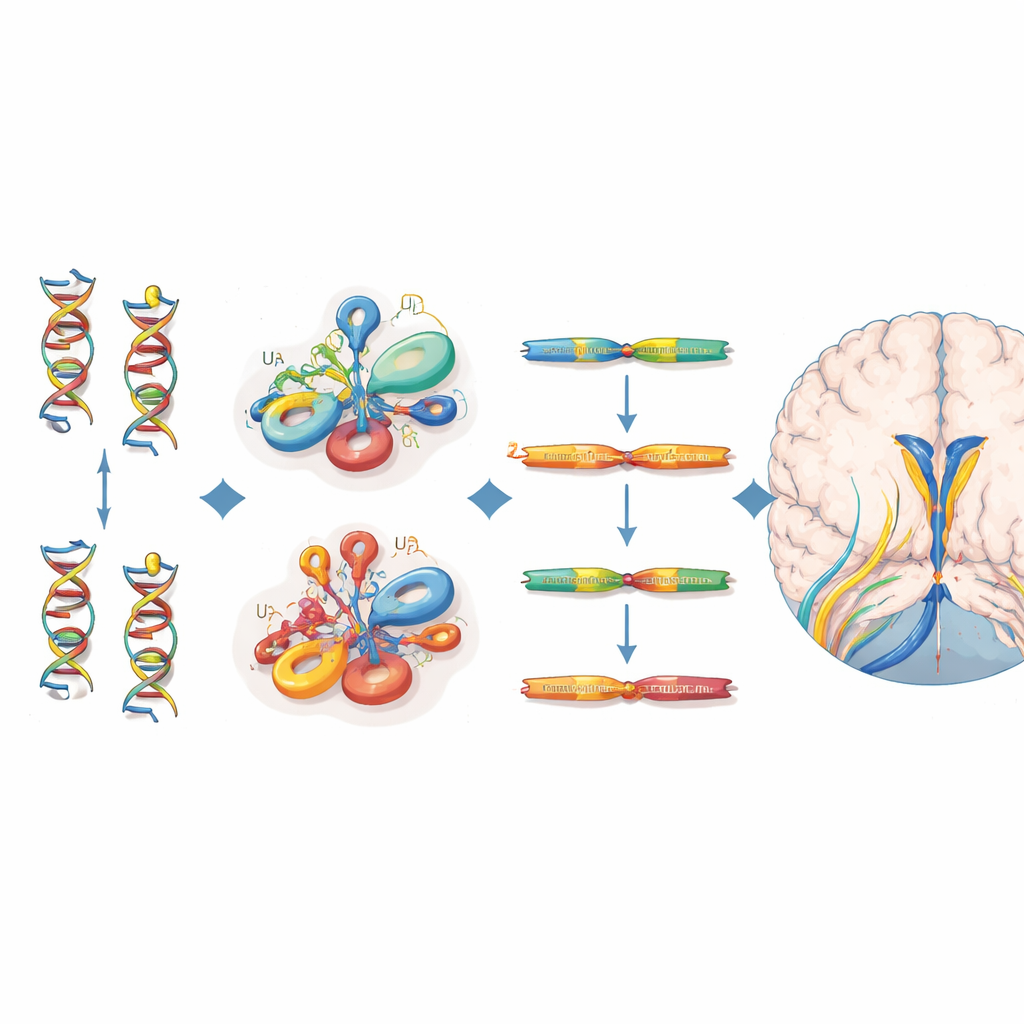
Localizando las mutaciones y su impacto molecular
Los 38 individuos afectados portaban variantes bialélicas que se agrupaban en regiones estructurales específicas del ARN U4—particularmente la región Stem II que se une al ARN U6, una curvatura pronunciada llamada k-turn que recluta proteínas, y un tramo necesario para la unión de las proteínas Sm estabilizadoras. Muchas de estas posiciones coinciden con sitios equivalentes en un ARN relacionado, RNU4ATAC, donde ya se sabe que mutaciones causan otros trastornos recesivos. Para evaluar la gravedad de cada variante, los autores se apoyaron en un experimento de edición genómica por saturación que midió cómo cientos de cambios posibles en RNU4-2 afectan la supervivencia celular. Las variantes en pacientes con enfermedad neurodesarrollativa tendieron a tener puntuaciones funcionales más bajas que las observadas en voluntarios sanos del UK Biobank, lo que respalda su papel en la enfermedad, aunque no todas las variantes clínicas importantes superaron un umbral estricto en este ensayo celular.
Mecanismo de enfermedad distinto al del síndrome hermano dominante
Mediante el análisis de datos de secuenciación de ARN, los investigadores mostraron que los niños con la condición recesiva de RNU4-2 tienen niveles marcadamente reducidos de ARN RNU4-2, junto con un fuerte aumento de un ARN estrechamente relacionado, RNU4-1. La proporción RNU4-2/RNU4-1 fue mucho más baja que en miles de muestras de otros pacientes y pudo distinguir de forma fiable a los individuos afectados, lo que sugiere un mecanismo de pérdida de función parcialmente compensado—pero no totalmente rescatado—por la regulación al alza de RNU4-1. En contraste, las personas con el síndrome ReNU dominante mostraron en realidad niveles aumentados de RNU4-2 y un cambio característico en el uso de ciertos sitios de empalme, indicando una alteración molecular cualitativamente diferente. Es notable que, a pesar del papel central de U4 en el espliceosoma mayor, el equipo no detectó el patrón amplio de retención de intrones observado en trastornos relacionados del espliceosoma menor, lo que implica un defecto más sutil o específico de tejido en el procesamiento del ARN.
Qué significa esto para las familias y los futuros diagnósticos
Para los no especialistas, el mensaje clave es que este estudio define un nuevo trastorno cerebral hereditario causado por tener dos copias defectuosas de un gen pequeño de ARN no codificante. Los niños con esta condición suelen presentar retraso del desarrollo significativo, convulsiones frecuentes y un patrón característico de cambios en la sustancia blanca en la resonancia magnética, pero son clínicamente distintos de los pacientes con el síndrome ReNU de efecto dominante más común. El descubrimiento amplía el espectro conocido de enfermedades vinculadas a los componentes de ARN del espliceosoma, subraya la importancia de incluir genes de ARN pequeños en los paneles de pruebas genéticas y señala biomarcadores sencillos—como la proporción de expresión RNU4-2 a RNU4-1 y la presencia de dilatación extrema de los espacios perivasculares—que pueden ayudar a poner fin a la odisea diagnóstica de las familias afectadas.
Cita: Rius, R., Blakes, A.J.M., Chen, Y. et al. Biallelic variants in the noncoding RNA gene RNU4-2 cause a recessive neurodevelopmental syndrome with distinct white matter changes. Nat Genet 58, 761–773 (2026). https://doi.org/10.1038/s41588-026-02554-6
Palabras clave: trastorno del neurodesarrollo, espliceosoma, ARN no codificante, cambios en la sustancia blanca, RNU4-2