Clear Sky Science · fr
Des variantes bialléliques du gène d’ARN non codant RNU4-2 provoquent un syndrome neurodéveloppemental récessif avec altérations distinctes de la substance blanche
Pourquoi cette rare histoire génétique est importante
La plupart d’entre nous considèrent les gènes comme des plans pour fabriquer des protéines, mais certains gènes agissent en coulisse, aidant les cellules à éditer les messages d’autres gènes. Cet article révèle un nouveau trouble cérébral infantile causé non pas par une protéine défectueuse, mais par de petites altérations d’un gène d’ARN non codant appelé RNU4-2. En suivant des familles du monde entier, les chercheurs montrent comment des variantes héritées de ce gène perturbent le câblage du cerveau, produisent un motif reconnaissable à l’IRM, et diffèrent d’un trouble connexe mieux connu. Ce travail illustre comment des défauts subtils dans la machinerie d’édition de l’ARN peuvent remodeler le développement cérébral — et comment de nouveaux outils génomiques révèlent enfin ces maladies cachées.
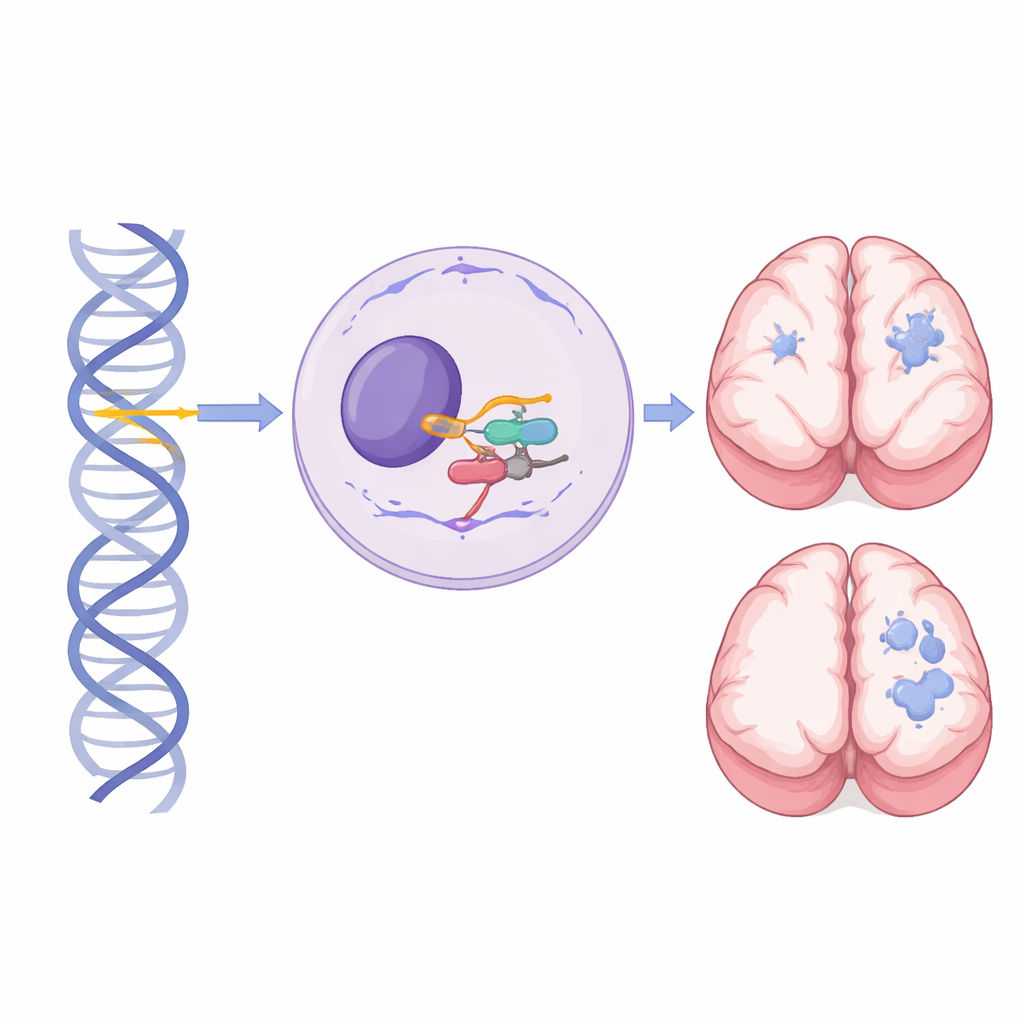
Un petit gène mais un rôle majeur dans le développement cérébral
À l’intérieur de chaque cellule, une grosse machinerie appelée spliceosome coupe et recolle les messages ARN pour que les gènes puissent être convertis en molécules fonctionnelles. RNU4-2 code pour l’ARN nucléaire petit U4, un composant essentiel du spliceosome majeur, qui traite la quasi-totalité des introns de nos gènes. Des mutations de novo dans une courte région centrale de RNU4-2 ont précédemment été montrées responsables d’un trouble neurodéveloppemental dominant commun connu sous le nom de syndrome ReNU : un enfant est affecté même si une seule copie du gène est altérée. En revanche, cette étude se concentre sur des personnes ayant hérité de variantes délétères sur les deux copies de RNU4-2 — une de chaque parent — révélant un syndrome récessif distinct.
Identification de familles et tableau clinique partagé
L’équipe a exploré de larges projets de séquençage de maladies rares et des biobanques pour repérer des individus porteurs de deux variantes de RNU4-2 et présentant des troubles du neurodéveloppement. Ils ont finalement identifié 38 personnes issues de 28 familles, et recueilli des données cliniques détaillées pour 31 d’entre elles. Presque tous présentaient un retard global du développement ou une déficience intellectuelle, souvent modérée à sévère, avec un retard d’élocution marqué ; environ la moitié n’avait pas de langage parlé significatif. De nombreux enfants ont marché tard, et plus d’un quart ne marchait jamais de manière indépendante à l’âge de cinq ans. L’hypotonie infantile, les crises d’épilepsie, les troubles du mouvement et de la coordination, ainsi que des problèmes comportementaux comme l’agressivité ou des traits obsessionnels étaient fréquents. Des anomalies cutanées, des problèmes oculaires, une petite taille et des anomalies génitales chez les garçons sont apparues chez une minorité substantielle, dessinant un tableau multisystémique plutôt qu’une maladie strictement limitée au cerveau.
Les scans cérébraux révèlent un signe frappant au niveau de la substance blanche
L’imagerie par résonance magnétique a fourni l’un des indices les plus nets que cette affection récessive est distincte du syndrome ReNU dominant. Parmi 27 individus disposant d’imageries ou de comptes rendus, 24 présentaient des anomalies, et un neuroradiologue pédiatrique a examiné en profondeur 13 scans. Chaque scan révisé montrait une atteinte de la substance blanche, le signe le plus caractéristique étant une dilatation des espaces périvasculaires — des espaces remplis de liquide entourant les petits vaisseaux — dans la substance blanche profonde et périventriculaire. Dans les cas les plus sévères, ces espaces se fondaient en amas serrés ressemblant à des microkystes, souvent accompagnés d’un amincissement du corps calleux et d’une atrophie cérébelleuse. Ce motif spectaculaire n’avait pas été décrit dans le syndrome ReNU et était rarement observé chez des personnes porteuses de variantes RNU4-2 dans la population générale, en faisant une signature radiologique puissante pouvant orienter vers un test génétique ciblé.
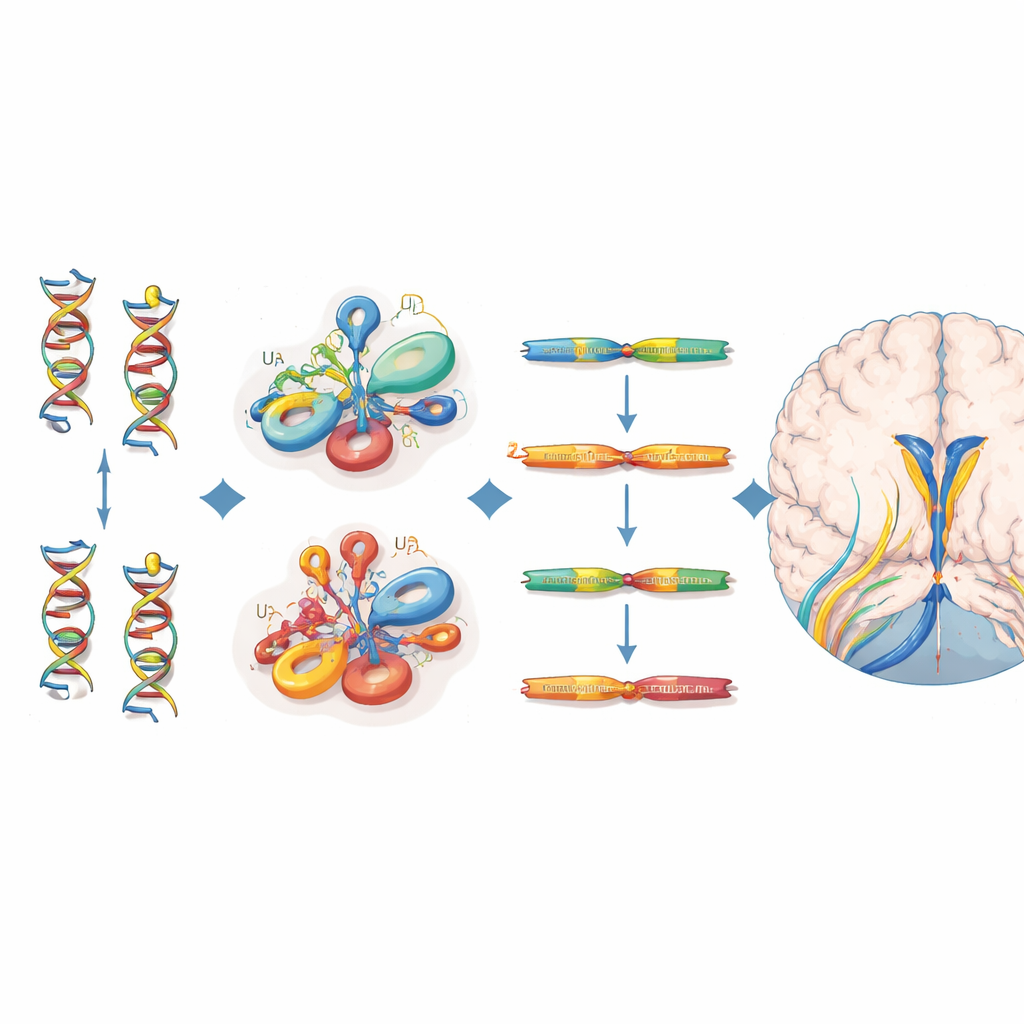
Localiser les mutations et leur impact moléculaire
Les 38 individus affectés portaient des variantes bialléliques regroupées dans des régions structurelles spécifiques de l’ARN U4 — en particulier la région Stem II qui se lie à l’ARN U6, un coude prononcé appelé k-turn qui recrute des protéines, et une séquence nécessaire à la liaison des protéines stabilisatrices Sm. Beaucoup de ces positions correspondent à des sites équivalents dans un ARN apparenté, RNU4ATAC, où des mutations sont déjà connues pour provoquer d’autres troubles récessifs. Pour évaluer la nocivité de chaque variante, les auteurs se sont appuyés sur une expérience d’édition génomique en saturation qui avait mesuré comment des centaines de changements possibles de RNU4-2 affectent la survie cellulaire. Les variantes observées chez les patients atteints de troubles neurodéveloppementaux avaient tendance à présenter des scores de fonction plus faibles que celles vues chez des volontaires sains du UK Biobank, soutenant leur rôle dans la maladie, même si toutes les variantes cliniquement importantes n’atteignaient pas un seuil strict dans ce test cellulaire.
Mécanisme de maladie différent de celui du syndrome dominant apparenté
En analysant des données de séquençage d’ARN, les chercheurs ont montré que les enfants atteints de la forme récessive liée à RNU4-2 présentent des niveaux nettement réduits d’ARN RNU4-2, associés à une forte augmentation d’un ARN étroitement apparenté, RNU4-1. Le rapport RNU4-2 / RNU4-1 était bien plus bas que dans des milliers d’autres échantillons et permettait de distinguer de manière fiable les individus affectés, suggérant un mécanisme de perte de fonction partiellement compensé — mais non entièrement sauvé — par la surexpression de RNU4-1. En revanche, les personnes atteintes du syndrome ReNU dominant présentaient en réalité des niveaux accrus de RNU4-2 et un changement caractéristique dans l’utilisation de certains sites d’épissage, indiquant une perturbation moléculaire qualitativement différente. Notamment, malgré le rôle central de U4 dans le spliceosome majeur, l’équipe n’a pas détecté le vaste schéma de rétention d’introns observé dans des troubles liés au spliceosome mineur, ce qui implique un défaut plus subtil ou spécifique à certains tissus dans le traitement de l’ARN.
Ce que cela signifie pour les familles et les diagnostics futurs
Pour les non-spécialistes, le message principal est que cette étude définit un nouveau trouble cérébral héréditaire causé par la présence de deux copies défectueuses d’un petit gène d’ARN non codant. Les enfants atteints présentent typiquement un retard de développement important, des crises fréquentes et un motif caractéristique de modification de la substance blanche à l’IRM, tout en se distinguant cliniquement des patients atteints du syndrome ReNU d’action dominante plus fréquent. Cette découverte élargit le spectre des maladies liées aux composants ARN du spliceosome, souligne l’importance d’inclure les petits gènes d’ARN dans les panels de tests génétiques, et indique des biomarqueurs simples — tels que le ratio d’expression RNU4-2 / RNU4-1 et la présence d’une dilatation périvasculaire extrême — qui peuvent aider à mettre fin à l’odyssée diagnostique des familles concernées.
Citation: Rius, R., Blakes, A.J.M., Chen, Y. et al. Biallelic variants in the noncoding RNA gene RNU4-2 cause a recessive neurodevelopmental syndrome with distinct white matter changes. Nat Genet 58, 761–773 (2026). https://doi.org/10.1038/s41588-026-02554-6
Mots-clés: trouble du neurodéveloppement, spliceosome, ARN non codant, altérations de la substance blanche, RNU4-2