Clear Sky Science · it
Nuovo metodo universale centrato sui domini per la classificazione delle proteine
Perché ordinare le proteine è importante per la salute
All’interno di ogni cellula, migliaia di piccole macchine proteiche mantengono la vita operativa. Tra le più importanti ci sono le chinasi proteiche, enzimi che accendono o spengono altre proteine e rappresentano bersagli chiave per molti farmaci moderni, in particolare le terapie contro il cancro. Tuttavia gli scienziati faticano ancora a classificare con chiarezza tutte le chinasi in famiglie che riflettano il loro funzionamento. Questo articolo presenta un nuovo modo di classificare le chinasi—e, in linea di principio, molte altre proteine—concentrandosi sulla regione centrale condivisa che svolge il lavoro, e sulle caratteristiche fisico-chimiche di base dei suoi mattoni. Ciò promette mappe più nitide delle famiglie proteiche e, in ultima analisi, indizi migliori per la progettazione di farmaci.
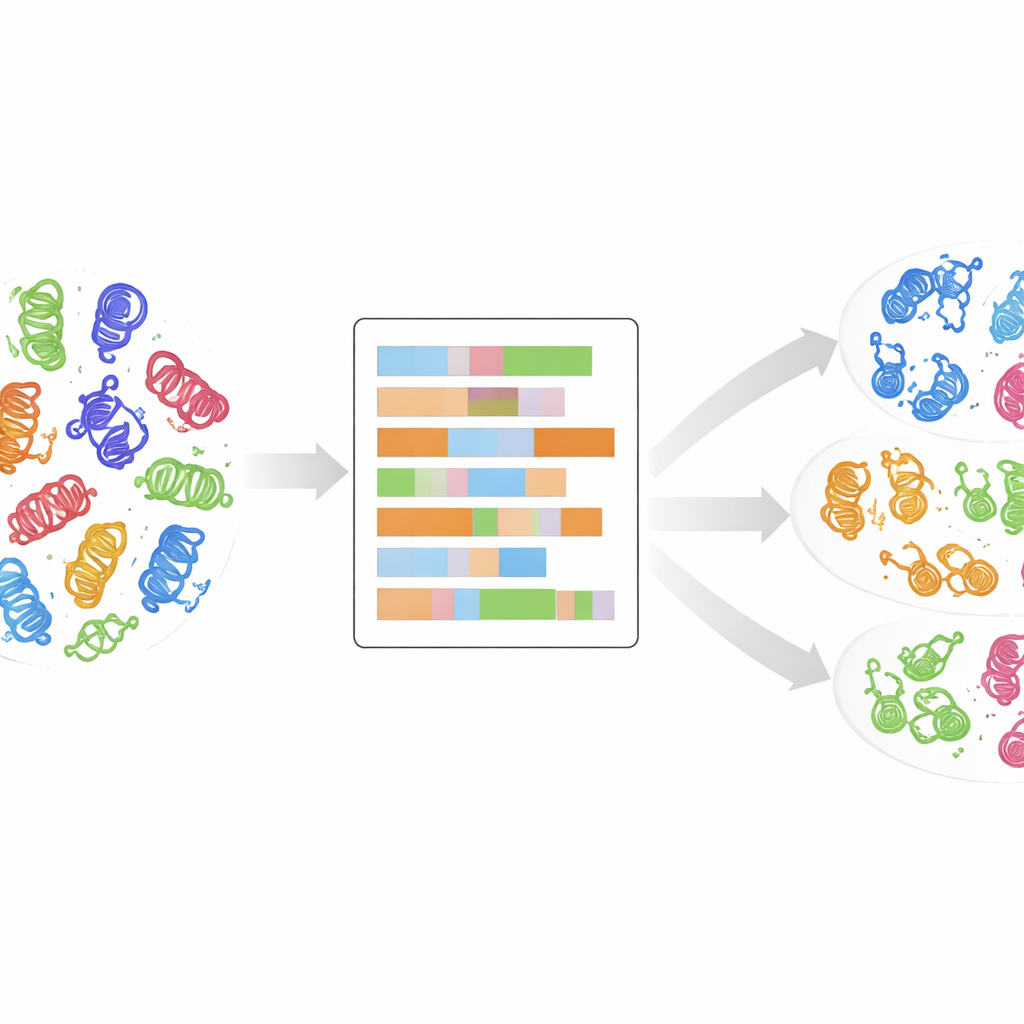
Dagli alberi genealogici a un’impronta più dettagliata
Tradizionalmente, le chinasi sono state raggruppate in classi confrontando le loro sequenze geniche o proteiche e costruendo “alberi familiari” evolutivi. Questo approccio ha avuto grande successo, rivelando circa 500 chinasi umane che rientrano in diversi gruppi principali come AGC, CAMK, CMGC, STE, TK, TKL e altri. Eppure molte chinasi di nuova scoperta non si inseriscono perfettamente in questi gruppi: le loro sequenze appaiono diverse, pur potendo comportarsi in modo simile nelle cellule. I confronti standard prestano inoltre scarsa attenzione alle proprietà intrinseche di ciascun amminoacido—dimensione, carica o carattere idrofilo—che determinano come una proteina si piega e funziona. Gli autori sostengono che per comprendere veramente le famiglie di chinasi è necessario andare oltre l’abbinamento alfabetico delle sequenze ed esaminare queste impronte fisico-chimiche.
Ingrandire il nucleo attivo delle chinasi
Per farlo, i ricercatori hanno utilizzato un allineamento di alta qualità di 497 domini di chinasi umane, i nuclei compatti che effettivamente eseguono la reazione chimica di aggiunta di gruppi fosfato. Per ogni posizione in questa mappa di dominio condivisa, hanno sostituito la lettera dell’amminoacido con fino a 30 descrittori numerici che catturano proprietà come carica, idrofobicità, polarità e dimensione, oltre a un indicatore per i gap. Il risultato è un ritratto numerico dettagliato di ciascun dominio di chinasi, dove comportamenti simili nello spazio tridimensionale dovrebbero tradursi in pattern simili in questi numeri. Hanno quindi ridotto la complessità di questi ritratti usando l’analisi delle componenti principali, una tecnica standard che condensa molte misure in poche direzioni principali che catturano le differenze maggiori.
Lascare che i dati si raggruppino da soli
Senza dire al computer a quale classe conosciuta appartenesse ogni chinasi, il team ha applicato un metodo di clustering non supervisionato chiamato k-means ai dati numerici ridotti. Hanno esplorato numerosi possibili numeri di cluster e utilizzato punteggi statistici per identificare i raggruppamenti più significativi, quindi hanno combinato diverse di queste soluzioni in un set finale di 24 cluster, ognuno con un punteggio di confidenza che riflette la stabilità tra le esecuzioni. Sorprendentemente, circa il 90% delle chinasi è finito in cluster che corrispondevano alle etichette di classe originali, suggerendo che il ritratto di dominio fisico-chimico recupera naturalmente—e a volte affina—le classificazioni esistenti. Alcuni cluster contenevano una miscela di una classe principale e chinasi precedentemente etichettate come “OTHER”, insinuando che quegli outlier potrebbero in realtà appartenere a una famiglia stabilita.
Scoprire punti caldi strutturali chiave
Oltre al raggruppamento, il metodo rivela quali parti del dominio della chinasi guidano effettivamente queste differenze. Combinando le componenti principali con le proprietà dei residui e poi mescolando i dati in test di randomizzazione, gli autori hanno individuato posizioni specifiche i cui pattern di proprietà distinguono fortemente una classe dalle altre. Un esempio particolarmente significativo è un sito nella regione del loop di attivazione delle chinasi CMGC che quasi sempre presenta un residuo carico positivamente, a differenza della maggior parte delle altre classi. I modelli strutturali mostrano che in una chinasi rappresentativa CMGC questo residuo contribuisce a stabilizzare siti fosforilati vicini, cruciali per l’attivazione dell’enzima. Interessante notare che una chinasi “non classificata” chiamata CDC7 condivide un ambiente simile in questo sito, supportando la previsione che si comporti come una chinasi CMGC anche se la sua storia evolutiva è diversa.
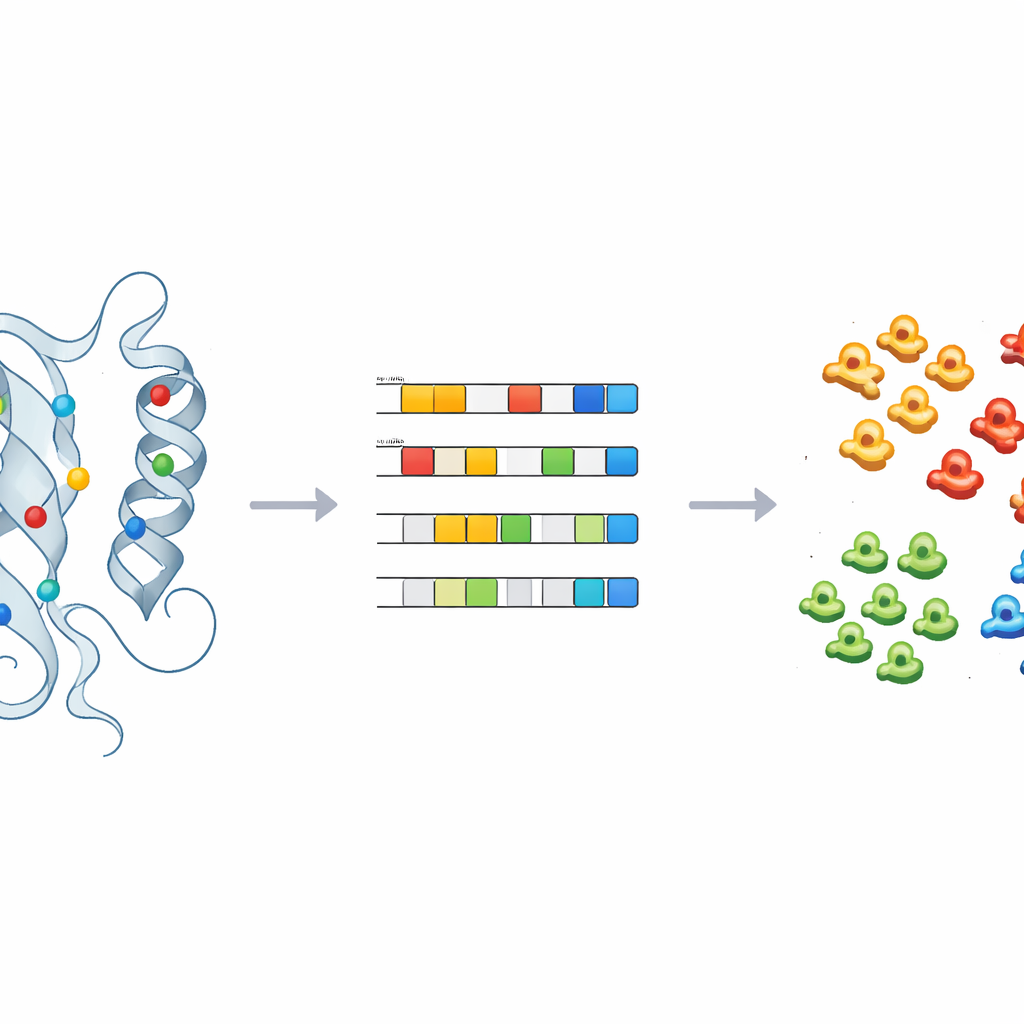
Insegnare alle macchine a etichettare gli ignoti
Per trasformare queste intuizioni in previsioni pratiche, il team ha addestrato modelli di apprendimento supervisionato—including regressione logistica, foreste casuali e un classificatore probabilistico—sui ritratti fisico-chimici delle chinasi con etichette note. Dopo un’attenta messa a punto e convalida incrociata, questi modelli sono stati in grado di assegnare accuratamente le chinasi alle classi principali usando solo un piccolo numero di componenti principali. Applicati a 66 chinasi lasciate nel gruppo generico “OTHER”, i modelli hanno riassegnato in modo coerente diverse di esse, come CDC7 e membri della famiglia ULK, a classi specifiche di chinasi. Controlli strutturali di queste riassegnazioni, soprattutto intorno alle posizioni chiave identificate in precedenza, hanno supportato le predizioni delle macchine e illustrato come il metodo possa guidare riclassificazioni e follow-up sperimentali.
Una ricetta generale per mappare le famiglie proteiche
In termini pratici, questo lavoro mostra che le proteine possono essere ordinate non solo scrutando le loro sequenze, ma distillando come si comportano fisicamente e chimicamente le loro parti centrali. Per le chinasi, questa visione centrata sul dominio e basata sulle proprietà recupera le famiglie note, aiuta a rietichettare gli elementi fuori posto e mette in evidenza “punti caldi” strutturali rilevanti per attività e regolazione. Poiché la ricetta si basa solo su un allineamento di dominio condiviso e su descrittori generali degli amminoacidi, gli autori dimostrano anche che può essere applicata ad altri gruppi proteici, come le piccole GTPasi, e potrebbe estendersi a immunoglobuline, recettori accoppiati a proteine G e oltre. Man mano che tali mappe diventano più raffinate, potrebbero orientare la progettazione di farmaci più selettivi, aiutare a interpretare mutazioni che causano malattie e offrire un atlante più chiaro e focalizzato sulle funzioni dell’universo proteico.
Citazione: Fadaei, S., Krebs, F.S. & Zoete, V. Novel universal domain-centric method for protein classification. Sci Rep 16, 11850 (2026). https://doi.org/10.1038/s41598-026-41142-w
Parole chiave: chinasi proteiche, classificazione delle proteine, apprendimento automatico, domini proteici, biologia basata sulla struttura