Clear Sky Science · de
Eine leichte, datengetriebene Segmentierungsmethode für mehrzuständige Brownsche Trajektorien
Beobachtung wandernder Moleküle
Innerhalb lebender Zellen rühren unzählige Moleküle ständig umher, binden und lösen sich wieder, und ihre Bewegung liefert Hinweise darauf, wie biologische Prozesse funktionieren. Moderne Mikroskope können einzelne Moleküle verfolgen, während sie sich bewegen, aber aus diesen verwobenen Pfaden klare Aussagen darüber zu gewinnen, wie schnell ein Molekül diffundiert oder wann es an einen Partner bindet, ist überraschend schwierig. Dieser Artikel stellt eine einfache, schnelle Methode vor, um solche Bewegungen in unterschiedliche „Zustände“ zu unterteilen, wodurch es Biologinnen und Biologen leichter fällt, die Informationen in Einzelmolekül‑Aufnahmen zu lesen.
Warum Molekültracking knifflig ist
Einzelpartikelverfolgungstechniken zeichnen die Positionen einzelner Moleküle über die Zeit auf und erzeugen so eine Trajektorie, die widerspiegelt, wie sie ihre Umgebung erkunden. In vielen realen Systemen bewegt sich ein Molekül nicht nur auf eine Weise: Es kann eine Zeitlang frei umherstreifen und dann abbremsen, wenn es an einen Rezeptor bindet oder in einem Cluster gefangen wird. Das bedeutet, die Trajektorie ist eine Mischung mehrerer Bewegungsmodi, jeder mit seiner eigenen charakteristischen Geschwindigkeit. Bestehende Analysetools können diese Modi prinzipiell trennen, aber weit verbreitete Methoden auf Basis versteckter Markov‑Modelle oder Deep Learning sind oft rechenintensiv, erfordern fachkundige Anpassung oder verhalten sich wie „Black Boxes“, deren Entscheidungen schwer zu interpretieren sind.
Eine schlanke Alternative zu schweren Algorithmen
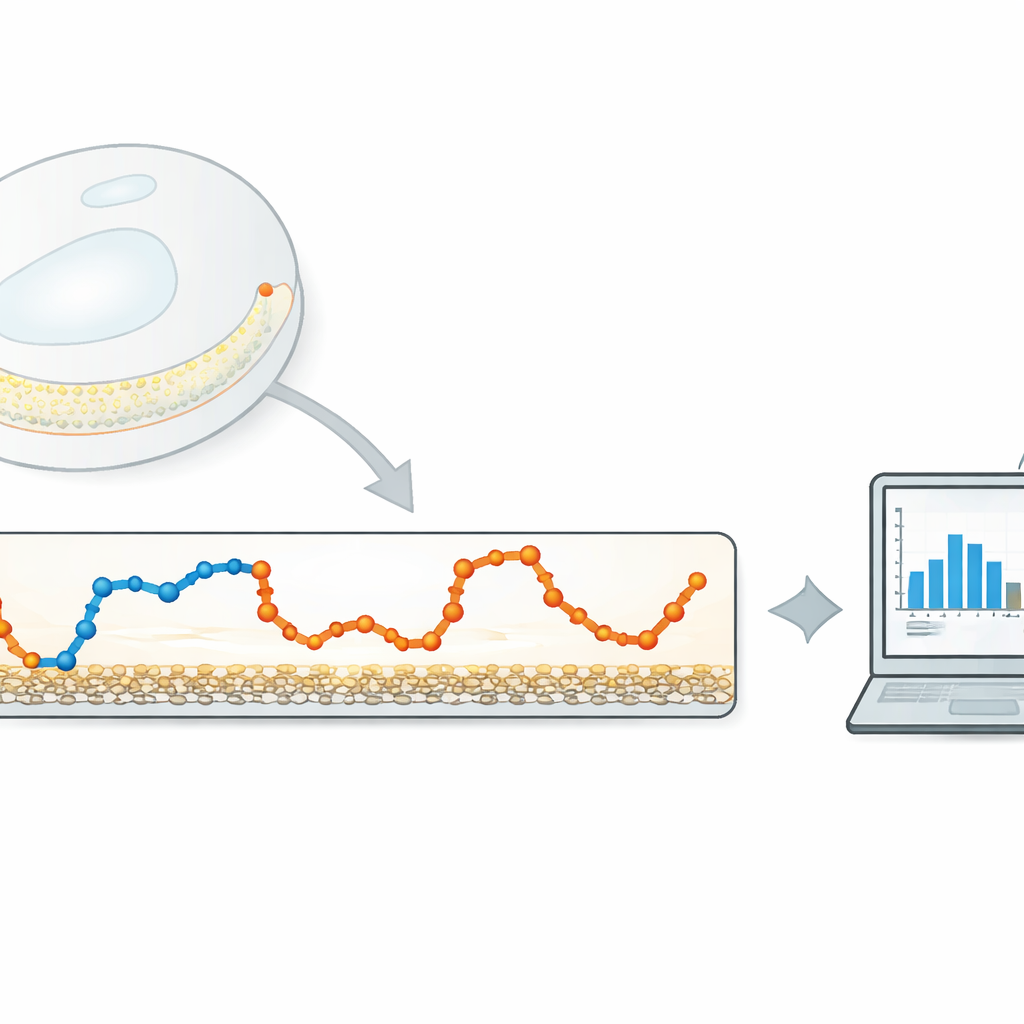
Die Autoren schlagen eine leichtgewichtige, datengetriebene Methode vor, die sich auf eine sehr einfache Größe konzentriert: wie weit sich das Teilchen zwischen aufeinanderfolgenden Kamerabildern bewegt. Zuerst berechnen sie diese schrittweisen Verschiebungen als Zeitreihe aus einer verfolgten Trajektorie. Anschließend wenden sie einen eindimensionalen Gauß‑Filter — eine Form eines gleitenden, glatt gewichteten Mittels — auf diese Serie an. Die Filterbreite steuert, wie stark benachbarte Schritte gemittelt werden. Ist der Filter zu schmal, wird wenig Rauschen entfernt; ist er zu breit, verwischen die Übergänge zwischen unterschiedlichen Bewegungszuständen. Die zentrale Idee ist, diese Breite automatisch so einzustellen, dass die gefilterten Schritte der einzelnen Bewegungszustände sich möglichst wenig überlappen.
Die Daten sich selbst sortieren lassen
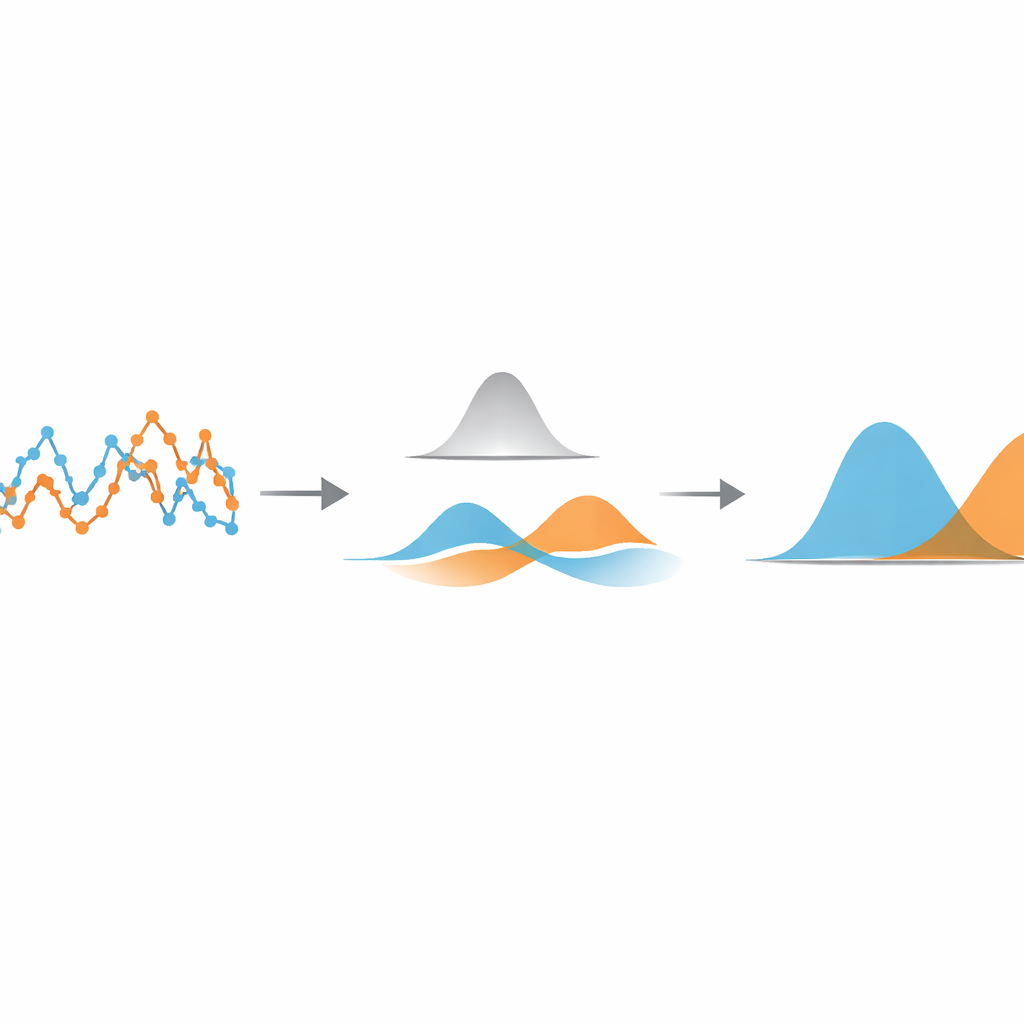
Um diesen optimalen Punkt zu finden, behandelt die Methode die gefilterten Verschiebungen als eine Mischung einfacher glockenförmiger Kurven. Mit einem standardmäßigen statistischen Werkzeug, dem Gaußschen Mischmodell, passen sie zwei solche Kurven an die gefilterten Daten und berechnen deren Überlappung. Indem sie verschiedene Filterbreiten durchprobieren und diejenige wählen, die diese Überlappung minimiert, macht der Algorithmus die unterschiedlichen Bewegungszustände so unterscheidbar, wie es die Daten zulassen. Sobald diese optimale Einstellung gefunden ist, wird jede Verschiebung dem Zustand zugeordnet, zu dessen Glockenkurve sie am wahrscheinlichsten gehört, wodurch die ursprüngliche Trajektorie effektiv in schnelle und langsame Abschnitte segmentiert wird. Wichtig ist, dass diese Segmentierung erfolgt, bevor physikalische Parameter wie Diffusionskoeffizienten oder Zustandsdauern geschätzt werden; diese können anschließend mit vertrauten, etablierten Formeln bestimmt werden.
Tests mit Simulationen und echten Molekülen
Die Forschenden prüften ihre Methode an computergenerierten Trajektorien, bei denen ein Teilchen zwischen zwei Diffusionsgeschwindigkeiten mit bekannten Eigenschaften wechselt. Sie variierten, wie stark sich die beiden Geschwindigkeiten unterschieden, wie lange das Teilchen in jedem Zustand verweilte, wie verrauscht die Positionsmessungen waren und wie viel Unschärfe die Kamera einführte. Über einen weiten Bereich realistischer Bedingungen — immer dann, wenn sich schneller und langsamerer Zustand zumindest um etwa den Faktor vier unterschieden und jeder Zustand länger als mehrere Kamerabilder andauerte — bezeichnete der Algorithmus mehr als 90 Prozent der Zeitpunkte korrekt. Entscheidend ist, dass die Methode auch bei experimentellen Daten von fluoreszenzmarkierten Proteinen in einer unterstützten Membran robust funktionierte und dort zwei klar getrennte Populationen aufdeckte: eine mobile und eine nahezu bewegungsunfähige.
Von sauberen Segmenten zu biologischen Einsichten
Sobald die Trajektorien segmentiert waren, zeigten die Autorinnen und Autoren, dass Diffusionskoeffizienten mit guter Genauigkeit wiedergewonnen werden können, selbst bei erheblichem Messrauschen oder Bewegungsunschärfe. Die Schätzung, wie lange Moleküle typischerweise in jedem Zustand verbleiben, war anspruchsvoller und erforderte längere Trajektorien, lieferte aber unter geeigneten Bedingungen dennoch sinnvolle Lebensdauern. Die zentrale Botschaft ist, dass ein vergleichsweise einfaches, transparentes Verfahren — temporäres Filtern von Schritten und das Anpassen eines Paars von Glockenkurven — mit komplexeren Ansätzen konkurrieren kann und dabei schnell auf gewöhnlichen Computern läuft. Für Experimentierende bedeutet das, Einzelpartikeldaten in Echtzeit zu verarbeiten, ihre Bildgebungsbedingungen live anzupassen und klarere Einblicke darin zu gewinnen, wie Moleküle in dicht gepackten zellulären Umgebungen binden, sich lösen und bewegen.
Zitation: El Korde, I., Lewis, J.M., Clarkson, E. et al. A light-weight, data-driven segmentation method for multi-state Brownian trajectories. npj Biol. Phys. Mech. 3, 6 (2026). https://doi.org/10.1038/s44341-026-00037-7
Schlüsselwörter: Einzelpartikelverfolgung, molekulare Diffusion, Trajektoriensegmentierung, Brownsche Bewegung, Membranproteine