Clear Sky Science · ar
أصول واتساع التأثير التبادلي الثنائي في حلزون α لإنزيم β‑لاكتاماز TEM‑1
لماذا تغييرات صغيرة في البروتين مهمة لمقاومة المضادات الحيوية
البكتيريا المقاومة للمضادات الحيوية تشكل تهديدًا متزايدًا، وتعتمد العديد منها على إنزيمات تفسد الدواء قبل أن يتمكن من العمل. أحد هذه الإنزيمات، المسمى TEM‑1 β‑لاكتاماز، يساعد بكتيريا الأمعاء الشائعة على مقاومة مضادات حيوية مستخدمة على نطاق واسع مثل الأموكسيسيلين. تركز هذه الدراسة على جزء صغير جدًا من ذلك الإنزيم—حلزون α مكوّن من 11 حمضًا أمينيًا—للإجابة عن سؤال كبير: كيف تتداخل زوجيًّا الطفرات لتجعل تطور المقاومة أسهل أو أصعب، وهل يمكننا التنبؤ بهذه التأثيرات من مبادئ فيزيائية أساسية ومن بيانات تطورية؟
حين تعتمد طفرة واحدة على أخرى
الفكرة الأساسية في هذه الدراسة هي «الإيبيستاسيس»، والتي تعني أن تأثير طفرة واحدة يعتمد على الطفرات الأخرى الموجودة. بدلاً من أن تعمل الطفرات باستقلالية، يمكن أن تساعد أو تضر بعضها بعضًا بطرق مفاجئة. بنى الباحثون مكتبة ضخمة تزيد عن 14,000 متغير من إنزيم TEM‑1، كل واحد يحمل تغييرًا واحدًا أو اثنين داخل حلزون α واحد لا يقع في موقع النشاط ولكنه يساعد في الحفاظ على شكل البروتين. ثم قاسوا مدى حماية كل متغير للبكتيريا من الأموكسيسيلين بطريقتين: بتتبع نمو البكتيريا في منافسة (مقياس مباشر لللياقة) وببتحديد أدنى تركيز للمضاد يمنع النمو (MIC، مقياس سريري نموذجي لمقاومة). سمحت هذه القياسات المزدوجة لهم بتحديد عدد المرات التي تكون فيها تأثيرات الطفرات معتمدة على السياق بدلًا من أن تكون مجردية ومضافة.
العديد من الطفرات تفسد الإنزيم، لكن معظم التداخلات يمكن التنبؤ بها
النتيجة اللافتة الأولى هي مدى هشاشة هذا الحلزون الصغير. يقضي تقريبًا نصف الطفرات الفردية في المنطقة على وظيفة الإنزيم في ظروف الاختبار، وكانت معظم الطفرات المزدوجة—ما يقرب من أربعة من أصل خمسة—غير وظيفية. كانت بعض الاستبدالات، مثل إدخال الحمض الأميني بروولين، قاتلة تقريبًا لأنها تعطل شكل الحلزون. عندما فحص الفريق كيفية تصرف الطفرات المزدوجة مقارنة بما كان متوقعًا من جمع تأثيرات الطفرات الفردية، وجدوا إيبيستاسيس واسع الانتشار: بعد استبعاد المتغيرات الميتة فعليًا، أظهرت حوالي 90% من الطفرات اعتمادًا واضحًا على السياق. ومع ذلك، كان لمعظم هذا الإيبيستاسيس نمط بسيط—كانت الطفرات تميل إلى أن تبدو أسوأ على خلفيات مضعفة بالفعل، وهو شكل من أشكال التداخل السلبي «العالمي».
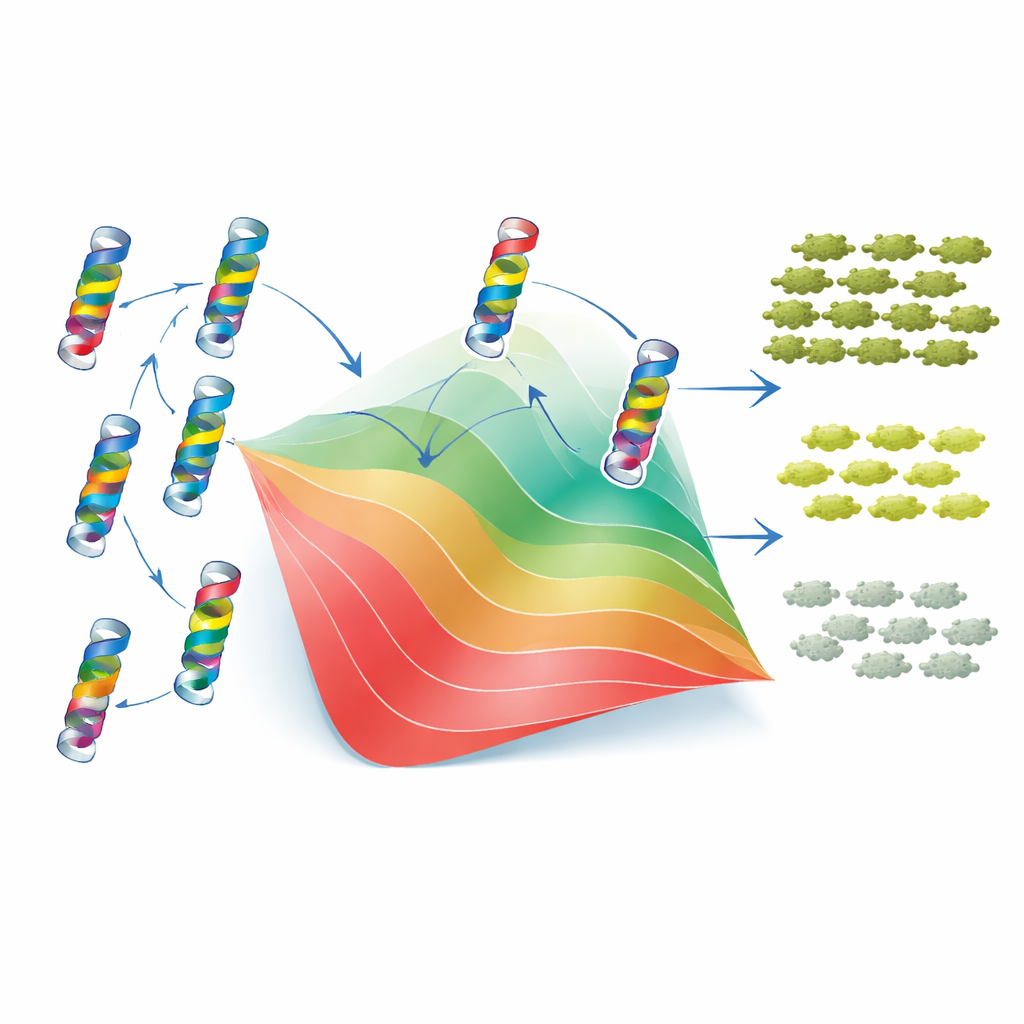
نموذج طي بسيط يوضح معظم التعقيد
لفهم سبب ظهور هذه الأنماط، لجأ المؤلفون إلى نموذج ثنائي الحالات الكلاسيكي لطي البروتين. في هذا الإطار، يكون TEM‑1 إما مطويًا ووظيفيًا أو مطويًا بشكل خاطئ وعديم الفائدة، وتعمل كل طفرة على تحريك التوازن بين هاتين الحالتين برفع أو خفض ثبات البروتين. بُنيةً حاسمة في النموذج تفترض أن تغييرات الثبات الناتجة عن الطفرات الفردية تتراكم، على الرغم من أن التأثير النهائي على اللياقة غير خطي: بمجرد أن يصبح البروتين غير مستقر بما يكفي، تصبح التغيرات الصغيرة التالية ذات عواقب كبيرة. عن طريق ملائمة هذا الإطار لبياناتهم، استطاع الباحثون إسناد «تكلفة ثبات» أو «مكسب ثبات» فعّال لكل طفرة. باستخدام هذه القيم ومعلمة ثبات أساسية واحدة، أعاد النموذج بدقة كبيرة كلًا من لياقة ومقدار MIC لآلاف الطفرات المفردة والمزدوجة، وكذلك التباين والميول العامة للتداخلات الإبيستاتية. بعبارة أخرى، تنشأ الكثير من التعقيدات الظاهرة في تداخل الطفرات من قيد فيزيائي بسيط: حاجة البروتين لأن يبقى مطويًا.
الروابط المحلية والتطور طويل الأمد يتركان أثرًا أدق
القصة ليست عالمية فحسب. عمل نموذج الحالتين بشكل أقل كفاءة للأزواج من البقايا التي تجلس قريبة جدًا من بعضها في البنية ثلاثية الأبعاد للإنزيم. بالنسبة لهؤلاء الجيران، كشفت البيانات عن إيبيستاسيس «فردي»—تركيبات محددة كانت تتصرف أفضل أو أسوأ مما كان متوقعًا من الثبات فقط، أحيانًا بتعويض شحنة أو شكل الآخر. لفحص ما إذا كانت التطور قد حفظ بصمات هذه التفاعلات المحلية، حلل المؤلفون آلاف تتابعات β‑لاكتاماز المماثلة باستخدام نموذج إحصائي من نوع «بوتس» يلتقط أي البقايا تميل إلى التغاير معًا عبر الأنواع. توافقت هذه الاقترانات المستمدة من التسلسلات بطريقتين مع النتائج التجريبية: ارتبطت بتأثيرات الثبات المستنتجة وبرزت العديد من أزواج البقايا نفسها حيث فشل نموذج الطي البسيط. عندما أعيد تحجيم مخرجات نموذج بوتس بعناية وأُدخلت عبر نفس إطار الطي، كانت قادرة حتى على التنبؤ جزئيًا بإشارة الإيبيستاسيس لأزواج طفرات جديدة.
ما يعنيه هذا لتوقع المقاومة
الخلاصة لغير المتخصصين هي أنه حتى في عنصر بنيوي صغير من بروتين واحد، تكون التفاعلات بين الطفرات شائعة لكنها ليست عشوائية. يمكن فهم معظمها كنتيجة لكيفية دفع الطفرات الإنزيم معًا نحو أو بعيدًا عن حالة مطوية مستقرة، بينما يعكس الجزء الأصغر تواصلات محلية مباشرة تضبط السلوك بدقة. حقيقة أن كلا النوعين من التأثيرات يتركان آثارًا قابلة للكشف في التطور الطويل الأمد لـ β‑لاكتامازات تشير إلى أن قواعد التفاعل الطفري مستقرة بما يكفي لأن تُتعلم وتُعمم. هذا يفتح احتمال أنه بدمج المسوحات الطفرية العميقة مع نماذج طي البروتين وبيانات التسلسل التطورية، قد نتمكن في نهاية المطاف من التنبؤ بكيفية تغير إنزيمات المقاومة—وتصميم أدوية أو علاجات يصعب على هذه الإنزيمات التحايل عليها.
الاستشهاد: Birgy, A., Roussel, C., Kemble, H. et al. Origins and breadth of pairwise epistasis in an α-helix of β-lactamase TEM-1. Nat Commun 17, 4083 (2026). https://doi.org/10.1038/s41467-026-70627-5
الكلمات المفتاحية: التأثير التبادلي (إيبيستاسيس), ثبات البروتين, β‑لاكتاماز, مقاومة المضادات الحيوية, المسح الطفري العميق للطفرات