Clear Sky Science · zh
基于DNA交叉构象、可编程的超分子水凝胶用于细胞行为的机械调控效应与细胞骨架重组
构建更适合细胞的凝胶
我们的身体不仅由细胞构成;每个细胞都被一种柔软且富含水分的支架包围并相互连接。这些天然支架不仅支撑组织,还传递机械信号,指引细胞如何生长、移动并维持健康。本研究展示了科学家如何利用DNA——同一种储存遗传信息的分子——构建高度可调的凝胶状材料,模拟这些支架并温和地引导细胞行为。
从遗传密码到智能果冻
研究者没有依赖难以细致调控且常需额外化学物质的传统材料(如胶原或海藻酸盐),而是将目光投向DNA作为构建材料。DNA的吸引力在于其组装规则简单且可预测:特定碱基按已知方式配对,使在纳米尺度上精确控制形状和连结成为可能。通过设计可组装成不同多臂结点的短DNA链,团队可以编程控制这些链如何连接成三维水凝胶——一种柔软、充水的固体,外观和触感类似生物组织。
设计定制凝胶库
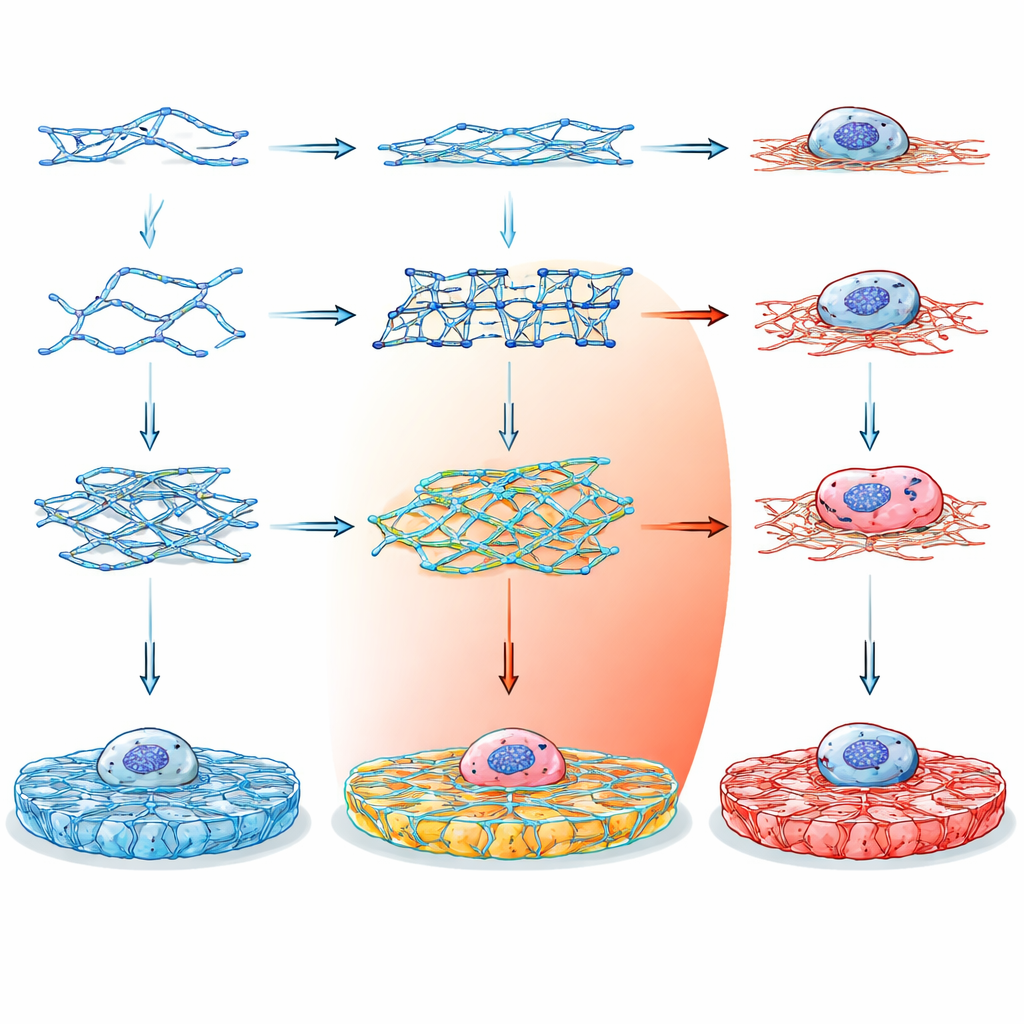
团队构建了十四种不同的DNA构件,分为三大类。双交叉(DX)构象是较为简单的阶梯状单元;旁纳米交叉(PX)构象具有更频繁的交联,使其固有更为坚硬;张弛平衡(tensegrity)构象形成具有三到六臂、在平衡张力下维持的星状单元。有些版本带有钝端无法形成网络,作为对照;另一些带有粘性末端,可通过灵活的回文连接或更具方向性的非回文连接钩连成扩展凝胶。通过精心选择链序列并用计算工具检查其稳定性,研究者确保每种构象按预期折叠并保持生物相容性。
观察并触摸DNA网络
为确认这些微小构件确实组装成更大的结构,团队使用了多种可视化和力学探测手段。结合DNA的荧光染料揭示了不同构象在显微镜下如何组织成网络:有些形成松散的团状网,有些则构成更规则、间距均匀的网格。原子力显微镜在干燥状态下提供了纳米级视图,显示张弛平衡基凝胶产生粗厚成束的纤维,在某些情况下类似天然胶原。通过用微观悬臂轻触水合凝胶并进行宏观流变学测量,他们发现这些凝胶的刚度范围广泛,约从50到185千帕,并且即便在远超过体内组织通常承受的应变下仍表现为固态类行为。
细胞对DNA微环境的响应
真正的考验是活细胞是否会注意到并从这些工程化的机械环境中受益。研究人员在覆盖有各种DNA凝胶的盖玻片上培养了人视网膜色素上皮细胞,并将其与聚-L-赖氨酸、胶原和商业基底膜提取物等标准涂层进行比较。在多种DNA架构和浓度下,细胞存活率提高,有些情况下相较于柔软的聚-L-赖氨酸对照提高了达四倍。位于适当调谐DNA凝胶上的细胞张开得更多,面积更大,且内部由肌动蛋白丝构成的支架发育更好。细胞核也变大,这是细胞与其环境强烈接触的一个标志。
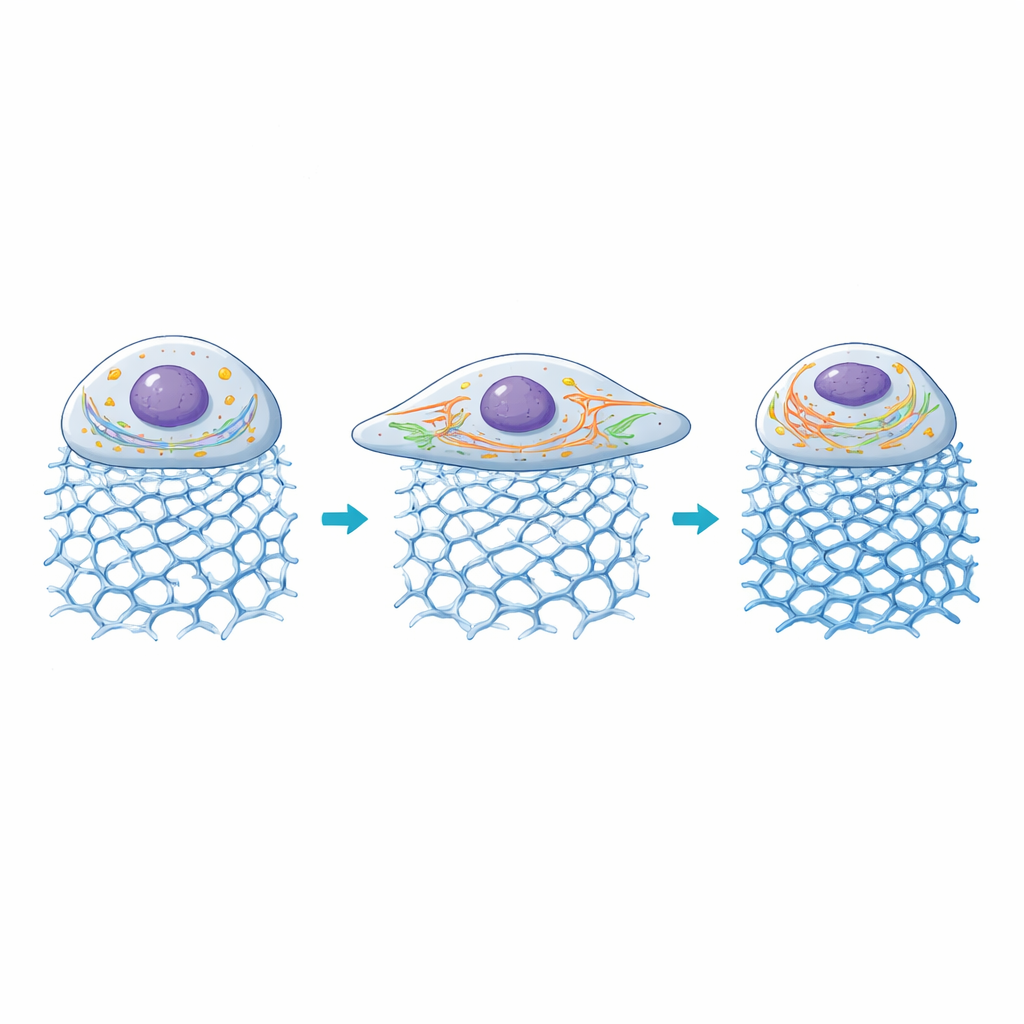
细胞内部:能量工厂与运输网络的适应
接着,研究者观察了两种关键内部结构的反应:线粒体(提供能量)和内质网(协助蛋白质与钙信号处理的网络)。在中等刚度的凝胶上,线粒体变得更分裂,这种状态与在活跃生长期间更高的能量周转相关;而内质网管状结构延长并在增大的细胞体内扩展。随着刚度超过约100千帕,细胞面积开始再次缩小,线粒体网络变得更融合,内质网信号下降,这表明过于刚性的环境会将这些细胞推离其舒适区。总体而言,这些凝胶使科学家能够将特定DNA架构与刚度水平联系到独特的细胞细胞器组织和机械信号模式。
迈向个性化组织支架
这项工作表明,DNA不仅可以作为遗传信息的载体,也可以作为可编程的构建材料,用于制造具有精细机械性能的细胞尺度景观。通过混合搭配不同的DNA构象和序列,有可能为特定细胞类型或组织调节出所需的刚度与结构,甚至加入对环境变化作出反应的响应元件。基于DNA的水凝胶指向未来的个性化支架,这些支架不仅在三维上支持细胞,还能主动引导其生长、健康与修复。
引用: Singh, A., Yadav, A., Singh, N. et al. DNA cross-over motifs-based, programmable supramolecular hydrogels for the mechanoregulatory effects of cellular behaviour and cytoskeleton reorganization. npj Biomed. Innov. 3, 30 (2026). https://doi.org/10.1038/s44385-026-00083-9
关键词: DNA水凝胶, 机械生物学, 组织工程, 细胞机械转导, 细胞外基质