Clear Sky Science · pt
Hidrogéis supramoleculares programáveis baseados em motivos de cruzamento de DNA para os efeitos mecanorregulatórios do comportamento celular e reorganização do citoesqueleto
Construindo Géis Mais Amigáveis às Células
Nossos corpos são feitos de mais do que apenas células; elas são mantidas unidas por andaimes macios e ricos em água que envolvem cada célula. Esses andaimes naturais não só sustentam os tecidos, como também transmitem sinais mecânicos que indicam às células como crescer, mover-se e permanecer saudáveis. Este estudo mostra como cientistas podem usar DNA — a mesma molécula que armazena informação genética — para construir materiais tipo gel altamente ajustáveis que imitam esses andaimes e direcionam de forma sutil o comportamento celular.
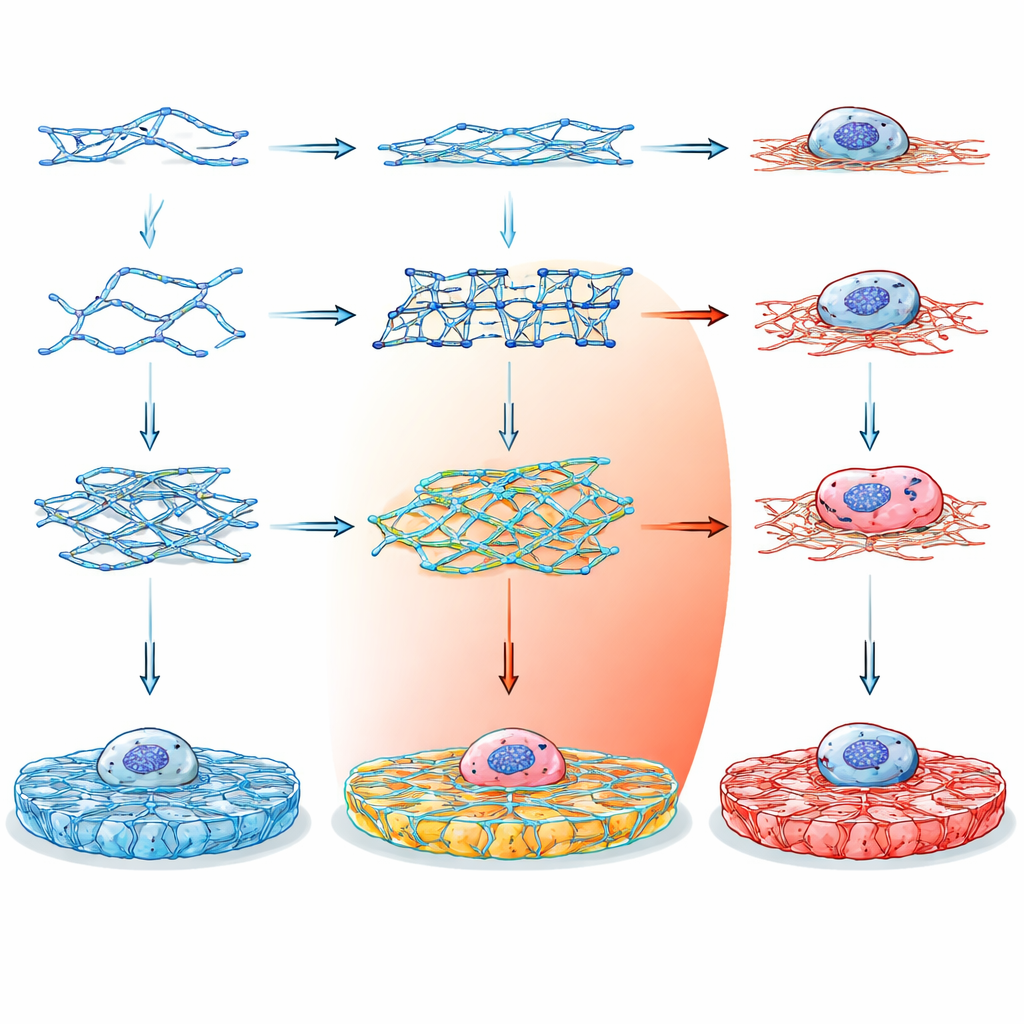
Do Código Genético ao Gel Inteligente
Em vez de depender de materiais tradicionais como colágeno ou alginato, que são difíceis de ajustar finamente sem adicionar produtos químicos extras, os pesquisadores recorreram ao DNA como material de construção. O DNA é atraente porque suas regras de montagem são simples e previsíveis: bases específicas pareiam-se de maneiras bem conhecidas, permitindo controle preciso da forma e da conectividade em escala nanométrica. Ao projetar oligonucleotídeos curtos que se autoensamblam em diferentes junções multiarmadas, a equipe pôde programar como as fitas se ligariam formando um hidrogel tridimensional — um sólido macio, cheio de água, que se parece e se comporta como tecido biológico.
Projetando uma Biblioteca de Géis Personalizados
A equipe criou quatorze blocos de construção de DNA diferentes, agrupados em três famílias principais. Motivos de dupla travessia (DX) são unidades relativamente simples, em forma de escada; motivos de travessia paranêmica (PX) apresentam entrecruzamentos mais frequentes, tornando-os intrinsecamente mais rígidos; e motivos de tensegridade formam unidades em forma de estrela com três a seis braços mantidos sob tensão balanceada. Algumas versões tinham extremidades cegas e não podiam formar redes, servindo como controles. Outras carregavam extremidades adesivas que permitiam que se conectassem em géis estendidos, com ligações palindrômicas flexíveis ou ligações não-palindrômicas mais direcionais. Ao escolher cuidadosamente as sequências das fitas e verificar sua estabilidade com ferramentas computacionais, os pesquisadores garantiram que cada motivo se dobrasse conforme o planejado e permanecesse biologicamente seguro.
Vendo e Sentindo as Redes de DNA
Para confirmar que esses minúsculos blocos realmente formavam estruturas maiores, a equipe usou várias técnicas de visualização e testes mecânicos. Corantes fluorescentes que se ligam ao DNA revelaram como diferentes motivos se organizaram em redes ao microscópio: alguns formaram teias frouxas e agregadas, enquanto outros criaram malhas mais regulares e uniformemente espaçadas. Microscopia de força atômica deu uma visão em estado seco na escala nanométrica, mostrando que géis baseados em tensegridade produziram fibras grossas e agrupadas que, em alguns casos, lembravam o colágeno natural. Ao sondar suavemente os géis hidratados com uma alavanca microscópica e realizar medições de reologia em escala macroscópica, eles descobriram que os géis cobriam uma ampla faixa de rigidez, de cerca de 50 a 185 quilopascais, e mantinham comportamento sólido mesmo sob deformações muito maiores do que aquelas tipicamente experimentadas pelos tecidos no corpo.
As Células Respondem à Paisagem de DNA
O teste real foi se células vivas notariam — e se beneficiariam de — esses ambientes mecânicos projetados. Células epiteliais pigmentares da retina humana foram cultivadas sobre lamínulas revestidas com os vários géis de DNA e comparadas com revestimentos padrão como poli-L-lisina, colágeno e extratos comerciais de membrana basal. Através de múltiplas arquiteturas de DNA e concentrações, a viabilidade celular aumentou, em alguns casos até quatro vezes em relação ao controle macio de poli-L-lisina. Células em géis de DNA adequadamente ajustados espalharam-se mais, com áreas maiores e citoesqueletos internos melhor desenvolvidos formados por filamentos de actina. Seus núcleos também aumentaram de tamanho, um marcador de células que interagem fortemente com o ambiente.
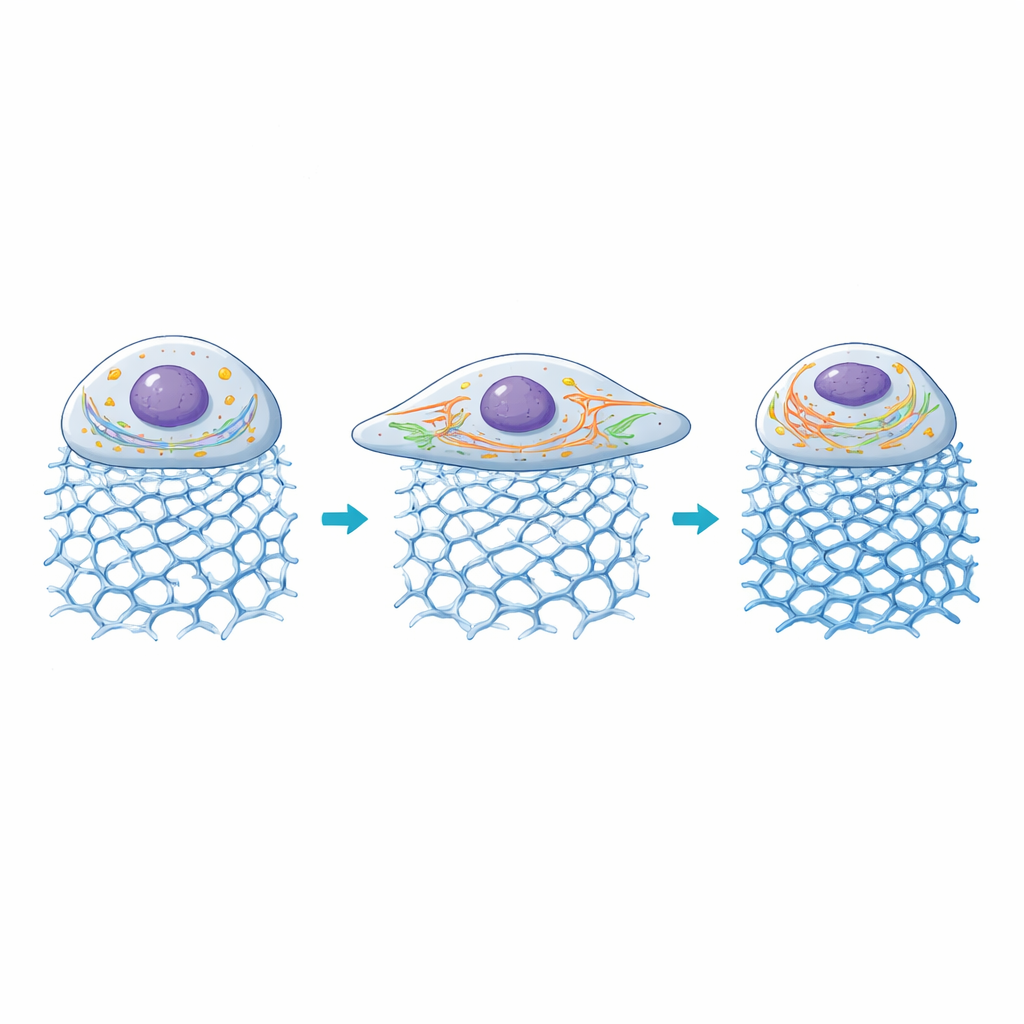
Dentro da Célula: Usinas e Rodovias se Adaptam
Os pesquisadores então observaram como duas estruturas internas-chave reagiram: mitocôndrias, que fornecem energia, e o retículo endoplasmático (RE), uma rede que ajuda a processar proteínas e sinais de cálcio. Em géis com rigidez moderada, as mitocôndrias tornaram-se mais fragmentadas, um estado associado a maior rotatividade de energia durante crescimento ativo, enquanto os túbulos do RE alongaram-se e espalharam-se pelo corpo celular ampliado. À medida que a rigidez aumentou além de aproximadamente 100 quilopascais, a área celular começou a encolher novamente, as redes mitocondriais tornaram-se mais fundidas e os sinais do RE diminuíram, sugerindo que ambientes muito rígidos deslocam essas células de sua zona de conforto. No geral, os géis permitiram aos cientistas ligar arquiteturas específicas de DNA e níveis de rigidez a padrões distintos de organização de organelas e sinalização mecânica.
Rumo a Andaimes Teciduais Personalizados
Este trabalho demonstra que o DNA pode servir não apenas como portador de informação genética, mas como um material de construção programável para criar paisagens do tamanho celular com propriedades mecânicas finamente ajustadas. Ao combinar diferentes motivos e sequências de DNA, deve ser possível ajustar com precisão a rigidez e a estrutura necessárias para tipos celulares ou tecidos particulares, e até adicionar elementos responsivos que reajam a mudanças no ambiente. Esses hidrogéis à base de DNA apontam para futuros andaimes personalizados que não só sustentam células em três dimensões, mas também orientam ativamente seu crescimento, saúde e reparo.
Citação: Singh, A., Yadav, A., Singh, N. et al. DNA cross-over motifs-based, programmable supramolecular hydrogels for the mechanoregulatory effects of cellular behaviour and cytoskeleton reorganization. npj Biomed. Innov. 3, 30 (2026). https://doi.org/10.1038/s44385-026-00083-9
Palavras-chave: hidrogéis de DNA, mecânobiologia, engenharia de tecidos, mecanotransdução celular, matriz extracelular