Clear Sky Science · sv
DNA-korsningsmotivsbaserade, programmerbara supramolekylära hydrogeler för mekanoreglerande effekter på cellbeteende och cytoskelettets omorganisation
Att bygga bättre cellvänliga geléer
Våra kroppar består av mer än bara celler; de hålls samman av mjuka, vattenrika skelett som omger varje cell. Dessa naturliga stödstrukturer inte bara ger mekaniskt stöd åt vävnader utan sänder också mekaniska signaler som berättar för cellerna hur de ska växa, röra sig och hålla sig friska. Denna studie visar hur forskare kan använda DNA – samma molekyl som lagrar genetisk information – för att bygga mycket justerbara, geléliknande material som imiterar dessa stödstrukturer och varsamt styr hur celler beter sig.
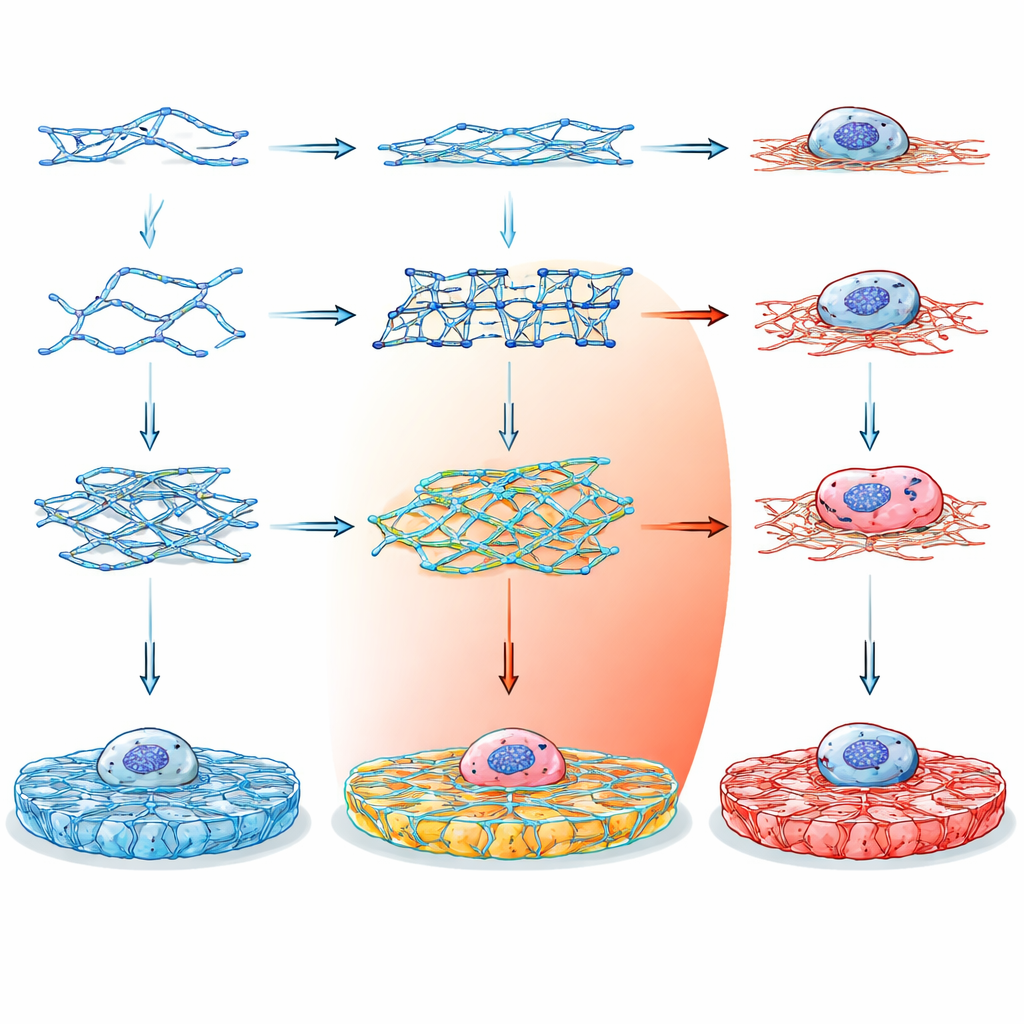
Från den genetiska koden till smart gelé
I stället för att förlita sig på traditionella material som kollagen eller alginat, som är svåra att finjustera utan extra kemikalier, vände sig forskarna till DNA som byggmaterial. DNA är attraktivt eftersom dess byggregler är enkla och förutsägbara: specifika baser parar sig på välkända sätt, vilket ger precis kontroll över form och kopplingar på nanometerskalan. Genom att designa korta DNA-strängar som monterar ihop sig till olika flermotade korsningar kunde teamet programmera hur strängarna länkas ihop till en tredimensionell hydrogel – ett mjukt, vattenfyllt material som ser ut och känns som biologisk vävnad.
Att designa ett bibliotek av skräddarsydda geléer
Teamet skapade fjorton olika DNA-byggblock, grupperade i tre huvudfamiljer. Double crossover (DX)-motiv är relativt enkla, stegliknande enheter; paranemic crossover (PX)-motiv har tätare korskopplingar och är därmed intrinsikalt styvare; och tensegrity-motiv bildar stjärnliknande enheter med tre till sex armar hållna under balanserad spänning. Vissa var avkapade i ändarna och kunde inte bilda nätverk och användes som kontroller. Andra hade klibbiga ändar som tillät dem att haka i varandra till utsträckta geléer, antingen med flexibla palindromiska kopplingar eller mer riktade, icke-palindromiska länkar. Genom att noggrant välja strängsekvenser och kontrollera deras stabilitet med beräkningsverktyg säkerställde forskarna att varje motiv veckade sig som planerat och förblev biologiskt säkert.
Att se och känna DNA-näten
För att bekräfta att dessa små byggblock verkligen bildade större strukturer använde teamet flera visualiserings- och mekaniska probemetoder. Fluorescerande färger som binder DNA visade hur olika motiv organiserade sig i nätverk under mikroskopet: vissa bildade lösa, klumpiga nät, medan andra skapade mer regelbundna, jämnt fördelade maskor. Atomkraftsmikroskopi gav en torkad-tillståndsbild på nanometerskalan och visade att tensegrity-baserade geléer producerade tjocka, samlade fibrer som i vissa fall liknade naturligt kollagen. Genom att försiktigt petta på de hydrerade geléerna med en mikroskopisk spak och göra bulk-rheologimätningar fann de att geléerna täckte ett brett styvhetsspektrum, från omkring 50 till 185 kilopascal, och förblev mer solidliknande även vid deformationer mycket större än de som vävnader normalt utsätts för i kroppen.
Celler reagerar på DNA-landskapet
Det verkliga testet var om levande celler skulle märka av – och gynnas av – dessa konstruerade mekaniska miljöer. Mänskliga retinala pigmentepitelceller odlades på täckglas belagda med de olika DNA-geléerna och jämfördes med standardbeläggningar som poly-L-lysin, kollagen och kommersiella basalmembranekstrakt. Över flera DNA-arkitekturer och koncentrationer ökade cellviabiliteten, i vissa fall upp till fyra gånger jämfört med den mjuka poly-L-lysin-kontrollen. Celler på lämpligt justerade DNA-geléer spred ut sig mer, med större ytor och bättre utvecklade interna skelett av aktinfilament. Deras cellkärnor förstoras också, ett kännetecken för celler som engagerar sig starkt med sin omgivning.
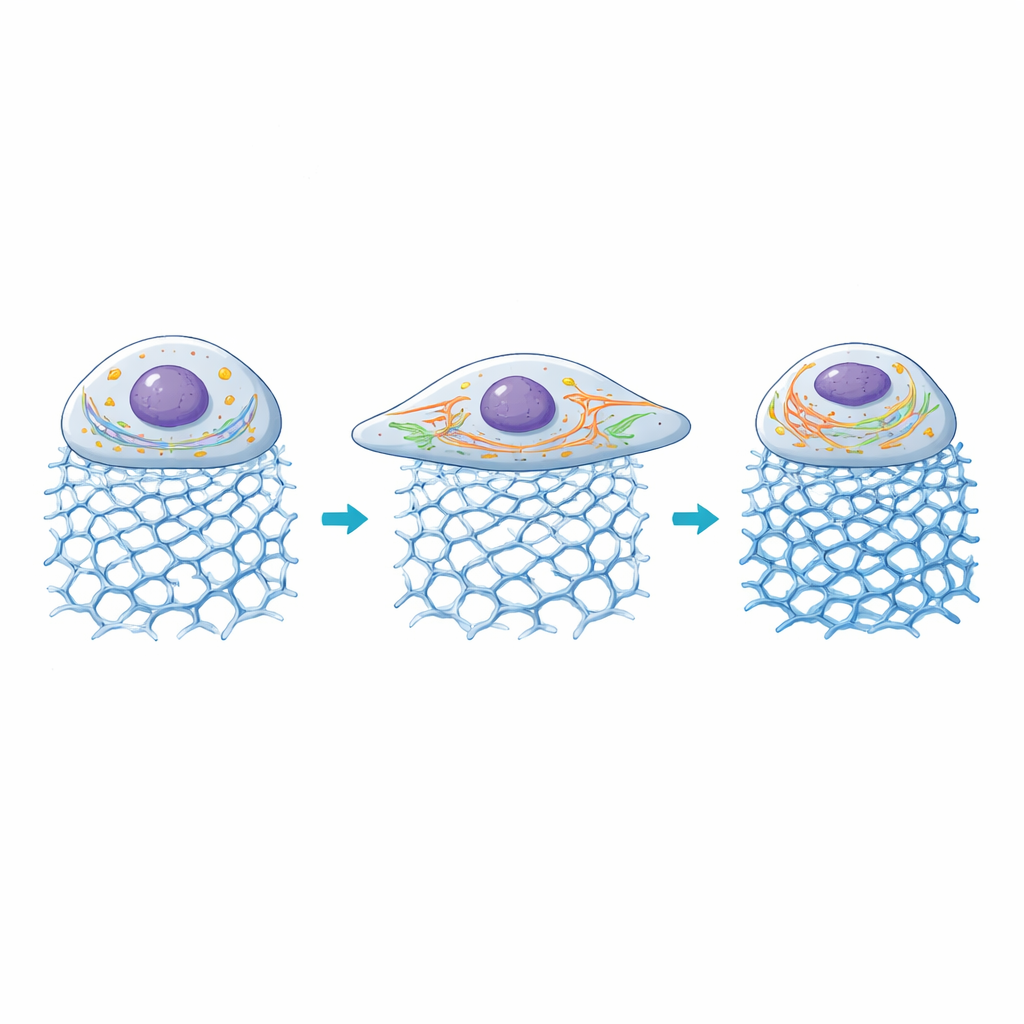
Inuti cellen: kraftverk och motorvägar anpassar sig
Forskarna undersökte sedan hur två centrala interna strukturer reagerade: mitokondrierna, som förser cellen med energi, och det endoplasmatiska retiklet (ER), ett nätverk som hjälper till att bearbeta proteiner och kalciumsignaler. På geléer med måttlig styvhet blev mitokondrierna mer fragmenterade, ett tillstånd associerat med högre energiförbrukning under aktiv tillväxt, medan ER-tubuli förlängdes och spreds genom den förstorade cellkroppen. När styvheten ökade över ungefär 100 kilopascal började cellytan krympa igen, mitokondriella nätverk blev mer sammansmälta och ER-signalerna minskade, vilket tyder på att mycket stela miljöer trycker dessa celler ur deras bekvämlighetszon. Sammantaget tillät geléerna forskarna att koppla specifika DNA-arkitekturer och styvhetsnivåer till distinkta mönster av organellorganisation och mekanisk signalering.
Mot personanpassade vävnadsskelett
Detta arbete visar att DNA kan fungera inte bara som bärare av genetisk information utan som ett programmerbart byggmaterial för att skapa cellskaliga landskap med fint avvägda mekaniska egenskaper. Genom att mixa och matcha olika DNA-motiv och sekvenser borde det vara möjligt att ställa in den styvhet och struktur som behövs för särskilda celltyper eller vävnader, och till och med lägga till responsiva element som reagerar på förändringar i miljön. Sådana DNA-baserade hydrogeler pekar mot framtida personanpassade skelett som inte bara stödjer celler i tre dimensioner utan också aktivt vägleder deras tillväxt, hälsa och reparation.
Citering: Singh, A., Yadav, A., Singh, N. et al. DNA cross-over motifs-based, programmable supramolecular hydrogels for the mechanoregulatory effects of cellular behaviour and cytoskeleton reorganization. npj Biomed. Innov. 3, 30 (2026). https://doi.org/10.1038/s44385-026-00083-9
Nyckelord: DNA-hydrogeler, mekanobiologi, vävnadsteknik, cellulär mekanotransduktion, extracellulär matrix