Clear Sky Science · es
Hidrogeles supramoleculares programables basados en motivos de cruce de ADN para los efectos mecanorreguladores del comportamiento celular y la reorganización del citoesqueleto
Construyendo geles más amigables para las células
Nuestros cuerpos están formados por más que células; están sostenidos por andamiajes blandos y ricos en agua que rodean cada célula. Estos andamiajes naturales no solo soportan los tejidos, sino que también envían señales mecánicas que indican a las células cómo crecer, moverse y mantenerse sanas. Este estudio muestra cómo los científicos pueden usar ADN —la misma molécula que almacena la información genética— para construir materiales con textura de gel altamente ajustables que imitan esos andamiajes y dirigen suavemente el comportamiento celular.
Del código genético a la gelatina inteligente
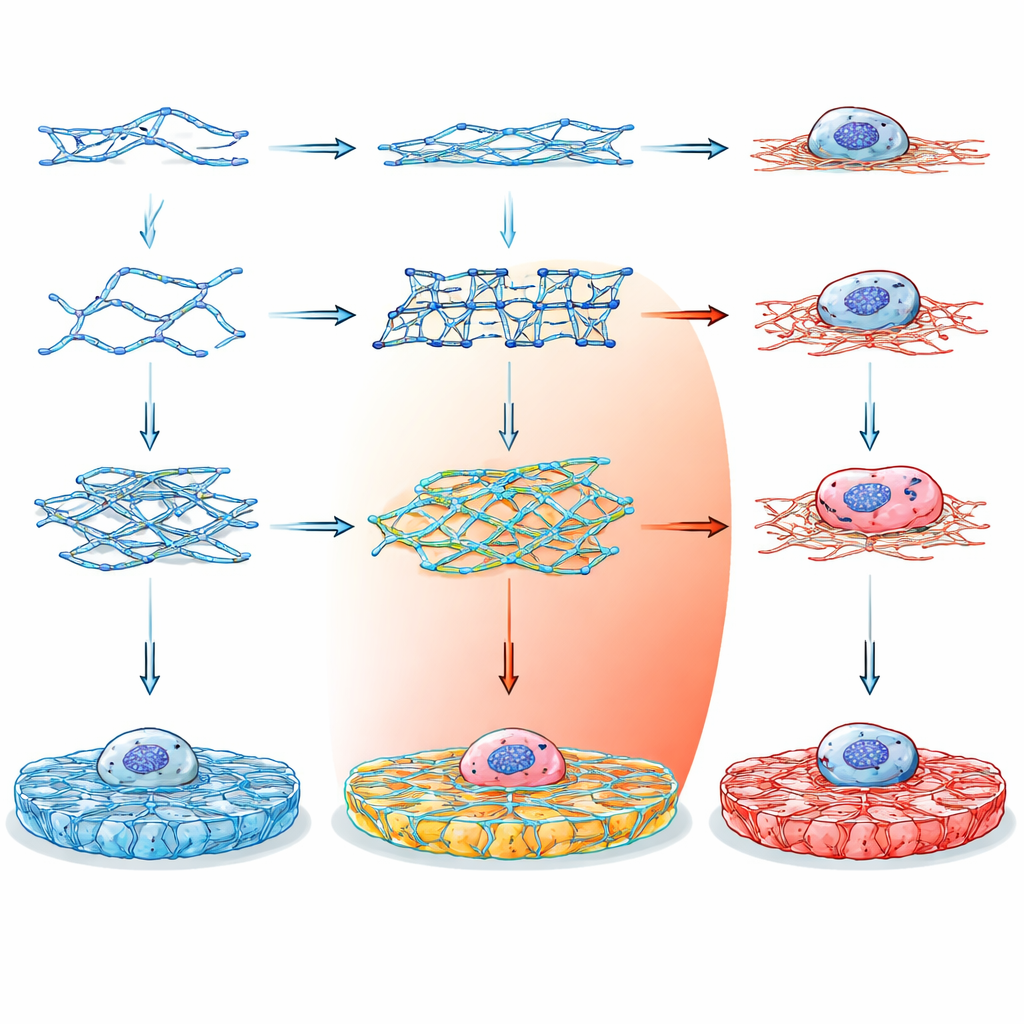
En lugar de depender de materiales tradicionales como el colágeno o el alginato, que son difíciles de afinar sin añadir químicos extra, los investigadores recurrieron al ADN como material de construcción. El ADN es prometedor porque sus reglas de ensamblaje son simples y predecibles: bases específicas se emparejan de formas bien conocidas, lo que permite un control preciso de la forma y la conectividad a escala nanométrica. Diseñando hebras cortas de ADN que se ensamblan en distintas uniones multiarmadas, el equipo pudo programar cómo las hebras se enlazan formando un hidrogel tridimensional —un sólido blando repleto de agua que se parece y se siente como tejido biológico.
Diseñando una biblioteca de geles a medida
El equipo creó catorce bloques de construcción de ADN diferentes, agrupados en tres familias principales. Los motivos de doble cruce (DX) son unidades relativamente simples, en forma de escalera; los motivos de cruce paranémico (PX) tienen cruces más frecuentes, lo que los hace intrínsecamente más rígidos; y los motivos de tensegridad forman unidades estelares con tres a seis brazos mantenidos bajo tensión equilibrada. Algunas versiones tenían extremos romos y no podían formar redes, sirviendo como controles. Otras llevaban extremos «pegajosos» que les permitían engancharse en geles extendidos, ya sea con conexiones palindrómicas flexibles o enlaces más direccionales y no palindrómicos. Al elegir cuidadosamente las secuencias de las hebras y comprobar su estabilidad con herramientas computacionales, los investigadores se aseguraron de que cada motivo se plegara según lo previsto y permaneciera biológicamente seguro.
Ver y sentir las redes de ADN
Para confirmar que estos diminutos bloques realmente formaban estructuras mayores, el equipo usó varias técnicas de visualización y sondas mecánicas. Colorantes fluorescentes que se unen al ADN revelaron cómo los distintos motivos se organizaban en redes bajo el microscopio: algunos formaban telarañas sueltas y apelmazadas, mientras que otros creaban mallas más regulares y espaciadas de manera uniforme. La microscopía de fuerza atómica ofreció una vista en estado seco a escala nanométrica, mostrando que los geles basados en tensegridad producían fibras gruesas y agrupadas que en algunos casos recordaban al colágeno natural. Al deformar suavemente los geles hidratados con una palanca microscópica y realizar medidas reológicas a escala macroscópica, encontraron que los geles abarcaban un amplio rango de rigidez, desde aproximadamente 50 hasta 185 kilopascales, y se comportaban como sólidos incluso bajo deformaciones mucho mayores que las que los tejidos experimentan típicamente en el cuerpo.
Las células responden al paisaje de ADN
La prueba real fue si las células vivas notarían —y se beneficiarían de— estos entornos mecánicos diseñados. Se cultivaron células epiteliales del pigmento retinal humano sobre cubreobjetos recubiertos con los distintos geles de ADN y se compararon con recubrimientos estándar como polilisina, colágeno y extractos comerciales de membrana basal. En múltiples arquitecturas y concentraciones de ADN, la viabilidad celular aumentó, en algunos casos hasta cuatro veces respecto al control blando de polilisina. Las células sobre geles de ADN ajustados apropiadamente se extendieron más, con áreas mayores y con andamiajes internos mejor desarrollados formados por filamentos de actina. Sus núcleos también se agrandaron, un indicio de que las células interactuaban de forma intensa con su entorno.
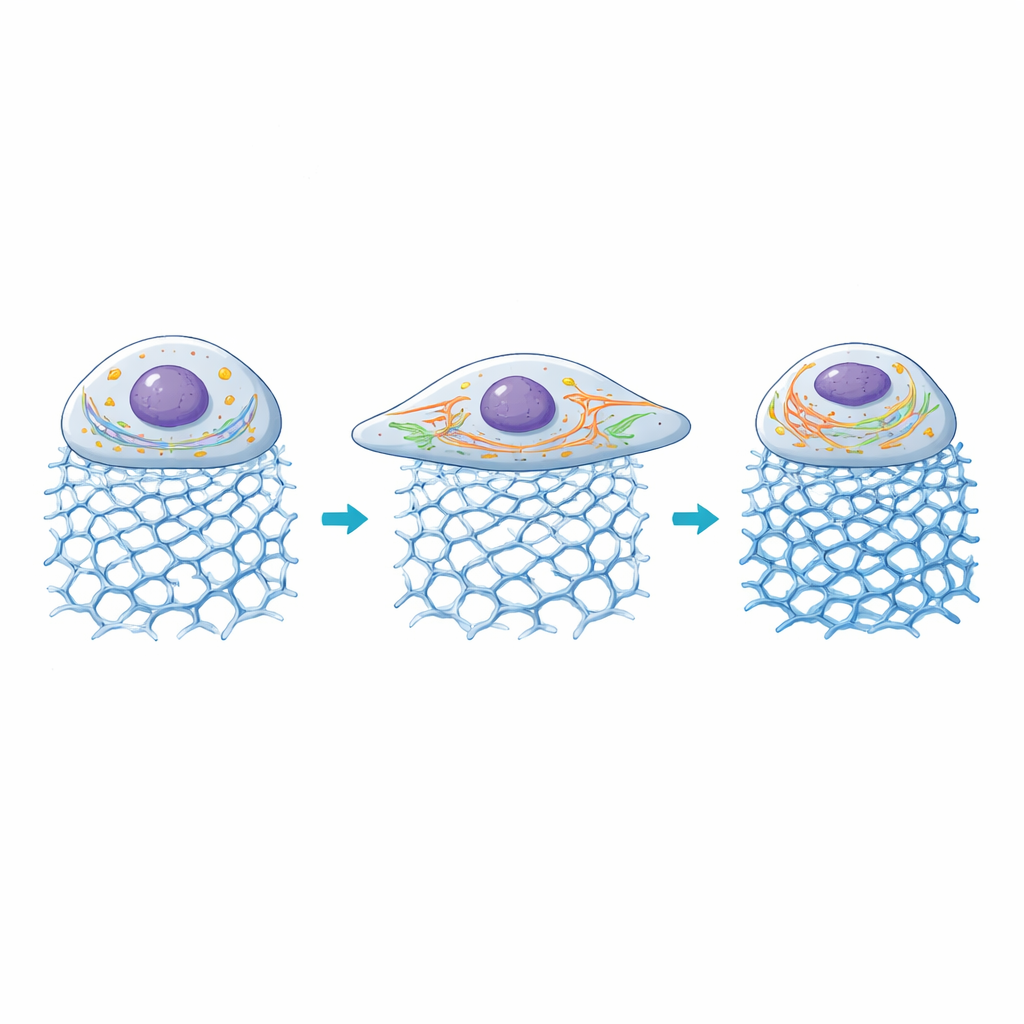
Dentro de la célula: centrales y autopistas se adaptan
Los investigadores examinaron entonces cómo reaccionaban dos estructuras internas clave: las mitocondrias, que suministran energía, y el retículo endoplásmico (RE), una red que ayuda a procesar proteínas y señales de calcio. En geles con rigidez moderada, las mitocondrias se volvieron más fragmentadas, un estado asociado a un mayor recambio energético durante el crecimiento activo, mientras que los túbulos del RE se alargaron y se extendieron por el cuerpo celular agrandado. Al aumentar la rigidez por encima de aproximadamente 100 kilopascales, el área celular comenzó a reducirse de nuevo, las redes mitocondriales se volvieron más fusionadas y las señales del RE disminuyeron, lo que sugiere que entornos muy rígidos sacan a estas células de su zona de confort. En conjunto, los geles permitieron a los científicos vincular arquitecturas específicas de ADN y niveles de rigidez con patrones distintivos de organización de orgánulos y señalización mecánica.
Hacia andamiajes tisulares personalizados
Este trabajo demuestra que el ADN puede servir no solo como portador de información genética, sino como un material de construcción programable para crear paisajes del tamaño celular con propiedades mecánicas finamente ajustadas. Mezclando y combinando distintos motivos y secuencias de ADN, debería ser posible sintonizar la rigidez y la estructura necesarias para tipos celulares o tejidos concretos, e incluso añadir elementos sensibles que reaccionen a cambios en el entorno. Estos hidrogeles basados en ADN apuntan hacia futuros andamiajes personalizados que no solo soporten a las células en tres dimensiones, sino que también guíen activamente su crecimiento, salud y reparación.
Cita: Singh, A., Yadav, A., Singh, N. et al. DNA cross-over motifs-based, programmable supramolecular hydrogels for the mechanoregulatory effects of cellular behaviour and cytoskeleton reorganization. npj Biomed. Innov. 3, 30 (2026). https://doi.org/10.1038/s44385-026-00083-9
Palabras clave: Hidrogeles de ADN, Mecanobiología, Ingeniería de tejidos, Mecanotransducción celular, Matriz extracelular