Clear Sky Science · de
DNA-Crossover-Motiv-basierte, programmierbare supramolekulare Hydrogele für die mechanoregulatorischen Effekte auf Zellverhalten und Zytoskelett-Reorganisation
Bessere zellfreundliche Gele entwickeln
Unser Körper besteht nicht nur aus Zellen; er wird von weichen, wasserreichen Gerüsten zusammengehalten, die jede Zelle umgeben. Diese natürlichen Gerüste stützen nicht nur das Gewebe, sondern senden auch mechanische Signale, die Zellen sagen, wie sie wachsen, sich bewegen und gesund bleiben sollen. Diese Studie zeigt, wie Wissenschaftler DNA – dasselbe Molekül, das genetische Informationen speichert – nutzen können, um hochgradig einstellbare, gelartige Materialien zu bauen, die diese Gerüste nachahmen und das Zellverhalten behutsam steuern.
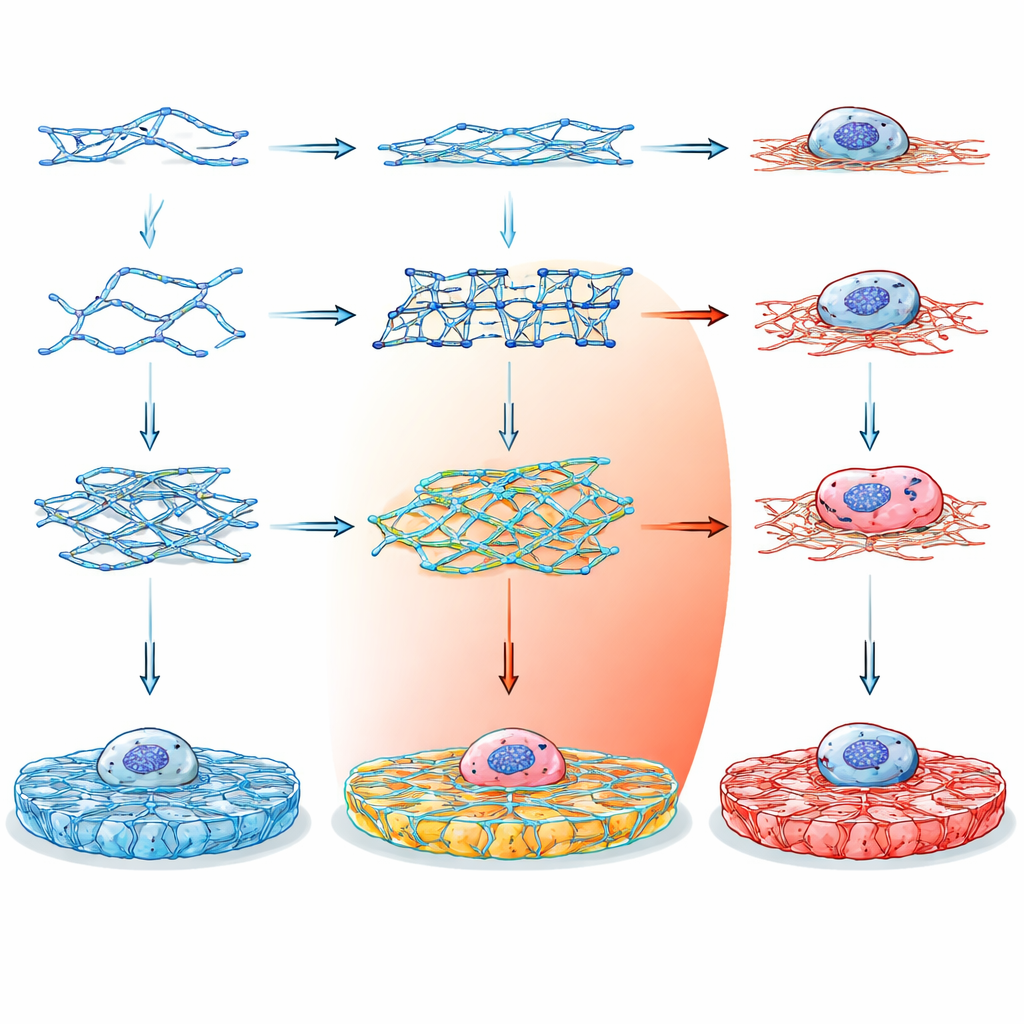
Vom genetischen Code zum smarten Gel
Anstatt sich auf traditionelle Materialien wie Kollagen oder Alginat zu stützen, die sich nur schwer feinabstimmen lassen ohne Zusatzstoffe, wandten sich die Forschenden DNA als Baumaterial zu. DNA ist attraktiv, weil ihre Bauprinzipien einfach und vorhersehbar sind: bestimmte Basen paaren sich auf bekannte Weise, was präzise Kontrolle über Form und Vernetzung im Nanometermaßstab erlaubt. Durch das Design kurzer DNA-Stränge, die sich zu unterschiedlich stark verzweigten Knoten zusammenschließen, konnte das Team programmieren, wie die Stränge zu einem dreidimensionalen Hydrogel vernetzen – einem weichen, wassergefüllten Feststoff, der in Aussehen und Gefühl biologischem Gewebe ähnelt.
Eine Bibliothek maßgeschneiderter Gele entwerfen
Das Team erzeugte vierzehn verschiedene DNA-Bausteine, die in drei Hauptfamilien gruppiert sind. Double-Crossover-(DX)-Motive sind relativ einfache, leiterartige Einheiten; paranemische Crossover-(PX)-Motive haben häufigere Querbindungen, was sie intrinsisch steifer macht; und Tensegrity-Motive bilden sternartige Einheiten mit drei bis sechs Armen, die unter ausgewogenem Zug stehen. Einige Varianten hatten stumpfe Enden und konnten keine Netzwerke bilden und dienten als Kontrollen. Andere trugen sticky ends, die ihnen erlaubten, sich zu ausgedehnten Gelen zu verbinden, entweder mit flexiblen palindromischen Verknüpfungen oder mit richtungsgebundenen, nicht-palindromischen Verbindungen. Durch sorgfältige Auswahl der Strangsequenzen und Überprüfung ihrer Stabilität mit Rechentools stellten die Forschenden sicher, dass sich jedes Motiv wie geplant faltete und biologisch verträglich blieb.
Die DNA-Netzwerke sehen und ertasten
Um zu bestätigen, dass diese winzigen Bausteine tatsächlich größere Strukturen bildeten, nutzte das Team mehrere Visualisierungs- und Mechanikmethoden. Fluoreszierende Farbstoffe, die an DNA binden, zeigten unter dem Mikroskop, wie sich verschiedene Motive zu Netzwerken organisierten: manche bildeten lockere, klumpige Netze, während andere regelmäßigere, gleichmäßigere Maschen erzeugten. Die Rasterkraftmikroskopie lieferte eine Ansicht im getrockneten Zustand auf Nanometerskala und zeigte, dass tensegrity-basierte Gele dicke, gebündelte Fasern produzierten, die in einigen Fällen natürlichem Kollagen ähnelten. Durch sanftes Antasten der hydrierten Gele mit einem mikroskopischen Cantilever und Messungen der Scherrheologie im Volumenbereich fanden sie heraus, dass die Gele ein weites Steifigkeitsspektrum abdeckten, von etwa 50 bis 185 Kilopascal, und selbst bei Dehnungen, die deutlich größer sind als jene, denen Gewebe im Körper typischerweise ausgesetzt sind, weiterhin festartig blieben.
Zellen reagieren auf die DNA-Landschaft
Der eigentliche Test war, ob lebende Zellen diese konstruierten mechanischen Umgebungen wahrnehmen — und davon profitieren würden. Menschliche retinal-pigmentierte Epithelzellen wurden auf Deckgläsern kultiviert, die mit den verschiedenen DNA-Gelen beschichtet waren, und mit Standardbeschichtungen wie Poly-L-Lysin, Kollagen und kommerziellen Basement-Membrane-Extrakten verglichen. Über mehrere DNA-Architekturen und Konzentrationen hinweg stieg die Zellviabilität an, in einigen Fällen bis zu vierfach im Vergleich zur weichen Poly-L-Lysin-Kontrolle. Zellen auf entsprechend abgestimmten DNA-Gelen breiteten sich stärker aus, zeigten größere Flächen und besser entwickelte interne Gerüste aus Aktinfilamenten. Auch ihre Zellkerne vergrößerten sich, ein Kennzeichen dafür, dass Zellen intensiv mit ihrer Umgebung interagieren.
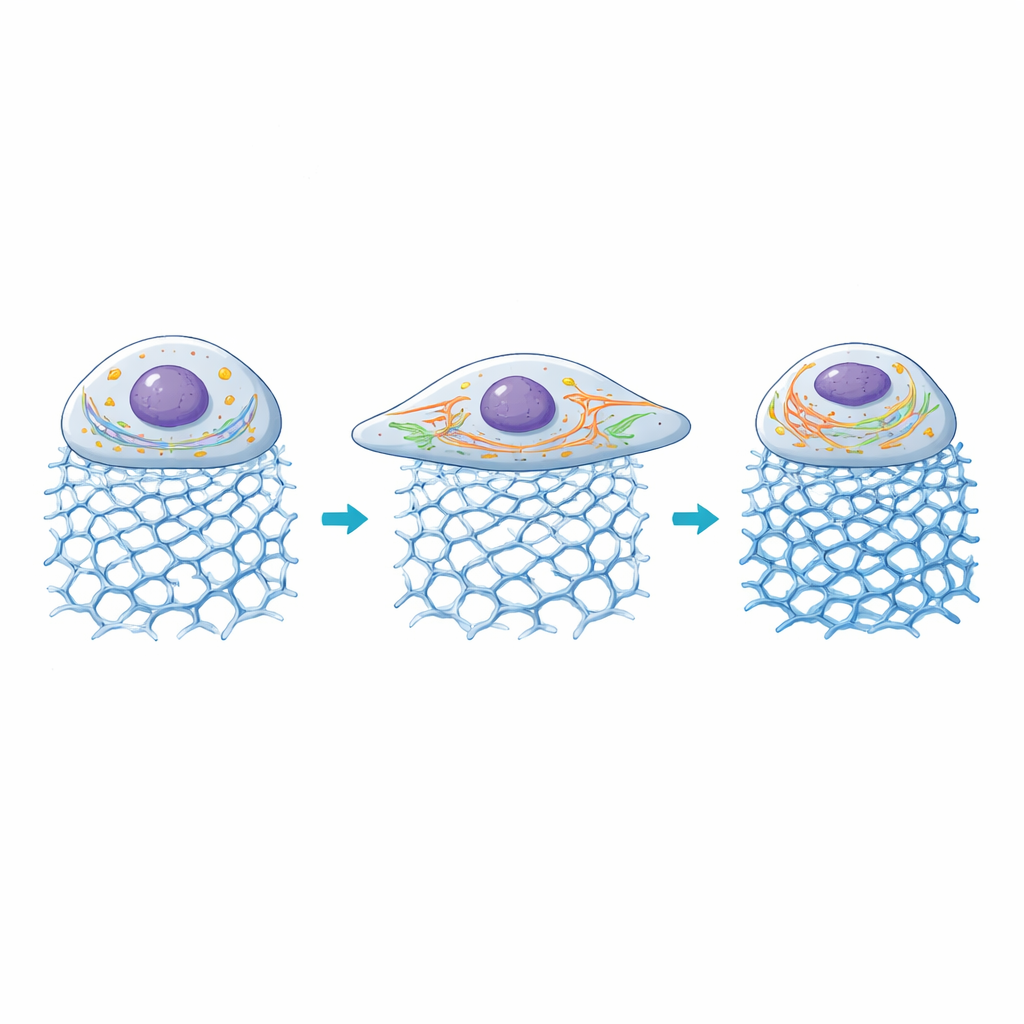
Im Inneren der Zelle: Kraftwerke und Autobahnen passen sich an
Die Forschenden untersuchten dann, wie zwei wichtige intrazelluläre Strukturen reagierten: Mitochondrien, die Energie bereitstellen, und das endoplasmatische Retikulum (ER), ein Netzwerk, das bei der Proteinverarbeitung und Kalziumsignalisierung hilft. Auf Gelen mit moderater Steifigkeit wurden Mitochondrien fragmentierter, ein Zustand, der mit höherem Energieumsatz während aktivem Wachstum assoziiert ist, während ER-Tubuli sich verlängerten und sich durch den vergrößerten Zellkörper ausbreiteten. Mit zunehmender Steifigkeit jenseits von etwa 100 Kilopascal begann die Zellfläche wieder zu schrumpfen, mitochondriale Netzwerke verschmolzen stärker und ER-Signale nahmen ab, was darauf hindeutet, dass sehr starre Umgebungen diese Zellen aus ihrer Komfortzone drängen. Insgesamt ermöglichten die Gele den Wissenschaftlern, spezifische DNA-Architekturen und Steifigkeitsstufen mit charakteristischen Mustern der Organellenorganisation und mechanischen Signalgebung zu verknüpfen.
Auf dem Weg zu personalisierten Gewebegerüsten
Diese Arbeit zeigt, dass DNA nicht nur als Träger genetischer Information dienen kann, sondern auch als programmierbares Baumaterial, um zellgroße Landschaften mit fein abgestimmten mechanischen Eigenschaften zu bauen. Durch das Mischen und Kombinieren verschiedener DNA-Motive und -Sequenzen sollte es möglich sein, die nötige Steifigkeit und Struktur für bestimmte Zelltypen oder Gewebe einzustellen und sogar reaktive Elemente hinzuzufügen, die auf Umweltveränderungen reagieren. Solche DNA-basierten Hydrogele weisen auf zukünftige personalisierte Gerüste hin, die Zellen nicht nur dreidimensional stützen, sondern ihr Wachstum, ihre Gesundheit und Reparatur aktiv lenken.
Zitation: Singh, A., Yadav, A., Singh, N. et al. DNA cross-over motifs-based, programmable supramolecular hydrogels for the mechanoregulatory effects of cellular behaviour and cytoskeleton reorganization. npj Biomed. Innov. 3, 30 (2026). https://doi.org/10.1038/s44385-026-00083-9
Schlüsselwörter: DNA-Hydrogele, Mechanobiologie, Gewebeengineering, zelluläre Mechanotransduktion, extrazelluläre Matrix