Clear Sky Science · fr
Hydrogels supramoléculaires programmables basés sur des motifs d’échanges d’ADN pour les effets mécanorégulateurs du comportement cellulaire et la réorganisation du cytosquelette
Concevoir de meilleurs gels compatibles avec les cellules
Nos corps sont faits de bien plus que de simples cellules ; elles sont maintenues par des échafaudages mous riches en eau qui entourent chaque cellule. Ces structures naturelles soutiennent les tissus, mais envoient aussi des signaux mécaniques qui indiquent aux cellules comment croître, se déplacer et rester en bonne santé. Cette étude montre comment des chercheurs peuvent utiliser l’ADN — la même molécule qui porte l’information génétique — pour construire des matériaux gélatineux hautement modulables qui imitent ces échafaudages et orientent en douceur le comportement cellulaire.
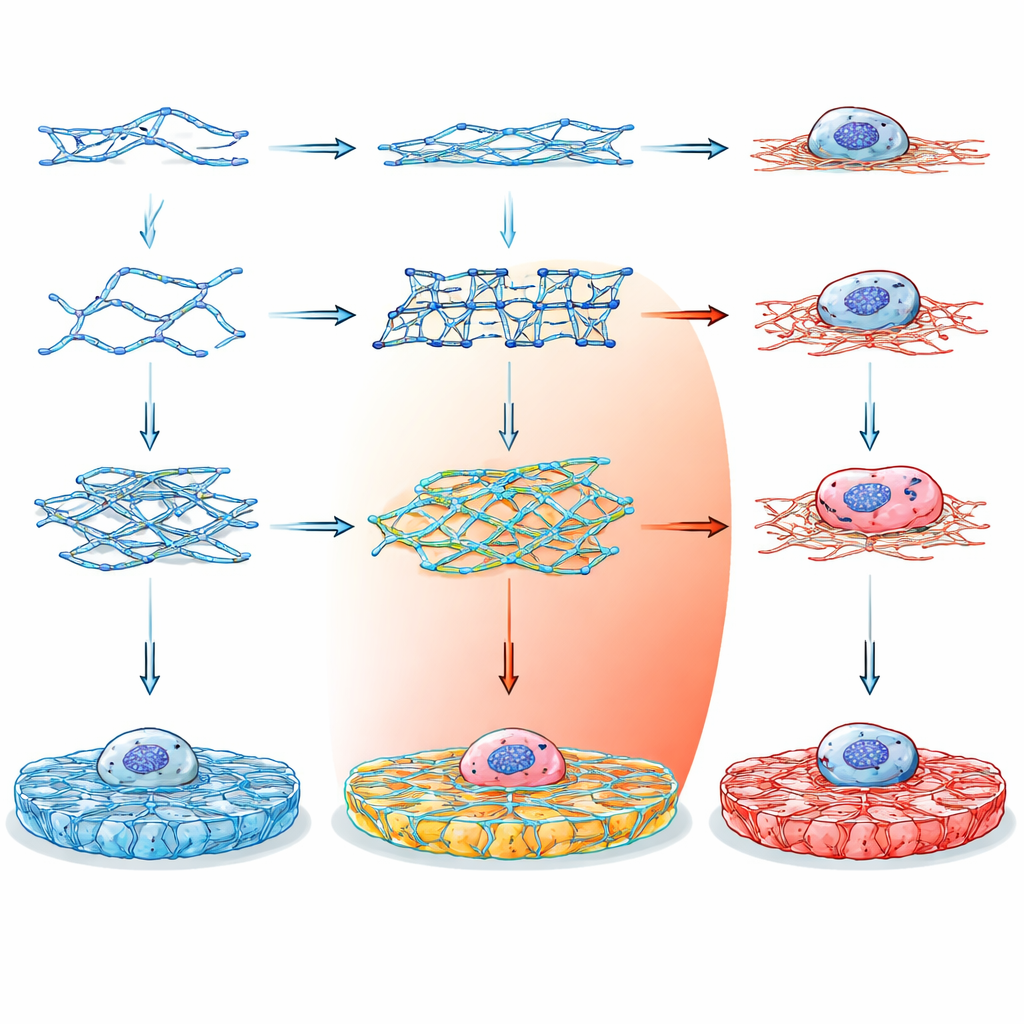
Du code génétique au gel intelligent
Plutôt que de s’appuyer sur des matériaux traditionnels comme le collagène ou l’alginate, difficiles à affiner sans additifs, les chercheurs ont choisi l’ADN comme matériau de construction. L’ADN est attrayant parce que ses règles d’assemblage sont simples et prévisibles : les bases complémentaires s’apparient de façons bien connues, permettant un contrôle précis de la forme et de la connectivité à l’échelle nanométrique. En concevant de courts brins d’ADN qui s’assemblent en jonctions multi-bras, l’équipe a pu programmer la manière dont les brins se relient pour former un hydrogel tridimensionnel — un solide mou rempli d’eau qui ressemble et se comporte comme un tissu biologique.
Concevoir une bibliothèque de gels sur mesure
L’équipe a créé quatorze blocs de construction d’ADN différents, regroupés en trois familles principales. Les motifs à double échange (DX) sont des unités relativement simples, en forme d’échelle ; les motifs paranémiques (PX) présentent des croisements plus fréquents, les rendant intrinsèquement plus rigides ; et les motifs de tensegrité forment des unités en étoile avec trois à six bras maintenus sous tension équilibrée. Certaines versions avaient des extrémités franches et ne pouvaient pas former de réseaux, servant de témoins. D’autres portaient des extrémités adhésives qui leur permettaient de s’accrocher pour former des gels étendus, soit avec des connexions palindromiques flexibles, soit avec des liaisons non palindromiques plus directionnelles. En choisissant soigneusement les séquences des brins et en vérifiant leur stabilité par des outils de calcul, les chercheurs se sont assurés que chaque motif se repliait comme prévu et restait biologiquement sûr.
Voir et ressentir les réseaux d’ADN
Pour confirmer que ces petits blocs de construction formaient bien des structures plus grandes, l’équipe a utilisé plusieurs techniques de visualisation et d’exploration mécanique. Des colorants fluorescents se liant à l’ADN ont révélé comment les différents motifs s’organisaient en réseaux au microscope : certains formaient des toiles lâches et agrégées, tandis que d’autres créaient des maillages plus réguliers et uniformes. La microscopie à force atomique a donné une vue à l’état sec à l’échelle nanométrique, montrant que les gels basés sur la tensegrité produisaient des fibres épaisses et en faisceaux qui, dans certains cas, ressemblaient au collagène naturel. En sondant délicatement les gels hydratés avec un cantilever microscopique et en réalisant des mesures rhéologiques en vrac, ils ont constaté que les gels couvraient une large plage de rigidités, d’environ 50 à 185 kilopascals, et restaient de type solide même sous des déformations bien supérieures à celles que subissent habituellement les tissus dans le corps.
Les cellules réagissent au paysage d’ADN
Le véritable test était de savoir si des cellules vivantes remarqueraient — et bénéficieraient de — ces environnements mécaniques conçus. Des cellules épithéliales pigmentaires rétiniennes humaines ont été cultivées sur des lamelles recouvertes des différents gels d’ADN et comparées à des revêtements standard tels que la poly-L-lysine, le collagène et des extraits commerciaux de membrane basale. Pour de nombreuses architectures et concentrations d’ADN, la viabilité cellulaire a augmenté, dans certains cas jusqu’à quatre fois par rapport au témoin mou en poly-L-lysine. Les cellules sur des gels d’ADN ajustés convenablement se sont davantage étalées, avec des surfaces plus grandes et des échafaudages internes d’actine mieux développés. Leurs noyaux se sont aussi élargis, un signe caractéristique d’une forte interaction avec leur environnement.
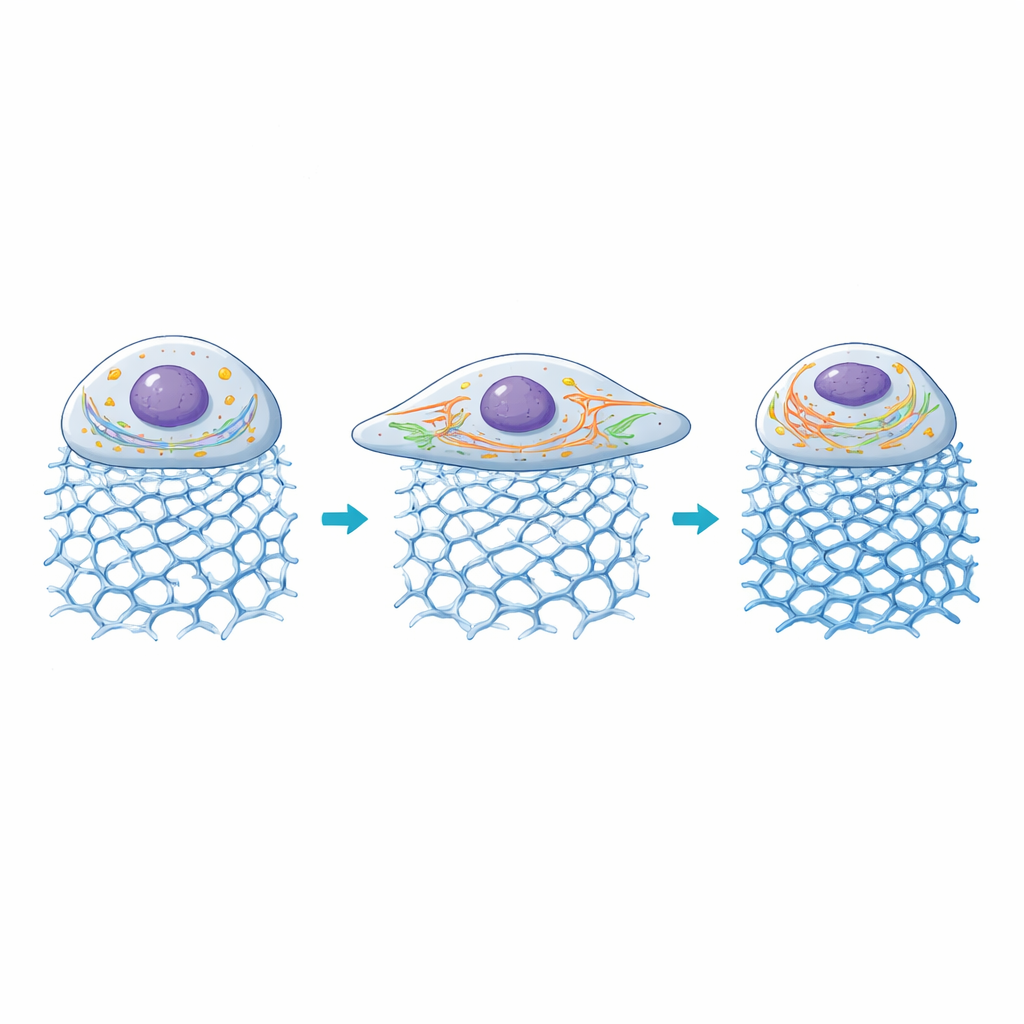
À l’intérieur de la cellule : adaptation des centrales et des voies de transport
Les chercheurs ont ensuite examiné la réaction de deux structures internes clés : les mitochondries, qui fournissent l’énergie, et le réticulum endoplasmique (RE), un réseau qui aide à traiter les protéines et les signaux calciques. Sur des gels de rigidité modérée, les mitochondries sont devenues plus fragmentées, un état associé à un turnover énergétique plus élevé durant une croissance active, tandis que les tubules du RE se sont allongés et sont devenus plus étendus dans le corps cellulaire agrandi. Lorsque la rigidité dépassait environ 100 kilopascals, la surface cellulaire a commencé à se réduire à nouveau, les réseaux mitochondriaux sont devenus plus fusionnés et les signaux du RE ont diminué, suggérant que des environnements très rigides poussent ces cellules hors de leur zone de confort. Globalement, les gels ont permis aux scientifiques de relier des architectures d’ADN et des niveaux de rigidité spécifiques à des schémas distincts d’organisation des organites et de signalisation mécanique.
Vers des échafaudages tissulaires personnalisés
Ce travail démontre que l’ADN peut servir non seulement de support d’information génétique, mais aussi de matériau de construction programmable pour créer des paysages à l’échelle cellulaire avec des propriétés mécaniques finement ajustées. En combinant différents motifs et séquences d’ADN, il devrait être possible de régler la rigidité et la structure nécessaires pour des types cellulaires ou des tissus particuliers, et même d’ajouter des éléments réactifs qui répondent aux changements de l’environnement. Ces hydrogels à base d’ADN ouvrent la voie à de futurs échafaudages personnalisés qui non seulement soutiennent les cellules en trois dimensions, mais guident aussi activement leur croissance, leur santé et leur réparation.
Citation: Singh, A., Yadav, A., Singh, N. et al. DNA cross-over motifs-based, programmable supramolecular hydrogels for the mechanoregulatory effects of cellular behaviour and cytoskeleton reorganization. npj Biomed. Innov. 3, 30 (2026). https://doi.org/10.1038/s44385-026-00083-9
Mots-clés: hydrogels d’ADN, mécanobiologie, génie tissulaire, mécanotransduction cellulaire, matrice extracellulaire